第二节 爱护水资源 知识点题库
(1)磷元素的原子结构示意图是 .
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2═6CaSiO3+P4O10 10C+P4O10═P4+10CO
每生成1molP4时,就有 mol电子发生转移.
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量.发生的反应为:C6H8O6+I2═C6H6O6+2H++2I﹣ 2S2O32﹣+I2═S4O62﹣+2I﹣
在一定体积的某维生素C溶液中加入a mol•L﹣1I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2 , 消耗b mol•L﹣1Na2S2O3溶液V2mL.该溶液中维生素C的物质的量是 mol.
II、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
(4)铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3•6H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是 .
(5)在某强酸性混合稀土溶液中加入H2O2 , 调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:
Ce3++ H2O2+ H2O═ Ce(OH)4↓+ .
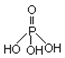
磷单质及其化合物在工业生产中有着广泛的应用.白磷可用于制备高纯度的磷酸(磷酸结构式如图),三聚磷酸钠(俗称“五钠”)是常用的水处理剂,次磷酸钠(NaH2PO2)可用于化学镀镍等.
-
(1) 磷元素原子核外最外层电子排布式为 .NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为
-
(2) 氧原子核外有 种不同能量的电子
-
(3) 写出与磷同周期的主族元素中,离子半径最小的元素,其最高价氧化物对应水化物的电离方程式
-
(4) 磷酸二氢钠主要用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂.其水溶液呈酸性的原因是
-
(5) 三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,其结构式为 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为
-
(6) 次磷酸钠(NaH2PO2)可用于化学镀镍.化学镀镍的溶液中含有Ni2+和H2PO2﹣ , 在一定条件下能发生如下反应: Ni2++ H2PO2﹣+ → Ni+ H2PO3﹣+ .请完成并配平该反应离子方程式.该反应的还原产物是
 HCO3-+OH- 热的纯碱溶液清洗油污
B . Al3++3H2O
HCO3-+OH- 热的纯碱溶液清洗油污
B . Al3++3H2O  Al(OH)3+3H+ 明矾净水
C . TiCl4+(x+2)H2O(过量)
Al(OH)3+3H+ 明矾净水
C . TiCl4+(x+2)H2O(过量)  TiO2·xH2O↓+4HCl 制备TiO2·xH2O
D . SnCl2+H2O
TiO2·xH2O↓+4HCl 制备TiO2·xH2O
D . SnCl2+H2O  Sn(OH)Cl+HCl 配制氯化亚锡溶液时加入氢氧化钠
Sn(OH)Cl+HCl 配制氯化亚锡溶液时加入氢氧化钠
 ]。下列说法正确的是( )
]。下列说法正确的是( ) 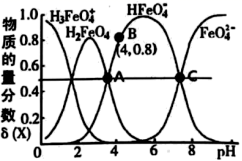
 H3FeO
H3FeO  (aq)的平衡常数K<100
D . K2FeO4起杀菌消毒作用是因为其遇水生成了Fe(OH)3胶体
(aq)的平衡常数K<100
D . K2FeO4起杀菌消毒作用是因为其遇水生成了Fe(OH)3胶体

-
(1) I.下列均为中学化学中常见的物质:①明矾、②氯化铁溶液、③水玻璃、④纯碱、⑤硅酸钠、⑥过氧化钠、⑦小苏打、⑧干冰。
属于电解质的有(填序号)。
-
(2) 写出⑥的电子式,利用上述物质证明碳酸酸性比硅酸强的化学方程式为。
-
(3) 明矾净水的原理是。
-
(4) II.在Na+浓度为0.5mol·L-1的某澄清溶液中,还可能含有K+、Ag+、Ba2+、
 、
、  、
、  等离子,取该溶液100mL进行下图连续实验(所加试剂均过量、气体全部逸出)。
等离子,取该溶液100mL进行下图连续实验(所加试剂均过量、气体全部逸出)。 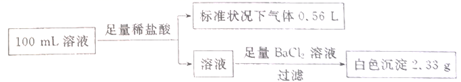
该溶液中除Na+外,肯定不存在的离子是(填离子符号,下同),肯定存在的离子是,可能存在的离子是。
-
(5) 若要确定可能存在的离子一定存在,必须满足的条件是。



