第一节 醇 酚 知识点题库
经元素质量分析测得乙醇的分子式是C2H6O.由于有机化合物普遍存在同分异构现象,根据价键理论,推测乙醇结构可能是图1两种之一:
为确定其结构,应利用物质的特殊性质进行定性、定量实验.现给出乙醇、钠、水等药品及必要的仪器,用如图2所示的装置进行实验确定乙醇的结构.某学生得到一组实验数据:
乙醇的用量(物质的量) | 产生氢气的体积(标准状况) |
0.10mol | 1.12L |

-
(1) 根据以上数据推断乙醇的结构应为 ,理由 (用化学方程式表示).
-
(2) 写出工业上以乙稀为原料制取乙醇的化学方程式
-
(3) 图2装置用来测量产生氢气的体积是否有误差? (答“有”或“无”)
下列关于乙醇和乙酸的说法中,正确的是( )
A . 乙醇和乙酸在一定条件下能发生酯化反应
B . 乙酸能溶于水,但不溶于乙醇
C . 乙醇和乙酸均能使紫色石蕊试液变红
D . 乙醇和乙酸分子中都含有C=O键
含苯酚的工业废水处理的流程图如图所示:

-
(1) 上述流程里,设备Ⅰ中进行的是操作(填操作名称),实验室里这一步操作可以用进行(填仪器名称).
-
(2) 由设备Ⅱ进入设备Ⅲ的物质A是,由设备Ⅲ进入设备Ⅳ的物质B是
-
(3) 在设备Ⅲ中发生反应的化学方程式为
-
(4) 在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和,通过操作(填操作名称)可使产物相互分离.
-
(5) 图中,能循环使用的物质是C6H6、CaO、.
下列物质中,不能使酸性KMnO4溶液褪色的物质是( )
① ![]() ②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH﹣COOH ⑥
②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH﹣COOH ⑥ ![]()
A . ①⑥
B . ①③④⑥
C . ①④
D . ①③⑥
可以证明乙醇分子中有一个氢原子与其他氢原子不同的方法是( )
A . 乙醇代替汽油作燃料,污染小,更环保
B . 1mol 乙醇燃烧生成3mol水
C . 1mol 乙醇与足量Na反应生成0.5 mol H2
D . 乙醇可以制饮料
模拟石油深加工合成CH2=CHCOOCH2CH3(丙烯酸乙酯)等物质的过程如下:

请回答下列问题:
-
(1) A能催熟水果,则A的名称为。
-
(2) B的结构简式为。
-
(3) 苯生成硝基苯的反应类型为。
-
(4) 石蜡油分解生成丙烯的同时,还会生成一种烷烃,该烷烃有种同分异构体。
-
(5) 写出由丙烯酸生成丙烯酸乙酯的化学方程式。
某二元醇的结构简式为  ,关于该有机物的说法错误的是( )
,关于该有机物的说法错误的是( )
 ,关于该有机物的说法错误的是( )
,关于该有机物的说法错误的是( )
A . 用系统命名法命名:5-甲基-2,5-庚二醇
B . 该有机物通过消去反应能得到6种不同结构的二烯烃
C . 该有机物可通过催化氧化得到醛类物质
D . 1mol 该有机物能与足量金属 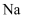 反应产生
反应产生 
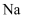 反应产生
反应产生 
春季复工复学后,做好防护是控防新型冠状病毒传播的有效措施。下列说法正确的是( )
A . 为减少直接吸入飞沫形成的气溶胶感染病毒的几率,就餐时人人间距至少应为1米
B . 生产医用口罩的主要原料聚丙烯(PP)属于天然高分子化合物
C . 95%的乙醇溶液、84消毒液可直接用作环境消毒剂
D . 40%的甲醛溶液可做公共餐具消毒剂
下列实验装置或操作与实验目的不相符的是( )
| | | | |
| A.证明Cl2氧化性强于Br2 | B.除去乙醇中的乙酸 | C.用海水制取蒸馏水 | D.配制100mL0.1mol/LNaCl溶液 |
A . A
B . B
C . C
D . D
常用的食品抗氧化剂BHT的合成方法如下图所示(假设原料均能恰好完全反应):

下列说法中错误的是( )
A . 方法一的原子利用率为100%
B . 方法二属于取代反应
C . X与Y均能与 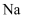 、
、  溶液、溴水发生反应
D .
溶液、溴水发生反应
D .  在稀
在稀  条件下发生消去反应可生成
条件下发生消去反应可生成 
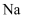 、
、  溶液、溴水发生反应
D .
溶液、溴水发生反应
D .  在稀
在稀  条件下发生消去反应可生成
条件下发生消去反应可生成 
-
(1) I.乳酸在多种生物化学过程中起着重要作用,酸牛奶中含有乳酸,其结构简式如图所示:

下列物质与乳酸互为同系物的是,与乳酸互为同分异构体的是。
①
 ②
②  ③
③  ④
④ 
-
(2) 研究人员在珠峰山顶发现了“微塑料”,这是目前地球上发现塑料污染海拔最高的地方。聚乳酸(PLA)可微生物降解,是理想的绿色高分子材料,可以代替塑料制品减少“微塑料”带来的环境污染。写出用乳酸制取聚乳酸的化学方程式。
-
(3) II.当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子,则B中手性碳原子的个数为;若使A失去手性,则采取的方法为(用化学方程式表示)。

1,2-二溴乙烷可作汽油抗爆剂添加剂,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。

有关数据如下:
| 乙醇 | 1,2-溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g∙cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
-
(1) 在此制备实验中,要尽可能迅速把反应温度升高到170℃左右,最主要目的是(填正确选项前的字母)。
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
-
(2) 写出本题中制备1,2-二溴乙烷的两个化学反应方程式:;。
-
(3) 容器c中
 溶液的作用是。
溶液的作用是。
-
(4) 判断该制备反应已经结束的最简单方法是。
-
(5) 将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”)。
-
(6) 若产物中有少量副产物乙醚,可用的方法除去。
A、B、C、D、E、F、G均为有机物,其中A是常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系。请回答下列问题:

-
(1) 写出A、D、G的结构简式:A; D; G。
-
(2) A、B中官能团的名称:A; B。
-
(3) 在F的同系物中最简单的有机物的空间构型为。
-
(4) 与F互为同系物且含有5个碳原子的同分异构体共有种。
-
(5) 写出下列编号对应反应的化学反应方程式,并注明反应类型:
①、反应;
②、反应;
④、反应。
我国科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理学或医学奖。已知二羟甲戊酸(如图)是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法中正确的是( )

A . 与乙醇发生酯化反应生成产物的分子式为C8H18O4
B . 能发生加成反应,不能发生取代反应
C . 在铜的催化下与氧气反应的产物含有醛基
D . 标准状况下,1mol该有机物可以与足量金属钠反应产生22.4LH2
下列物质中,不属于烃的衍生物的是( )
A . 乙醇
B . 甲烷
C . 乙酸
D . 一氯甲烷
羟甲香豆素(Z)是一种治疗胆结石的药物。其合成涉及如下转化:

下列有关说法正确的是( )
A . Y的分子式为C10H8O4
B . X分子中不含有手性碳原子
C . 1 mol Y与足量NaOH溶液反应,最多消耗3 mol NaOH
D . 1 mol Z与足量浓溴水反应,只发生加成反应消耗1 mol Br2
化学与生产、生活联系密切。下列有关说法错误的是( )
A . 光导纤维的主要成分是二氧化硅
B . 乙醇用作消毒剂,主要是利用其强氧化性
C . “臭氧空洞”的形成与氮氧化合物和氟氯烃的排放有关
D . 电动汽车的推广使用,有效地减少了温室气体的排放
下列说法错误的是( )
A . 乙酸分子中羧基上的氢原子较乙醇中羟基上的氢原子更活泼
B . 乙醇能与钠反应放出氢气,说明乙醇能电离出H+而表现酸性
C . 用金属钠分别与水和乙醇反应,可比较水分子中氢原子和乙醇羟基中氢原子的活泼性
D . 食醋浸泡水垢,可比较乙酸和碳酸的酸性强弱
实验室制取乙烯的装置如图Ⅰ所示。根据实验及有关操作回答下列问题。

-
(1) 甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:。
-
(2) 乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:

①Ⅱ装置abcd中可盛放的试剂的顺序依次是(填序号)。
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是。
-
(3) 丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。

①图Ⅲ中装置a的作用是。
②为除去混合气中的SO2和CO2 , 装置b中应该盛放的试剂是。
③浓溴水的作用是。
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是。
下列关于有机物的说法正确的是( )
A . 医用酒精为无水乙醇
B . 苯可以使酸性高锰酸钾溶液褪色
C . 蛋白质能发生水解转化为氨基酸
D . 乙烯与氯化氢加成得到氯乙烯
最近更新







