课题二 身边化学问题的探究 知识点题库
;
纯碱溶液呈碱性的原因是(用离子方程式表示) .
(2)为探究纯碱溶液呈碱性是由CO32﹣引起的,请你设计一个简单的实验方案: .
(3)为证明盐的水解是吸热反应,四位学生分别设计了如下方案,其中正确的是 .
A.甲学生:在醋酸钠溶液中滴入2滴酚酞,加热后红色加深,说明盐类水解是吸热反应
B.乙学生:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热反应
C.丙学生:将硝酸铵晶体溶于水,水温下降,说明盐类水解是吸热反应
D.丁学生:在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热反应.
选项 | 实验操作 | 现象 | 结论 |
A | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 | 测定醋酸钠溶液pH |
B | 向盐酸中滴入少量NaAlO2溶液 | 无明显现象 | AlO2-与H+未发生反应 |
C | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
D | 蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液可能是浓盐酸 |

-
(1) 25℃时,CH3COOH和NH3×H2O的电离常数相等。取10mL0.1mol×L-1醋酸溶液测得其pH=3。0.1mol×L-1氨水(NH3×H2O溶液)的pH=。用pH试纸测定该氨水pH的操作方法为。
-
(2) 某温度(t℃)时,测得0.01 mol×L-1的NaOH溶液的pH=11,则该温度下水的KW=。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合,若所得混合液为中性,且a+b=12,则Va: Vb。
-
(3) 25℃时,0.1 mol×L-1的HA溶液中
 。请回答下列问题:
。请回答下列问题: ①HA是(填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是(填字母)。
a.c(HA) b.
 c.c(H+)与c(OH-)的乘积 d.c(OH-)
c.c(H+)与c(OH-)的乘积 d.c(OH-)


| 目的 | 操作 | |
| A | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点滴于试纸的中部,与标准比色卡对比 |
| B | 验证Ksp(AgCl)>Ksp( AgI) | 取2 mL0. 1mol·L-1AgNO3溶液,先后滴加3滴0.1mol·L-1NaCl溶液和5滴0.1mol·L-1KI溶液,先生成白色沉淀,后又产生黄色沉淀 |
| C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴人BaCl2溶液,观察溶液的变化 |
| D | 检验Fe(NO3)2晶体是否已 氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;
②测定新制氯水的  时,先用玻璃棒蘸取液体滴在
时,先用玻璃棒蘸取液体滴在  试纸上,再与标准比色卡对照;
试纸上,再与标准比色卡对照;
③用米汤直接检验食用盐中是否含有碘元素;
④  在5.6~7.0之间的降水通常称为酸雨;
在5.6~7.0之间的降水通常称为酸雨;
⑤加入 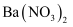 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有
溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有  存在;
存在;
⑥  通入紫色石蕊试液,溶液先变红后褪色;
通入紫色石蕊试液,溶液先变红后褪色;
⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便转移到容量瓶中,导致结果偏高;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤;
⑨蒸干 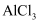 溶液可得纯净的无水氯化铝;
溶液可得纯净的无水氯化铝;



