课题2 获取安全的饮用水 知识点题库
某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质.利用拜耳法生产氧化铝的流程如图所示:

(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是 .
(2)AlO(OH)与NaOH反应的化学方程式为 .
(3)在稀释、结晶过程中:稀释的目的是 ;加Al(OH)3晶核的目的是促进Al(OH)3的析出.上述“稀释、结晶”工艺,也可用通入足量的 气体的方法来代替.
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式: .
(5)该生产流程能实现 (填化学式)的循环利用.
 、Ca2+、NO
、Ca2+、NO  、HCO
、HCO  B . 强碱性溶液中:NH
B . 强碱性溶液中:NH  、Al3+、HCO
、Al3+、HCO  、NO
、NO  C . 在强碱溶液中:Na+、K+、Cl﹣、CO
C . 在强碱溶液中:Na+、K+、Cl﹣、CO  D . 在无色溶液中:K+、H+、Cl﹣、MnO
D . 在无色溶液中:K+、H+、Cl﹣、MnO 
-
(1) 下列实验基本操作或说法正确的是(填写序号)
A.金属钠着火时使用泡沫灭火器灭火
B.为了有效地除去粗盐中的Ca2+ 、Mg2+ 、SO42- , 可先加入NaOH,再加入BaCl2 , 最后加入Na2CO3 , 将沉淀过滤后,再用HCl调整溶液至中性
C.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可
D.稀释浓硫酸时,应将水沿器壁缓缓加入浓硫酸中,并不断用玻璃棒搅拌
E.容量瓶中含有少量蒸馏水,对配制一定物质的量浓度的硫酸溶液无影响
F.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
G.在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒
H.用试管加热碳酸氢钠固体时使试管口竖直向上
-
(2) 有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为无色溶液;②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生。③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
根据以上实验现象可知,该白色固体中一定含有,(填化学式,下同)一定不含有,可能含有。
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
综合上述实验,你认为以下结论正确的是( )
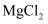 和
和 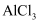 各
各  ,向其中逐滴滴加
,向其中逐滴滴加 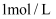 的
的  溶液至过量,下列关系图象正确的是( )
溶液至过量,下列关系图象正确的是( )
 B .
B .  C .
C .  D .
D . 
|
选项 |
表述Ⅰ |
表述Ⅱ |
|
A |
Cl2有强氧化性 |
氯水可使石蕊试液最终褪色 |
|
B |
SiO2具有弱氧化性 |
工业上利用SiO2与焦炭制备高纯硅 |
|
C |
白色沉淀Ag2CO3可与硝酸反应而溶解 |
检验Cl-时用稀硝酸酸化的AgNO3溶液 |
|
D |
Fe3+有氧化性 |
用KSCN溶液可以鉴别Fe3+ |
| 选项 | 实验操作和现象 | 结论 |
| A | 强酸性溶液X中加入Ba(NO3)2溶液,静置后再加入KSCN溶液,先生成白色沉淀,后溶液变红 | 溶液X中一定含有 |
| B | 检验HCl气体中是否含有Cl2 , 将气体通入品红溶液中,品红溶液褪色,加热后溶液不恢复成红色 | HCl气体中含有Cl2 |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的还原性比I2强 |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结 | NH4Cl固体易升华 |
 B . 能使酚酞变红的溶液中:
B . 能使酚酞变红的溶液中:  C . 0. 1 mol·L−1KI 溶液:
C . 0. 1 mol·L−1KI 溶液:  D . 常温下,
D . 常温下,  的溶液中:
的溶液中: 
-
(1) 除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为
-
(2) 某同学在实验室用铝土矿(含有
 和
和  ,不考虑其他杂质)取金属铝的流程如下:
,不考虑其他杂质)取金属铝的流程如下: 
①操作Ⅰ所加物质a为(选填
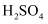 或NaOH),
或NaOH),  与a反应的离子方程式为。
与a反应的离子方程式为。②滤液Ⅱ中溶质的用途之一是。
③工业上在电解熔融的
 时,还加入了冰晶石
时,还加入了冰晶石  作熔剂,其作用是降低
作熔剂,其作用是降低  的熔点。冰晶石在物质的分类中属于(填字母)。
的熔点。冰晶石在物质的分类中属于(填字母)。a.酸 b.碱 c.盐 d.氧化物
-
(3) 铝与
 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中  的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将  还原为
还原为  ,完善并配平该反应:
,完善并配平该反应:  ,。每消耗
,。每消耗  ,转移的电子数目为。
,转移的电子数目为。
-
(4) 已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化
 ,也能氧化
,也能氧化  。
。 ①取
 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4 , 振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4 , 振荡后,下层为无色液体。以上实验结论表明还原性: 
 (填“>”或“<”)。
(填“>”或“<”)。②若在
 溶液中通入标准状况下672mL的Cl2 , 取少量反应后的溶液加入CCl4 , 振荡后下层液体呈色,写出该反应的离子方程式。
溶液中通入标准状况下672mL的Cl2 , 取少量反应后的溶液加入CCl4 , 振荡后下层液体呈色,写出该反应的离子方程式。
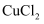 和
和  的混合溶液中加入少量的
的混合溶液中加入少量的 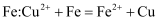 B . 碱性锌锰干电池的正极反应式:
B . 碱性锌锰干电池的正极反应式: 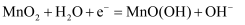 C . 向
C . 向  溶液中加少量
溶液中加少量 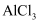 溶液:
溶液: 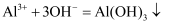 D . 磁性氧化铁溶于浓硝酸:
D . 磁性氧化铁溶于浓硝酸: 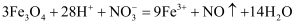
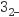 、SO
、SO B . Cu2+、SO
B . Cu2+、SO 、HCO
、HCO 、Na+
C . Cu2+、SO
、Na+
C . Cu2+、SO 、NO
、NO 、Fe3+
D . OH-、Na+、Mg2+、SO
、Fe3+
D . OH-、Na+、Mg2+、SO
 溶液:
溶液: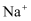 、
、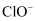 、
、 、
、 B .
B .  溶液:
溶液: 、
、 、
、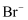 、
、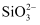 C .
C . 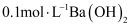 溶液:
溶液: 、
、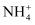 、
、 、
、 D .
D .  溶液:
溶液: 、
、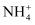 、
、 、
、
 和Fe3+
和Fe3+


