第三节 盐类的水解 知识点题库
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:

(1)相同条件下,0.1mol•L﹣1NH4Al(SO4)2中c(NH4+) (填“等于”、“大于”或“小于”)0.1mol•L﹣1NH4HSO4中c(NH4+).
(2)如图1是0.1mol•L﹣1电解质溶液的pH随温度变化的图象.
①其中符合0.1mol•L﹣1NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母);
②20℃时,0.1mol•L﹣1NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)= mol•L﹣1 . (不做近似计算)
(3)室温时,向100mL 0.1mol•L﹣1NH4HSO4溶液中滴加0.1mol•L﹣1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 .
实验室在配制Na2CO3溶液时,为了抑制水解应向溶液中加入少量的 .
将0.1mol/L的AlCl3溶液加热、蒸干、灼烧最后得到的固体是( )
A . Al
B . Al(OH)3
C . AlCl3
D . Al2O3
在25℃时,某稀溶液中由水电离产生的c(OH﹣)=10﹣10 mol•L﹣1 . 下列有关该溶液的叙述正确的是( )
A . 该溶液一定呈酸性
B . 该溶液中c(H+)可能等于10﹣5 mol•L﹣1
C . 该溶液的pH可能为4也可能为10
D . 该溶液有可能呈中性
下列关于醋酸钠溶液的说法中正确的是( )
A . 溶液呈酸性
B . c(H+)=c(CH3COO﹣)+c(OH﹣)
C . c(Na+)>c(CH3COO﹣)>c(OH﹣)>c(H+)
D . c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)
已知c(NH4Cl)<0.1mol•L﹣1时,溶液的pH>5.1,现用0.1mol•L﹣1盐酸滴定10mL 0.05mol•L﹣1氨水,用甲基橙作指示剂,达到终点时所用盐酸的量应是( )
A . 10 mL
B . 5 mL
C . 大于5 mL
D . 小于5 mL
常温下,向100mL 0.01mol•L﹣1 HA溶液中逐滴加入0.02 mol•L﹣1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,不正确的是( )
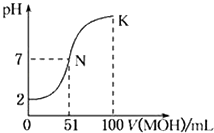
A . HA为一元强酸
B . MOH为一元弱碱
C . N点水的电离程度小于K点水的电离程度
D . K点对应的pH=10,则有c(MOH)+c(OH﹣)﹣c(H+)=0.005mol•L﹣1
对于下列四幅图象的表述正确的是( )
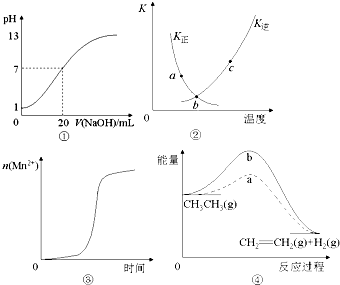
A . 图①表示25℃时,用0.1 mol•L﹣1NaOH溶液滴定20 mL 0.1 mol•L﹣1盐酸溶液,溶液的pH随加入NaOH溶液体积的变化
B . 图②中表示反应2SO2(g)+O2(g)⇌2SO3(g);△H<0的有关曲线,图中a.b.c三点中只有b点已经达到化学平衡状态.
C . 图③表示10 mL 0.01 mol•L﹣1KMnO4酸性溶液与过量的0.1 mol•L﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用)
D . 图④中a、b曲线分别表示反应CH3CH3→CH2=CH2(g)+H2(g);△H>0使用和未使用催化剂时,反应过程中的能量变化
已知25℃时,CH3COONH4溶液呈中性.
-
(1) Ⅰ.将0.1mol•L﹣1的CH3COOH溶液与0.1mol•L﹣1的NaOH溶液等体积混合(混合溶液的体积变化忽略不计),测得混合溶液的pH=9.回答下列问题:
用离子方程式表示混合溶液的pH=9的原因.
-
(2) 混合后溶液中c(CH3COOH)=mol•L﹣1(填写精确值).
-
(3) 相同温度相同浓度的下列四种溶液:①(NH4)2CO3②CH3COONH4③(NH4)2SO4④NH4Cl,pH由大到小的排列顺序为(填序号).
-
(4) Ⅱ.Mg(OH)2沉淀可溶解于NH4Cl溶液.同学对有关该反应的原理的解释如下:甲同学认为是NH4Cl水解,溶液呈酸性,H+中和了Mg(OH)2电离出的OH﹣导致沉淀溶解;乙同学认为是NH4+与Mg(OH)2电离出的OH﹣反应生成弱电解质NH3•H2O,导致沉淀溶解.
丙同学不能肯定哪位同学的解释合理,于是选用下列一种试剂来验证甲、乙两同学的观点,他选用的试剂是
A . NH4NO3 B . CH3COONH4 C . Na2CO3 D . NH3•H2O -
(5) 丙同学选择该试剂的理由是:.
-
(6) 丙同学将所选试剂滴加到Mg(OH)2悬浊液中,Mg(OH)2溶解,由此可知:(填“甲”或“乙”)的解释更合理.Mg(OH)2沉淀与NH4Cl溶液反应的离子方程式为:.
-
(7) 现有Mg(OH)2和Al(OH)3沉淀的混合物,若除去Mg(OH)2得到纯净的Al(OH)3 , 可用(填写所用试剂的化学式,试剂从本题涉及的试剂中选取,下同);若除去Al(OH)3得到纯净的Mg(OH)2 , 可用.
常温下,向20mL 0.5mol•L﹣1的CH3COOH溶液中逐滴滴加0.5mol•L﹣1的NaOH溶液,滴定曲线如图.相关分析正确的是( )

A . 滴加至①时,c(Na+)=c(CH3COO﹣),酸碱恰好完全反应
B . 滴加至②时,c(OH﹣)﹣c(H+)=c(CH3COOH)
C . 滴定中,  逐渐减小
D . 滴定中.c(CH3COOH)与c(CH3 C00﹣)之和保持不变
逐渐减小
D . 滴定中.c(CH3COOH)与c(CH3 C00﹣)之和保持不变
 逐渐减小
D . 滴定中.c(CH3COOH)与c(CH3 C00﹣)之和保持不变
逐渐减小
D . 滴定中.c(CH3COOH)与c(CH3 C00﹣)之和保持不变
过氧化钙,化学式为CaO2 , 微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。现有一种制备过氧化钙的实验方案,流程如下图,其主要反应的化学方程式为:CaCl2+2NH3·H2O+H2O2=CaO2↓+2NH4Cl+2H2O表示。回答下列问题:

-
(1) 步骤①中,加入氨水的目的是,小火煮沸的作用是。
-
(2) 步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体;再将溶液煮沸,趁热过滤。此过程中,将溶液煮沸的作用是。
-
(3) 制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到产品。此法工艺简单、操作方便,但是得到的产品纯度较低,往往CaCO3、Ca(OH)2等杂质含量较高。若实验室只提供稀盐酸和澄清石灰水两瓶试剂,以及试管、小烧杯、胶头滴管、药匙各1个,请设计实验检验所得产品中含有CaCO3。(简要描述方案即可)。
25oC时,浓度均为0.1 mol·L–1的几种溶液的pH如下:
| 溶液 | ①CH3COONa溶液 | ②NaHCO3溶液 | ③CH3COONH4溶液 |
| pH | 8.88 | 8.33 | 7.00 |
下列说法错误的是( )
A . ①中, c(Na+) = c(CH3COO–) + c( CH3COOH)
B . 由①②可知,CH3COO–的水解程度大于  的水解程度
C . ③中,c(CH3COO–) = c(NH4+) < 0.1 mol·L–1
D . 推测25oC,0.1 mol·L–1 NH4HCO3溶液的pH <8.33
的水解程度
C . ③中,c(CH3COO–) = c(NH4+) < 0.1 mol·L–1
D . 推测25oC,0.1 mol·L–1 NH4HCO3溶液的pH <8.33
 的水解程度
C . ③中,c(CH3COO–) = c(NH4+) < 0.1 mol·L–1
D . 推测25oC,0.1 mol·L–1 NH4HCO3溶液的pH <8.33
的水解程度
C . ③中,c(CH3COO–) = c(NH4+) < 0.1 mol·L–1
D . 推测25oC,0.1 mol·L–1 NH4HCO3溶液的pH <8.33
下列说法错误的是( )
A . 0.1mol/L 的硫酸铵溶液中:C(NH  )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
 )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
25℃时,向10mL 0.1 mol∙L−1一元弱碱XOH溶液中逐滴滴加0.1 mol∙L−1的HCl溶液,溶液的变化  如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是( )
如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是( )
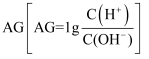 如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是( )
如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是( ) 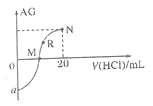
A . a的最小值是−12
B . M点消耗盐酸的体积为10mL
C . R点溶液中可能存在 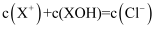 D . M点到N点,水的电离程度逐渐增大
D . M点到N点,水的电离程度逐渐增大
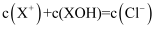 D . M点到N点,水的电离程度逐渐增大
D . M点到N点,水的电离程度逐渐增大
CH3COONa溶液是常见的强碱弱酸盐,可由醋酸和NaOH溶液反应得到。
-
(1) CH3COONa水溶液呈(填“酸”或“碱”)性。
-
(2) CH3COONa在溶液中发生水解反应的离子方程式是。
-
(3) 用0.1000 mol/L NaOH分别滴定25.00mL 0.1000 mol/L盐酸和25.00 ml 0.1000mol/L醋酸,滴定过程中pH变化曲线如下图所示。
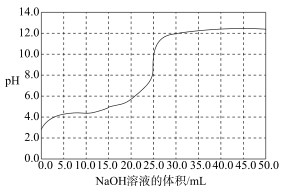
①在上述滴定过程中,不需要使用的玻璃仪器(填序号)。
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
②由图中数据可判断滴定盐酸的pH变化曲线如图,判断的理由如下(答出2点):

i.起始未滴加NaOH溶液时,。
ii.。
③滴定CH3COOH溶液的过程中,当滴加12.50mL NaOH溶液时,溶液中各离子浓度由大到小的顺序是(用符号“c”及“>”表示)。
-
(4) 向0.1 mol/ L CH3COONa溶液中逐滴加入0.1mol/L盐酸至恰好反应。反应过程中,你认为 CH3COONa的水解平衡向(填“左”或“右”)移动,分析的过程:当滴入稀盐酸后,。
室温下,向10.00 mL0.1000 mol/LNaHCO3溶液中滴加0.1000 mol/L的盐酸,溶液的pH随加入的盐酸的体积V变化的曲线如图所示(已知室温下H2CO3的电离平衡常数: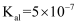 ,
,  。忽略混合时溶液体积和温度的变化)。下列说法正确的是( )
。忽略混合时溶液体积和温度的变化)。下列说法正确的是( )
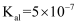 ,
,  。忽略混合时溶液体积和温度的变化)。下列说法正确的是( )
。忽略混合时溶液体积和温度的变化)。下列说法正确的是( )
A . a点时,对于反应 , 反应达到平衡状态时,平衡常数
, 反应达到平衡状态时,平衡常数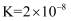 B . b点溶液中的全部溶质为NaHCO3和NaCl
C . c点溶液中,c(Na+)>c(
B . b点溶液中的全部溶质为NaHCO3和NaCl
C . c点溶液中,c(Na+)>c( )>c(Cl-)>c(H+)>c(OH-)
D . d点溶液中存在
)>c(Cl-)>c(H+)>c(OH-)
D . d点溶液中存在
 , 反应达到平衡状态时,平衡常数
, 反应达到平衡状态时,平衡常数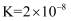 B . b点溶液中的全部溶质为NaHCO3和NaCl
C . c点溶液中,c(Na+)>c(
B . b点溶液中的全部溶质为NaHCO3和NaCl
C . c点溶液中,c(Na+)>c( )>c(Cl-)>c(H+)>c(OH-)
D . d点溶液中存在
)>c(Cl-)>c(H+)>c(OH-)
D . d点溶液中存在
向盛有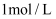
 溶液的烧杯中,加入少量氨水,再加入过量Mg粉,有大量气泡产生。将湿润的红色石蕊试纸放在烧杯口,试纸变蓝。溶液的pH随时间的变化如图。
溶液的烧杯中,加入少量氨水,再加入过量Mg粉,有大量气泡产生。将湿润的红色石蕊试纸放在烧杯口,试纸变蓝。溶液的pH随时间的变化如图。
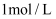
 溶液的烧杯中,加入少量氨水,再加入过量Mg粉,有大量气泡产生。将湿润的红色石蕊试纸放在烧杯口,试纸变蓝。溶液的pH随时间的变化如图。
溶液的烧杯中,加入少量氨水,再加入过量Mg粉,有大量气泡产生。将湿润的红色石蕊试纸放在烧杯口,试纸变蓝。溶液的pH随时间的变化如图。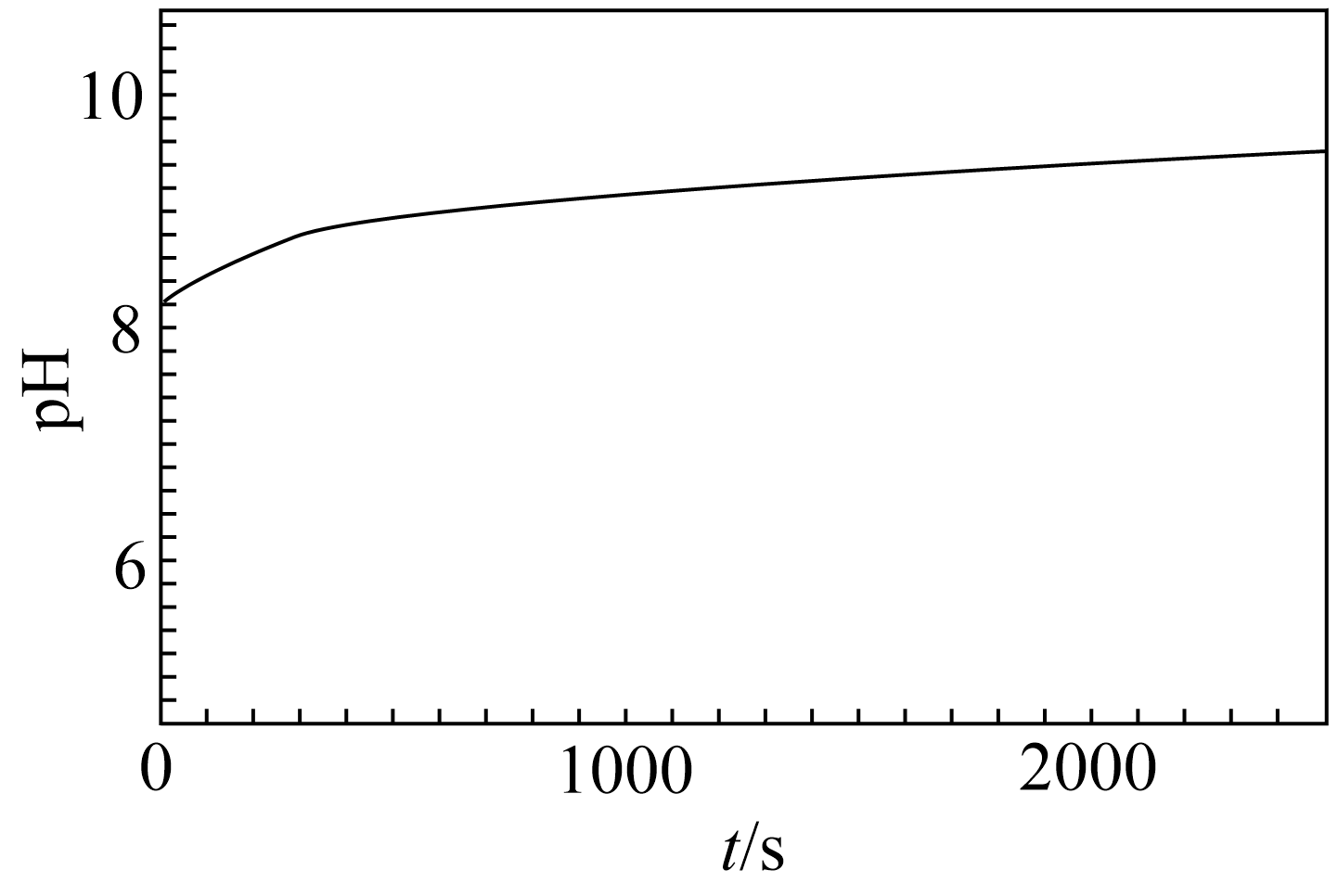
下列说法不正确的是( )
A . 随着反应的进行, 降低
B . 产生的气体是混合物
C . pH=9时,溶液中
降低
B . 产生的气体是混合物
C . pH=9时,溶液中 D . 溶液的pH升高可能是Mg与
D . 溶液的pH升高可能是Mg与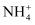 、
、 反应的结果
反应的结果
 降低
B . 产生的气体是混合物
C . pH=9时,溶液中
降低
B . 产生的气体是混合物
C . pH=9时,溶液中 D . 溶液的pH升高可能是Mg与
D . 溶液的pH升高可能是Mg与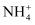 、
、 反应的结果
反应的结果
常温下,下列溶液中水的电离程度大于纯水的电离程度的是( )
A . 0.1mol·L-1盐酸
B . 0.1mol·L-1NaOH溶液
C . 0.1mol·L-1NH4Cl溶液
D . 0.1mol·L-1NaHSO4溶液
水溶液呈碱性的盐是( )
A .  B .
B .  C .
C .  D .
D . 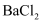
 B .
B .  C .
C .  D .
D . 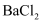
电导率是衡量电解质溶液导电能力大小的物理量。室温下,用 的
的 滴定10.00mL浓度均为
滴定10.00mL浓度均为 的NaOH和
的NaOH和 的混合溶液,所得电导率曲线如图所示。已知
的混合溶液,所得电导率曲线如图所示。已知 ,
,  , 下列说法错误的是( )
, 下列说法错误的是( )
 的
的 滴定10.00mL浓度均为
滴定10.00mL浓度均为 的NaOH和
的NaOH和 的混合溶液,所得电导率曲线如图所示。已知
的混合溶液,所得电导率曲线如图所示。已知 ,
,  , 下列说法错误的是( )
, 下列说法错误的是( )
A . a点的混合溶液中: 约为
约为 B . b点的混合溶液中:
B . b点的混合溶液中: C . c点的混合溶液中:
C . c点的混合溶液中: D . a点→c点过程中,溶液中水的电离程度一直增大
D . a点→c点过程中,溶液中水的电离程度一直增大
 约为
约为 B . b点的混合溶液中:
B . b点的混合溶液中: C . c点的混合溶液中:
C . c点的混合溶液中: D . a点→c点过程中,溶液中水的电离程度一直增大
D . a点→c点过程中,溶液中水的电离程度一直增大
最近更新



