第三单元 物质的分散系 知识点题库
某固体化合物A不导电,但熔化或溶于水都能完全电离,下列关于A的说法中正确的是
A . A为非电解质
B . A是强电解质
C . A是分子晶体
D . A为弱电解质
下列有关溶液的说法不正确的是( )
A . 溶液由溶质和溶剂组成,所以每种溶液里只有两种物质
B . 硫酸钠溶液能导电是因为溶液中含有较多自由移动的离子
C . 配置0.09%的生理盐水的一般步骤是计算、称量和溶解
D . 在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中
在一定温度下,向饱和烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温度,下列说法正确的是( )
A . 溶液中Na+浓度增大,有O2放出
B . 溶液pH值不变,有H2放出
C . 溶液中Na+数目减少,有O2放出
D . 溶液中pH值增大,有O2放出
往蛋白质溶液里加入下列物质会产生沉淀,但再加水稀释,沉淀又会溶解的是( )
A . CuSO4
B . (NH4)2SO4
C . H2SO4
D . 酒精
下列中学课本中涉及的实验,需要通电才能完成的是( )
① 电解质的电离 ②工业上合成氨 ③证明氢氧化铁胶粒带正电
④ 冶炼大量铝 ⑤ 钢铁的吸氧腐蚀
A . ①⑤
B . ③④
C . ①③⑤
D . 全部
下列关于纯净物、混合物、电解质、非电解质的正确组合为 ( )

A . A
B . B
C . C
D . D
下列有关概念和原理的说法正确的是( )
A . 酸和碱反应只能生成盐和水
B . 由14N和中子在宇宙射线影响下形成12C 为化学变化: 14N+1n→ 12C+ 3H
C . 金属主要发生吸氧腐蚀,其本质是被氧化
D . Na2O2的水溶液能导电,所以Na2O2是电解质
下列关于胶体的叙述错误的是( )
A . 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间
B . 胶体和溶液一样,其分散质可透过滤纸
C . 用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D . Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
离子反应是中学化学中重要的反应类型,在发生离子反应的反应物或生成物中,一定存在:( )
①单质;②氧化物;③电解质;④盐;⑤化合物
A . ①②
B . ③⑤
C . ④⑤
D . ①②④
下列反应过程中溶液的导电性有显著变化的是( )
A . 向NaOH溶液中滴加相同浓度的醋酸至完全中和
B . 向Ba(OH)2溶液中滴加相同浓度的盐酸至完全中和
C . 向Ba(OH)2溶液中滴加相同浓度的稀硫酸至沉淀完全
D . 向BaCl2溶液中滴加相同浓度的硝酸银溶液至沉淀完全
化学与生活、社会发展息息相关,下列有关说法错误的是( )
A . “时气错逆,霾雾蔽日”,雾所形成的气溶胶能产生丁达尔效应
B . “青蒿一握,以水二升渍,绞取汁”;屠呦呦改进提取青蒿素的方法,提取过程中发生了化学变化
C . 刘禹锡的“千淘万漉虽辛苦,吹尽狂沙始到金”可以看出金性质稳定,可通过物理方法得到
D . “外观如雪,强烧之,紫青烟起”。对硝酸钾的鉴定过程中利用了焰色反应
今有10种物质:①Na ②稀硝酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2 ⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
-
(1) 能导电的物质;(用序号填空,下同)
-
(2) 电解质,但熔融状态下并不导电。
-
(3) 强电解质;
-
(4) 非电解质;
-
(5) 区分Fe(OH)3胶体和FeCl3溶液实验方法(具体操作);
-
(6) 写出②和⑨反应的离子方程式。
-
(7) 向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现,原因:,随后,原因(用离子方程式表示)。
现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向氯化铁溶液中加入少量的NaOH溶液;
II.乙同学向沸水中滴加饱和氯化铁溶液后,长时间加热;
III.丙同学向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
-
(1) 其中操作正确的同学是;他的操作中涉及到的制备胶体的离子反应方程式为。
-
(2) 判断胶体制备是否成功,可利用胶体的。
-
(3) 丁同学将所制得的Fe(OH)3胶体分成两份,并进行下列实验:
①将其中一份装入U形管内,用石墨作电极,接通直流电,通电一段时 间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶体粒子带(填“正”或“负”)电荷。
②向另一份Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a.先出现红褐色沉淀,原因是;
b.随后沉淀溶解,此反应的离子方程式是。
纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗,其制备过程如图所示,下列叙述不合理的是( )

A . 在反应②中,  的作用可能是促进氯化铁水解
B . 直接加热FeCl3溶液也可以得到四氧化三铁
C . 反应③的化学反应方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
D . 纳米四氧化三铁在水中形成的分散系,有可能产生丁达尔现象
的作用可能是促进氯化铁水解
B . 直接加热FeCl3溶液也可以得到四氧化三铁
C . 反应③的化学反应方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
D . 纳米四氧化三铁在水中形成的分散系,有可能产生丁达尔现象
下列实验现象或操作正确且与结论相匹配的是( )
| 现象或操作 | 结论 | |
| A | 相同条件下,分别测量0.1 mol•L-1和0.01 mol•L-1醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| B | 将H2O2溶液滴加到酸性KMnO4溶液中,溶液褪色 | H2O2具有氧化性 |
| C | 常温下将大小相同的铝片分别加入到浓硝酸和稀硝酸中,浓硝酸比稀硝酸反应更剧烈 | 反应物浓度越大,反应速率越快 |
| D | 向碘水中加入CCl4振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
A . A
B . B
C . C
D . D
下列关于物质分类正确的是( )
A . 混合物:水煤气、冰醋酸、冰水混合物
B . 电解质:氯化氢、硫酸钡、水
C . 正盐:小苏打、纯碱、氯化钠
D . 碱性氧化物:氧化钙、四氧化三铁、过氧化钠
下表中物质的分类组合完全正确的是( )
| 编组 | A | B | C | D |
| 强电解质 | NaCl | Ba(NO3)2 | H2SO4 | H2S |
| 弱电解质 | HF | CH3COOH | BaSO4 | NH3·H2O |
| 非电解质 | Cu | NH3 | CO2 | 蔗糖 |
A . A
B . B
C . C
D . D
如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是( )
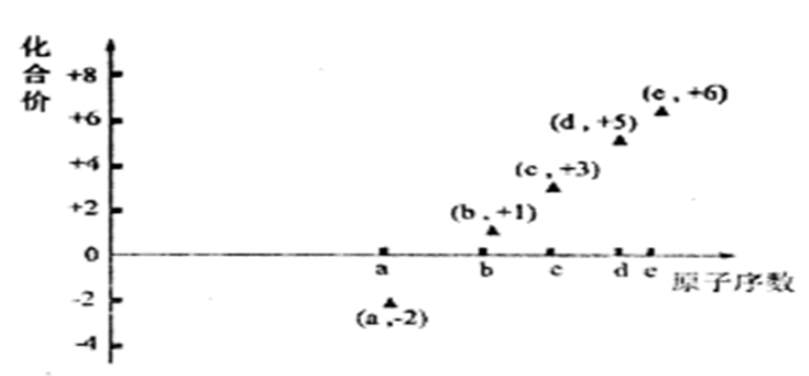
A . 16a和18a属于同种核素
B . 气态氢化物的稳定性:e>a
C . 第一电离能:d>e
D . 因为b2a溶于水导电,所以b2a是电解质
在煮沸的蒸馏水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,制得Fe(OH)3胶体。下列关于胶体的说法正确的是( )
A . Fe(OH)3胶体是电中性的
B . Fe(OH)3胶体和FeCl3溶液的本质区别是能否产生丁达尔效应
C . 可用滤纸分离提纯Fe(OH)3胶体
D . 胶体的分散剂一定是水
常温下,0.1 mol∙L−1下列溶液:①HCl、②H2SO4、③CH3COOH,导电能力强弱顺序是( )
A . ②>①>③
B . ①=②>③
C . ①>②>③
D . ①=②=③
最近更新



