第一单元 含硫化合物的性质 知识点题库
下列关于浓硫酸的说法正确的是( )
A . 在加热条件下能使不活泼金属铜溶解,表现出浓硫酸的强氧化性和酸性
B . 可以用铁制或铝制容器贮运,表现出浓硫酸有稳定的化学性质
C . 能使胆矾晶体由蓝色变为白色,表现出浓硫酸的脱水性
D . 能使蔗糖炭化,表现出浓硫酸的吸水性
下列物质都具有漂白性,其中一种与其它物质的漂白原理不相同,这种物质是( )
A . HClO
B . H2O2
C . O3
D . SO2
下列解释物质用途或现象的反应方程式不准确的是( )
A . 硫酸型酸雨的形成会涉及反应:2H2SO3+O2  2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2S2O3溶液中加入稀硫酸:S2O32-+2H+ ═SO2↑+S↓+H2O
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
Si+CO2↑
C . Na2S2O3溶液中加入稀硫酸:S2O32-+2H+ ═SO2↑+S↓+H2O
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
 2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2S2O3溶液中加入稀硫酸:S2O32-+2H+ ═SO2↑+S↓+H2O
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
Si+CO2↑
C . Na2S2O3溶液中加入稀硫酸:S2O32-+2H+ ═SO2↑+S↓+H2O
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
⑴活性炭⑵氯水⑶二氧化硫⑷臭氧 ⑸过氧化钠 ⑹双氧水.
A . (1)(2)(4)(6)
B . (1)(2)(3)(5)
C . (2)(4)(5)(6)
D . (3)(4)(5)(6)
下列解释物质用途或现象的反应方程式不准确的是( )
A . 硫酸型酸雨的形成会涉及反应:2H2SO3+O2  2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H
Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H  ═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
 2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C
2H2SO4
B . 工业上制取粗硅的化学方程式:SiO2+C  Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H
Si+CO2↑
C . Na2 S2O3溶液中加入稀硫酸:S2O+2H  ═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
═SO2+S↓+HO2
D . 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl﹣+ClO﹣+2H+═Cl2↑+H20
下列实验用来证明气体SO2的存在,其中正确的( )
①能使品红溶液褪色 ②能使湿润的蓝色石蕊试纸变红 ③能使澄清的石灰水变浑浊 ④通入到足量的NaOH溶液中,再滴入BaCl2溶液,有白色沉淀生成,该沉淀溶于盐酸 ⑤通入到溴水中使其褪色,再滴入Ba(NO3)2溶液,有白色沉淀生成
A . ①②④⑤
B . 都不能证明
C . ①⑤能证明
D . 只有⑤能证明
下列金属或氧化物可以完全溶解的是( )
A . 1molZn与含1molHCl的稀盐酸共热
B . 1molCu与含2molH2SO4的浓硫酸共热
C . 1molCu与含4molHNO3的浓硝酸
D . 1molMnO2与含4molHCl的浓盐酸共热
二氧化硫能够使品红溶液褪色,表现了二氧化硫的( )
A . 氧化性
B . 还原性
C . 漂白性
D . 酸性氧化物的性质
下列叙述正确的是( )
A . 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2 , 产生沉淀.
B . 向FeCl3溶液中滴加氨水,产生红褐色沉淀;再加入NaHSO4溶液,沉淀消失
C . 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
D . 分液时,分液漏斗中下层液体从下口流出,上层液体也从下口放出
用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是 ( )
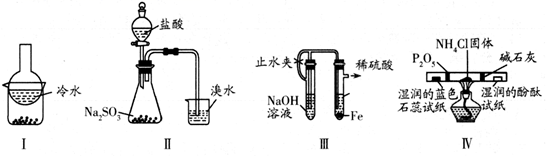
A . 加热装置I中的烧杯分离I2和高锰酸钾固体
B . 用装置II验证二氧化硫的漂白性
C . 用装置III制备氢氧化亚铁沉淀
D . 用装置IV检验氯化铵受热分解生成的两种气体
下列基本实验操作中,不合理的是( )
A . 分液操作时,分液漏斗下端管口尖端处紧靠烧杯内壁
B . 可用湿润的pH试纸检验氨气
C . 稀释浓硫酸时,可向盛有浓硫酸的烧杯中直接加蒸馏水
D . 试管可用酒精灯直接加热,也可用水浴加热
银耳本身为淡黄色,某地出产一种雪耳,颜色洁白如雪,其制作过程如下:将银耳堆放在密封状况良好的塑料棚内,在棚的一端支一口锅,锅内放硫黄,加热使硫黄熔化并燃烧,两天左右雪耳就制成了。雪耳炖不烂,且对人体有害,制作雪耳利用的是( )
A . 硫的还原性
B . 二氧化硫的漂白性
C . 二氧化硫的还原性
D . 硫的漂白性
欲进行下列实验,其方案设计合理的是( )
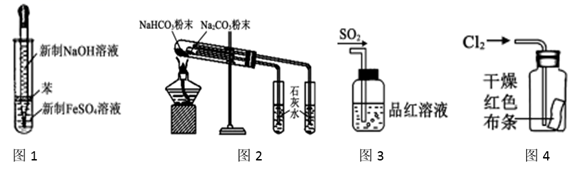
A . 图1为制备Fe(OH)2
B . 图2为比较Na2CO3和NaHCO3的稳定性
C . 图3为验证SO2的还原性
D . 图4为验证Cl2具有漂白性
“亲爱的水:每当我遇上你,我就有种沸腾的感觉。当我见不到你时,我甚至会在空气中寻找你的气息……”这是浓硫酸对水的真情告白。图中试管中盛有几毫升水,与大试管连通的U形细玻璃管内放有少量水(已染成红色)。如沿小试管壁小心地慢慢注入3mL浓硫酸,静置片刻后,U形细玻璃管中可观察到的液面现象是( )

A . 左高右低
B . 左低右高
C . 左右一样高
D . 来回振动
下列解释事实的方程式正确的是( )
A . CO2通入过量的NaOH溶液中:CO2+OH-=  B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 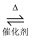 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
 B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 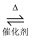 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
下列有关物质性质和用途说法错误的是( )
A . 液氨可用作制冷剂
B . MgO熔点很高,可用于制造耐火材料
C . SO2可用作食品防腐剂
D . ClO2可用于杀菌消毒,H2O2不可以
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 向浓盐酸中加入浓硫酸可制备氯化氢气体 | 浓盐酸易挥发,浓硫酸与水作用放出大量的热 | Ⅰ对,Ⅱ对; 有 |
B | Cu 能与浓 HNO3 反应 | 由于 Cu 具有还原性,浓HNO3 具有氧化性,在任何条件下生成的气体一定是 NO2 | Ⅰ对,Ⅱ错; 无 |
C | 硫单质在纯氧中燃烧有少量 SO3 生成 | 部分二氧化硫被氧化为SO3 | Ⅰ对,Ⅱ对; 无 |
D | 硝酸铵和碱石灰共热用于实验室制备 NH3 | 铵盐与碱能发生复分解反应 | Ⅰ对,Ⅱ对; 有 |
A . A
B . B
C . C
D . D
硫元素的几种化合物存在如图转化关系,下列判断错误的是( )

A . 反应①中浓硫酸被氧化生成 , 生成的
, 生成的 具有漂白性
B . 反应②中,当
具有漂白性
B . 反应②中,当 过量时,溶液中有
过量时,溶液中有 生成
C . 可以用
生成
C . 可以用 清洗实验③后附着在试管壁上的硫
D . 反应④的离子方程式为
清洗实验③后附着在试管壁上的硫
D . 反应④的离子方程式为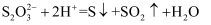
 , 生成的
, 生成的 具有漂白性
B . 反应②中,当
具有漂白性
B . 反应②中,当 过量时,溶液中有
过量时,溶液中有 生成
C . 可以用
生成
C . 可以用 清洗实验③后附着在试管壁上的硫
D . 反应④的离子方程式为
清洗实验③后附着在试管壁上的硫
D . 反应④的离子方程式为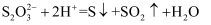
下图是有关二氧化硫性质的实验装置图,下列说法正确的是( )

A . a中紫色石蕊先变红后褪色
B . b中品红溶液褪色,加热后又恢复红色
C . c中氢硫酸溶液出现黄色浑浊,体现 的还原性
D . d中溴水褪色,体现了二氧化硫漂白性
的还原性
D . d中溴水褪色,体现了二氧化硫漂白性
 的还原性
D . d中溴水褪色,体现了二氧化硫漂白性
的还原性
D . d中溴水褪色,体现了二氧化硫漂白性
喷泉实验装置如图所示。应用下列各组气体一溶液,能出现喷泉现象的是( )

气体 | 溶液 | |
A |
| 稀 |
B |
| 饱和NaOH溶液 |
C | NO |
|
D |
| 稀盐酸 |
A . A
B . B
C . C
D . D
最近更新

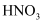
 稀溶液
稀溶液