氧气的检验和验满 知识点题库
如图所示为实验室中常见的气体制备和收集装置.

请回答下列问题:
-
(1) 实验室用高锰酸钾制取氧气,应选用发生装置(填字母序号),反应的化学反应符号表达式为.若用装置D收集氧气,验满的方法是.若用装置F来收集氧气,结束时先
, 再.其主要的目的是 .
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是.
-
(3) 欲使用装置E用排空气法收集二氧化碳,则气体应从(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从
(填“a”或“b”)端通入.
-
(4) 已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母序号).
实验目的 | 实验方案 | |
A | 鉴别AgNO3溶液与NaNO3溶液 | 分别滴加稀盐酸,振荡,观察是否产生沉淀 |
B | 除去CO中混有的CO2 | 将混合气体通过灼热的氧化铜 |
C | 鉴别纯铝和硬铝 | 将两者相互刻画,比较硬度 |
D | 检验集气瓶中是否集满氧气 | 将带火星的木条伸入集气瓶口,观察木条能否复燃 |

B . 振荡试管
B . 振荡试管 
C . 氧气验满
C . 氧气验满
D . 过滤
D . 过滤
 干燥氢气
B .
干燥氢气
B .  检验氧气是否集满
C .
检验氧气是否集满
C .  检验X溶液中是否含有
检验X溶液中是否含有 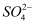 D .
D .  验证Zn、Fe、Cu的活动性强弱
验证Zn、Fe、Cu的活动性强弱
自来水消毒过程中通常会发生如下甲乙两个化学反应,其反应的微观过程可用下图表示:( ![]() 表示氯原子,
表示氯原子, ![]() 表示氧原子,
表示氧原子, ![]() 表示氢原子)
表示氢原子)

-
(1) 请写出甲图所示反应的化学方程式。
-
(2) 收集一瓶E物质,检验E物质的方法和看到的现象是。
-
(3) 从上述反应可知,反应前后原子的没有改变。
集气瓶编号 | 瓶内预装水 体积/毫升 | 充入氧气 体积/毫升 | 瓶内空气 体积/毫升 | 瓶内空气里氧气 体积的百分比 | 木条能否复燃 |
1 | 120 | 120 | 197 | 50.9% | 能 |
2 | 97 | 97 | 220 | % | 能 |
3 | 90 | 90 | 227 | 43.4% | 能 |
4 | 84 | 84 | 233 | 41.9% | 能 |
5 | 81 | 81 | 236 | 41.2% | 不能 |
-
(1) 请指出得到5瓶含氧量不同的空气的具体方法 ;
-
(2) 试将上表空白处补充完整 (保留1位小数);
-
(3) 由该实验可得到的结论是 。


-
(1) 该兴趣小组同学利用如图所示装置制取氧气,称取一定质量的KMnO4固体放入试管中,试管内的药品放入试管底部,开始加热时,要让试管均匀受热,具体操作是。
-
(2) 有同学认为用过氧化氢溶液和二氧化锰制取氧气更好,其理由是。
-
(3) 为了使实验数据更加具体和准确,小组同学经讨论,他们准备用不同体积分数的氧气来进行实验。利用如图所示装置收集氧气得到1号瓶,并利用这种方法依次得到2-4号瓶。分别将带火星的木条伸入集气瓶中,得到的现象如下:
1号瓶(收集34%的氧气)
2号瓶(收集35%的氧气)
3号瓶(收集36%的氧气)
4号瓶(收集37%的氧气)
不复燃
不复燃,但很亮
很亮,复燃
立即复燃
某同学根据实验现象得出结论:“氧气约占36%时就是带火星木条复燃的最低体积分数”,而其他同学立即反对,原因是。
-
(4) 反思交流:结合上述探究,排空气法收集氧气时,检验氧气是否集满采用使带火星的木条复燃的方法,你认为是否科学?。
 B . 过滤
B . 过滤 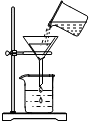 C . 给液体加热
C . 给液体加热  D . 铁丝在氧气中燃烧
D . 铁丝在氧气中燃烧 

步骤一:向大烧杯中注入足量的冷水,打开K1、关闭K2 , 向下压左侧注射器活塞,使生成的氧气持续通入U形管,并观察U形管中现象;
步骤二:关闭K1、打开K2 , 向下压右侧注射器活塞,使生成的二氧化碳将U形管内的氧气排尽,然后将烧杯中的冷水换成等量的80℃的热水,并观察U形管中现象;
步骤三……,并观察U形管中现象。
-
(1) 根据图示信息,写出生成氧气的化学方程式 。
-
(2) 简述步骤二中判断U形管内氧气已经排尽的方法。 。
-
(3) 补充完整步骤三的操作,并写出U形管中应观察到的现象。 。

-
(1) 仪器①的名称是 ,用B装置制取氧气的化学方程式为。
-
(2) 若用F装置收集氧气,检验氧气是否收集满,带火星的应放在(填“a”或“b”)端口。
-
(3) 氨气极易溶于水,且密度比空气小。实验室可用氯化铵固体和氢氧化钙固体混合加热制取氨气,反应原理为:2NH4Cl+Ca(OH)2
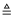 2NH3↑CaCl2+2H2O;用该原理制取氨气,气体发生装置和收集氨气的装置应分别选择(填标号)。
2NH3↑CaCl2+2H2O;用该原理制取氨气,气体发生装置和收集氨气的装置应分别选择(填标号)。
 B . 除去一氧化碳中混有的二氧化碳
B . 除去一氧化碳中混有的二氧化碳  C . 验证氧气是否收集满
C . 验证氧气是否收集满  D . 测定空气中氧气的含量
D . 测定空气中氧气的含量 

-
(1) 检验b管中气体的方法是。
-
(2) 往水中加入少量的硫酸可以增强溶液导电性(硫酸不参与反应),若用溶质的质量分数为6%的硫酸溶液100克进行实验,有20克水被电解,则此时硫酸溶液的溶质的质量分数为。

①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上。
②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象。
-
(1) 可观察到带火星的棒香立即。
-
(2) 写出上述实验中H2O2分解的化学方程式:
-
(3) 假定上述实验中的完全反应,可产生氧气的质量为g(精确到0.01)
-
(4) 下列各项是同学们对该创新实验的评价,其中不合理的是 (填字母,多选)A . 实验中所用的仪器、材料及药品均易得到 B . 实验中使用的药品用量太大 C . 反应速度太慢,耽误时间 D . 实验现象明显,整个装置好似点燃的灯塔,趣味性强

-
(1) 该反应的化学方程式为,其基本反应类型是.
-
(2) 用排空气法收集氧气,判断已经收集满的方法是.
|
同学序号 |
质量分数相同的过氧化氢溶液 |
溶液中加入的物质 |
收集到的气体体积 |
|
甲 |
100mL |
未加其他物质 |
amL |
|
乙 |
100mL |
氧化铁0.5g |
bmL |
|
丙 |
100mL |
二氧化锰0.5g |
cmL |
-
(1) 甲同学认为乙同学收集到的气体有可能是氮气,乙同学马上从理论上推翻了甲同学的观点,为什么?
-
(2) 乙同学应该如何检验实验所生成的气体。
-
(3) 欲探究氧化铁在实验中是否起催化作用,首先应比较(填“a与b”、“b与c”或“a与c”)的大小,其次需补充做如下实验(无需写出具体操作):①;②反应前后氧化铁的化学性质有没有改变。

【提出问题】这些气泡究竟是怎样产生的?是什么气体?
【猜 想】小科:是氧气;小华:是氯化氢;小琪:是氨气(NH3);小金:是氢气。小马马上否定了小琪的猜想,他否定的依据是;
【实验探究】他们开始着手收集所产生的气体.
实验一:小科用带火星的木条检验该气体,木条不复燃。说明生成的气体不是氧气;
实验二:为继续探究反应后生成的气体是否是氯化氢气体,请你提出一种实验方案;
实验三:为确定气体是否是氢气,小金设计如图实验装置(每个装置均充分反应),甲、丙装置中无水硫酸铜的作用是不同的,请指出它们的区别。

步骤 1:利用图甲所示装置, 将干燥的 O2 从导管 a 通入 U 形管(装置气密性良好, 药品 如图所示);待 U 形管内充满 O2 后,在导管 b 处连接一活塞推至底部的注射器,收集 20 mLO2 后在导管 a 处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤 2:一段时间后,观察 U 形管内的铁丝,其现象如表所示。
| 观察对象 | 现象 |
| ①干燥的普通铁丝 | 没有明显变化 |
| ②潮湿的普通铁丝 | 较多红褐色锈斑 |
| ③潮湿的纯铁丝 | 没有明显变化 |
-
(1) 步骤 1 中, 检查 U 形管内是否已充满 O2的方法是。
-
(2) 铁制品的锈蚀条件之一是需要 O2 , 在此实验中能支持此条件的证据是。
-
(3) 通过对比实验现象, 此实验还可得出铁制品锈蚀的条件是。



