酸的化学性质 知识点题库
-
(1) 浓硫酸在实验室常用作干燥剂,因为浓硫酸有性。
-
(2) 写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,不属于酸的共同性质的是(填编号)

-
(1) 两个装置所盛放的液体分别是和水.
-
(2) 几十天以后,两个装置中的镁带表面都未变黑,于是小柯猜想,黑色物质可能是碳和碳酸镁的混合物,如果小柯的猜想成立,那么取黑色物质加入足量的稀盐酸,会观察到哪些现象?.

X | Y | Z | |
A | CO2 | Na2CO3 | CaCO3 |
B | CuO | Cu(NO3)2 | Cu(OH)2 |
C | HCl | BaCl2 | NaCl |
D | Mg | MgO | MgCl2 |
如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

-
(1) 制备氯气选用的药品为:高锰酸钾和浓盐酸,相关的化学反应方程式为:.
-
(2) 装置B是安全瓶,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象.
-
(3) 装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入(选a或b或c)
a
b
c
I
干燥的有色布条
湿润的有色布条
湿润的有色布条
II
碱石灰
浓硫酸
无水氯化钙
III
湿润的有色布条
干燥的有色布条
干燥的有色布条
| 实验操作 | 现象 | 结论 |
| A.向盛有少量无色溶液的试管中滴加酚 酞试液 | 溶液不变色 | 该溶液一定呈酸性 |
| B.向盛有少量无色溶液的试管中滴加氯化 钡溶液 | 出现白色沉 淀 | 该溶液中一定含有硫酸根 离子 |
| C.向盛有少量固体的试管中滴加稀盐酸 | 产生气泡 | 该固体中一定含有碳酸盐 |
| D.点燃某气体,在火焰上方罩一个干冷 的烧杯 | 烧杯内壁出 现水珠 | 该气体中一定含有氢元素 |
⑴用四支试管分别取出每种溶液,分别滴入几滴酚酞,B和D中都显红色,其余仍为无色。
⑵另取两支试管,分别取出B和D溶液,分别向其中通入少量二氧化碳,B中产生浑浊,D中仍澄清。
⑶另取两支试管,分别取A和C溶液,分别滴入BaCl2溶液,只有C中出现白色沉淀。
根据以上实验事实,试推断A、B、C、D四种溶液中溶质的化学式,其中:
B是,C是,D是


-
(1) 已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是;
-
(2) B位置“队员”所代表的物质的一种用途是;
-
(3) 写出连线④代表的物质间发生反应的化学方程式。
| 选项 | 性质 | 用途 |
| A | 白色硫酸铜粉末遇水会变蓝色 | 检验水的存在 |
| B | 浓硫酸具有脱水性 | 干燥氧气 |
| C | 稀盐酸能与某些金属反应 | 除铁锈 |
| D | 氢氢化钠固体能潮解 | 干燥二氧化碳 |
|
同学 |
甲 |
乙 |
丙 |
|
操作 |
各取一支相同规格的试管,在试管中加入一定量的待测溶液 |
||
|
滴入无色酚酞试液 |
加入足量的 ? |
加入足量的BaCl2溶液 |
|
|
现象 |
变红 |
产生气泡 |
产生白色沉淀 |
|
结论 |
没变质 |
变质 |
变质 |
-
(1) 乙同学加入的“?”是。
-
(2) 乙同学认为甲同学的实验和结论不正确,理由是。
-
(3) 丙同学将沉淀过滤、洗涤、干燥,称量质量为1.97g。已知丙同学所取的待测溶液质量为10g,请根据化学方程式计算,该待测溶液中变质生成物的质量分数。
【实验方案】
|
实验步骤 |
实验现象 |
实验结论 |
|
|
小东 |
用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH |
pH试纸变色 pH>7 |
该溶液是氢氧化钠溶液 |
|
小南 |
取适量溶液于试管中,加入经打磨过的铝条 |
有气泡产生 |
该溶液是稀硫酸 |
【提出问题】为什么我们取相同溶液而实验结论却不同呢?
【解决问题】小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是蓝色沉淀产生 , 于是一致认为该溶液是氢氧化钠溶液,为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量。实验设计如下:

【回答问题】
-
(1) 写出操作Ⅰ中玻璃棒的作用:;
-
(2) a溶液是,选择该溶液的理由是;
-
(3) 溶液A中所含溶质是。
-
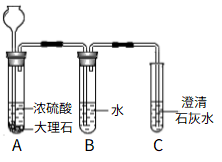
(1) 实验后向B中滴入紫色石蕊试液,可看到的现象。
-
(2) 选一种试剂代替水,在本实验中起到相同作用,你选的试剂是。
-
(3) 如果去掉B装置,将A、C直接连接,则C装置中可能发生反应的化学方程式是(写一条)。




