气体的净化 知识点题库
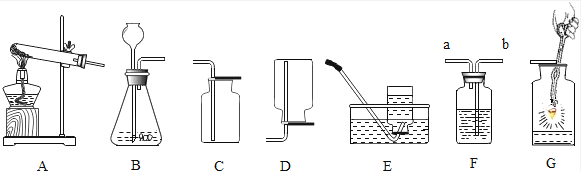
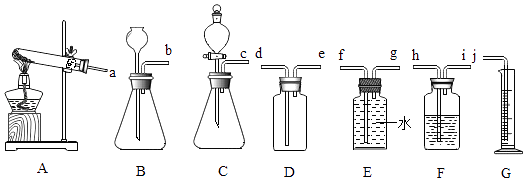
如图是实验室常见的装置,根据图示回答下列问题:
-
(1) 指出图两处明显的错误: , .
-
(2) 将图中的错误改正后,小军要制取二氧化碳应选用的装置是 (填字母).若要得到干燥的二氧化碳,他选用了F装置,装置中所盛的干燥剂是 ,气体应从 端通入.
-
(3) 小丽用A装置制取氧气,写出她制取氧气的一个化学方程式 ,该反应类型是 .用制得的氧气完成G装置所示实验时,集气瓶中留有少量水的原因是 ,铁丝绕成螺旋状的目的是 .
选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
A | 氧化钙 | 石灰石 | 高温 |
B | 稀盐酸 | 稀硝酸 | 加入过量的硝酸银溶液,过滤 |
C | 氯化钠 | 泥沙 | 加入足量的水溶解、蒸发、结晶 |
D | 氨气 | 水蒸气 | 通过足量的氢氧化钠固体干燥 |
某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。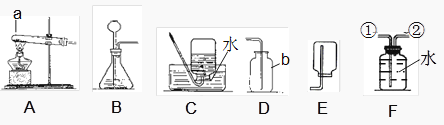
(1)写出图中仪器b的名称 b。
(2)实验室制取氢气的化学方程式是。应选择的气体发生装置是。
(3)实验室采用加热氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式是 , 若用盛满水的F装置收集氧气,应从导管(填①或②)通入。
(4)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是。
某研究性学习小组利用下列装置进行气体的制取实验,请分析回答下列问题. 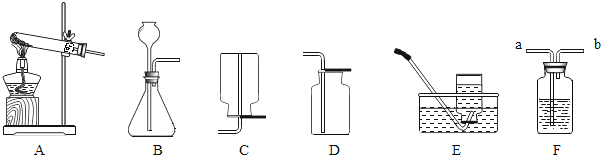
-
(1) 选用A装置制取氧气的化学方程式.
-
(2) A、E连接,制取的氧气不纯的原因是(写一点即可).
-
(3) 若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置F,则装置F中应放入的物质是,气体应从端通入(填“a”或“b”)
-
(4) 实验室制取二氧化碳选择的发生装置和收集装置是(填选项字母),选择该发生装置的依据是,检验二氧化碳是否收集满的方法是.
-
(5) 若用F装置检验制得的气体是否为二氧化碳,则F装置内发生反应的化学方程式为.
选项 | 物质 | 杂质 | 除杂方法 |
A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
C | H2 | CO | 通入O2 , 点燃 |
D | O2 | H2O |
-
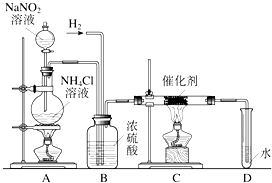
(1) C装置的硬质试管中发生反应的化学方程式为.
-
(2) 反应时N2和H2的最佳质量比是.如果按此比例进行反应,反应时,D中导管口是否会逸出气泡?(已知NH3极易溶于水),说明逸出气泡的原因:.
-
(3) B中浓硫酸的作用是.
-
(4) 用实验方法证明确实有NH3生成:.
-
(1) 写出指定仪器的名称:①;
-
(2) 某同学为测定一定量高锰酸钾产生氧气的体积,则他该选择的装置是,发生反应的化学方程式是.
-
(3) 某同学用BFD制取并收集干燥的二氧化碳,F中盛放的物质是,该装置中导管口的连接顺序是b→→→→.

-
(1) 写出有标号的仪器名称:②
-
(2) 实验室用高锰酸钾制氧气选用的发生装置是(填序号),反应的化学方程式为
-
(3) 实验室可用B或C装置制CO2 , 反应的化学方程式为,C相对于B装置的优点有
-
(4) 实验室可用F装置组合测量生成二氧化碳的体积,导管b的作用是;植物油的作用是。
-
(5) 若B装置中固体为锌粒,②中加入浓盐酸制H2 . 欲获得纯净干燥的氢气需经过两次D装置,第一个D装置中应盛放的试剂是溶液,第二个D装置中应盛放的试剂是(填名称),再用E装置收集H2 , 气体应从端通入(选填“a”或“b”)
-
(1) 常见化石燃料:煤、天然气、
-
(2) 常见集气方法:向上排空气、向下排空气、
-
(3) 常见 :生石灰、浓硫酸、烧碱

-
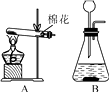
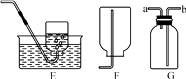
(1) 以上装置A~F中有一处明显的错误,请加以改正;利用改正后的装置完成后面的实验;
-
(2) 若选用装置B、D、G制取并收集干燥的二氧化碳气体,正确的组装顺序为,则在装置G中加入的液体试剂是(填名称);
-
(3) 实验室用高锰酸钾制取氧气,应选用的发生装置是,反应的化学方程式为;若用装置G收集氧气,气体从(选填“a”或“b”)端通入;
-
(4) 装置B、C都能用来制取氢气,相对于装置B,装置C的突出优点是。
-
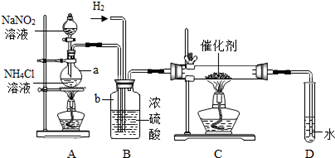
(1) 写出a、b两种仪器的名称:a:b:
-
(2) 为了获得较纯净的氢气,该实验中制取氢气的化学方程式最好是。
-
(3) 写出C装置的硬质试管中发生反应的化学方程式
-
(4) 反应时N2和H2的最佳质量比是.如果按此比例进行反应,反应时D中导管口是否会出气泡?(已知NH3极易溶于水),说明逸出气泡的原因
-
(5) B装置的作用除了将两种气体混合外,还有、
-
(6) 结合本实验装置,证明确实有NH3生成的简单方法及实验现象是
-
(7) 归纳与演绎是重要科学方法,也是常用的学习方法,我们已经学过实验室制取气体的反应原理、制取与收集方法请你归纳出实验室制取气体反应的共同点;(填序号).
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
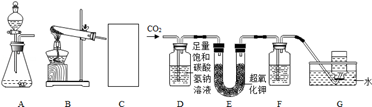
-
(1) C处应从A、B两种装置中选择作CO2发生装置。
-
(2) 已知CO2不溶于饱和碳酸氢钠溶液,D装置有足量碳酸氢钠溶液,其作用是;
-
(3) 据资料知,水与水蒸气也能与超氧化钾反应生成氧气。于是有同学提出,上述实验能生成氧气可能与CO2中混有的水蒸气有关,若要确认是CO2与超氧化钾反应生成氧气,你对上述实验装置的改进方法是。
-
(4) 为了除去O2中可能剩余的CO2 , F中可盛放过量溶液。
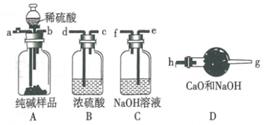
①用足量稀硫酸与已准确称量的纯碱样品作用,使纯碱样品中Na2CO3完全反应放出CO2气体;②当纯碱样品完全反应后,向产生CO2的装置内缓缓鼓入不含CO2的空气,把①产生的CO2 , 全部排入吸收CO2的装置中;③测出被吸收CO2的质量,求出样品中Na2CO3的质量分数。
-
(1) 各仪器连接顺序是(填写各接口的字母):空气→,接,接,接,接,。
-
(2) 装置B的作用是,若没有装置B,会导致测定Na2CO3的质量分数 (填“偏大”“偏小”或“不变”,下同)。
-
(3) 装置C的作用是 ,若没有装置C,会导致测定Na2CO3的质量分数 。
-
(4) 实验操作②中,鼓入空气“缓缓”地进行,其理由是 ,如果这步操作太快,会导致测定的碳酸钠的质量分数。
-
(5) 若样品质量为ng,测得产生CO2的质量为mg,则样品中Na2CO3的质量分数是。
草酸晶体(H2C2O4•2H2O)在浓H2SO4作用下加热分解产生H2O、CO和CO2 . 同学们设计了如图所示的实验装置,请回答下列问题:

-
(1) 图中A是制取一氧化碳的气体发生装置。
①装置A中,方便添加浓硫酸的仪器名称是;装置B中,提供热源的仪器名称是。
②装置B中发生反应的化学方程式为。
-
(2) 将E、F、G3个装置按一定顺序接入到方框中。
①正确的导管接口顺序是:a→→h。
②方框中的G装置是否可以省略?并说明理由。
-
(3) 一氧化碳还原氧化铁。
①实验前,要先通入CO,目的是除去装置(填写装置下方字母序号)中的空气。
②观察到时,熄灭B处的酒精喷灯,等到时,再熄灭D处的酒精灯。
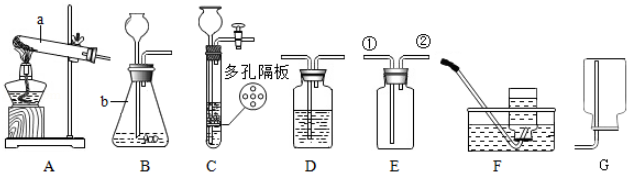
-
(1) 写出图中仪器b的名称:。
-
(2) 实验室用氯酸钾制取氧气应选择的发生装置是(填字母),用E装置收集氧气,则气体应从 (填“①”或“②”) 端进入。写出该反应的化学方程式。
-
(3) 实验室可用装置C代替装置B制取二氧化碳,其优点是;写出实验室制取二氧化碳的化学方程式:;如果用E装置收集二氧化碳,验满方法是:。
-
(4) 实验室用C装置制取氢气,则锌粒放在;若要干燥氢气,可将气体通入装有(填试剂名称)的D装置中。
-
(5) 已知用氯化铵(固体)与熟石灰(固体)混合加热可制取氨气,且氨气易溶于水,密度比空气小,则实验室制取并收集氨气,应选择的发生装置和收集装置为(填序号)。
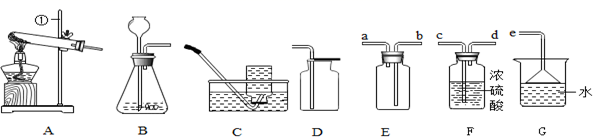
-
(1) 写出仪器①的名称。
-
(2) 用氯酸钾和二氧化锰制取氧气的化学方程式为,该反应属于。(填基本反应类型)用装置C收得的氧气不纯,可能的原因是。若用装置A装高锰酸钾制取氧气,则装置需要补充。若要收集到较纯净的氧气,其收集装置应选(填字母)。
-
(3) 用向上排空气法收集到的气体,检验是否为氧气的操作是。
-
(4) 通常状态下,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水形成盐酸。用如图所示装置收集一瓶干燥的HCl,装置的导管按气流方向连接的顺序是:气体→→→→→e(填字母)。
-
(5) G装置烧杯中的水改成氢氧化钠溶液可吸收污染物五氧化二磷,生成磷酸钠(Na3PO4)和水,反应的化学方程式为。
-
(6) 为了探究气体氨气(NH3) 的某些性质,小雨同学查阅了有关资料,知道具有碱性的物质可以使无色酚酞溶液变红;然后依次做了以下实验。
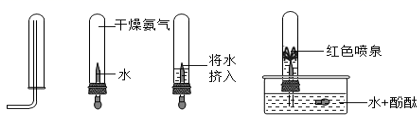
由以上实验,得出氨气的物理性质有、。



