质量守恒定律 知识点题库

 溶液
D . 图D是将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中
溶液
D . 图D是将形状相同质量相等的铁和锌分别加入到足量的质量和浓度都相等的稀硫酸中
 根据以上信息请回答下列问题:
根据以上信息请回答下列问题:
-
(1) 发生反应的化学方程式为;
-
(2) 根据已知条件列出求解50g该黄铜样品中锌的质量(x)的比例式为;
-
(3) 该黄铜样品中锌的含量;
-
(4) 用98%的浓硫酸配制上述实验所需的稀硫酸,需要水的质量是;
-
(5) 向反应后的滤液中加入209.4g水,所得溶液中溶质的质量分数是。
-
(6) 浓硫酸配成稀硫酸所用的仪器除了烧杯、玻璃棒外,还需的仪器是。
-
(1) 乙醇(C2H5OH)在空气中燃烧生成二氧化碳和水
-
(2) 能在氧气中燃烧,发出耀眼的白光,生成白色固体
-
(3) 有黑色固体生成的化合反应

-
(1) 化合反应,有水参加并放出大量热。
-
(2) 化合反应,有水参加且生成酸。
-
(3) 分解反应,生成物中有水。
-
(1) 水与人类的生活息息相关。
①保持水的化学性质的最小微粒是 (用化学符号表示)。
②生活中,通过过滤 (选填“能”或“不能”)使硬水软化。
-
(2) 为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请根据图示回答问题: (提示:硫酸铜与氢氧化钠反应生成氢氧化铜沉淀与硫酸钠)

①乙同学设计的实验如图B所示,实验中观察到反应前托盘天平的指针指向中间,反应后冷却,发现天平的指针发生偏转,天平不再平衡,其原因是 。
②甲同学设计A实验,通过实验得出结论:化学反应前后物质的总质量 。
③两位同学通过交流与反思得到启示:在探究化学反应前后物质的总质量是否发生改变 时,对于有气体参加或生成的反应一定要在 装置中进行。
④下列事实能用质量守恒定律解释的是 (填字母)。
A镁条燃烧后质量变大了
B蜡烛燃烧后质量变小了
C湿衣服晾干后变轻了
D碳酸钠与盐酸混合后质量变小了
E水结冰后,质量不变
-
(3) 实验室用34 g过氧化氢溶液和1 g二氧化锰制取氧气,实验的相关数据如图所示。请计算:
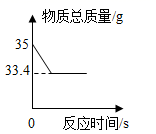
①反应生成氧气的质量为 g;
②过氧化氢溶液中含过氧化氢的质量是多少 。
 B .
B .  C .
C .  D .
D . 

-
(1) 图中仪器 A 的名称为;
-
(2) 实验室制取二氧化碳需要选择下列药品中的 ;(填字母)
A大理石 B 纯碱 C 稀盐酸 D 稀硫酸
-
(3) 组装用排空气法制取和收集二氧化碳,除选择仪器A和B外,还要从图中选择的仪器有;(填字母)
-
(4) 上述装置还可用于制某气体,制取该气体的化学方程式。

-
(1) 反应中二氧化锰的作用是。
-
(2) 计算过氧化氢溶液中溶质的质量分数。(写出计算过程)


-
(1) 化学反应前后和(选填分子、原子、元素)种类不发生改变
-
(2) 参加反应的两种分子的个数比是
-
(3) 反应前两种元素的化合价为
化学上有一种气体,只要你闻到它就会情不自禁地笑起来,因此人们称它为“笑气”。笑气的化学式是N2O,无色有甜味气体,是一种可以“得氧”的物质,但在室温,下稳定。它最早由英国化学家戴维通过加热硝酸铵分解制得,他在制得N2O的同时也得到了一种常见的无色液体。
由于吸入它会感到愉快,并伴有轻微麻醉作用,所以早期被用于牙科手术的麻醉,现在你可以在手术室、面包店、咖啡馆听到这个名字。
近年网络中流行的“奶油气弹”“笑气子弹”其实就是放置“笑气”的耐压钢瓶。一位20岁的大学生,独自在京求学,在酒吧参加生日聚会时,看到同行有人在吸食笑气而加入,随着吸食剂量越来越大,出现了头疼、四肢无力等症状。鉴于“笑气”可能存在的风险,警方表示这可能是一种新型毒品。
阅读文本,完成下列任务:
-
(1) N2O中氮元素的化合价为。
-
(2) 将N2O从耐压钢瓶释放到气球中的微观变化是。
-
(3) 戴维制得N2O的化学方程式为。
-
(4) 根据以上的短文,下列有关N2O的说法中正确的是。
A N2O可能是一种新型毒品,应禁止其使用
B N2O可发生氧化反应
C N2O中氮元素和氧元素的质量比为7:4
-
(1) 丁酸乙酯的相对分子质量为。
-
(2) 丁酸乙酯中,碳、氢、氧三种元素的质量比为。(填最简整数比)
-
(3) 58g丁酸乙酯中氧元素的质量是。
 水的电解
B .
水的电解
B .  木炭在密闭的容器内燃烧
C .
木炭在密闭的容器内燃烧
C .  加热一定量的高锰酸钾制氧气
D .
加热一定量的高锰酸钾制氧气
D .  等质量的氯酸钾在有无二氧化锰条件下加热
等质量的氯酸钾在有无二氧化锰条件下加热
-
(1) 化肥硫酸铵属于____(填序号)A . 氮肥 B . 磷肥 C . 钾肥 D . 复合肥
-
(2) 计算样品中硫酸铵的质量分数(写出计算过程)。

-
(1) 两个镁离子。
-
(2) 铝与稀硫酸恰好完全反应后溶液中溶质的化学式。
-
(3) 75%医用酒精溶质的化学式。
-
(4) 天然气完全燃烧的化学方程式。



