质量守恒定律 知识点题库
近期媒体曝光了某品牌洗发水中含有致癌的成分--二恶烷(C4H8O2),下列有关二恶烷的说法正确的是( )
A . 二恶烷是氧化物
B . 二恶烷是由4个碳原子、8个氢原子和2个氧原子构成的
C . 二恶烷中碳、氢、氧元素的质量比为6 :1 :4
D . 一个二恶烷分子中含有一个氧分子
在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 5 | 20 | 0 |
| 反应后质量/g | 6.4 | 5 | 待测 | 6.4 |
A . W可能是单质
B . Y一定是催化剂
C . 该化学反应中X和W的质量变化之比是1:1
D . 反应后Z物质的质量为17.2g
正确的化学方程式是( )
A . Mg+O2  MgO
B . 4Fe+3O2
MgO
B . 4Fe+3O2  2Fe2O3
C . P+O2
2Fe2O3
C . P+O2  PO2
D . S+O2
PO2
D . S+O2  SO2
SO2
 MgO
B . 4Fe+3O2
MgO
B . 4Fe+3O2  2Fe2O3
C . P+O2
2Fe2O3
C . P+O2  PO2
D . S+O2
PO2
D . S+O2  SO2
SO2
甲、乙、丙、丁4种物质在密闭容器中充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质的质量/g | 30 | 3 | 6 | 8 |
| 反应后物质的质量/g | 16 | m | 4 | 24 |
A . 参加反应的甲、丙的质量比一定是7:1
B . 乙一定是反应的催化剂
C . 甲和丙两物质中的元素种类与丁元素种类不同
D . 甲、丁一定都是单质
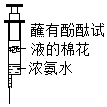
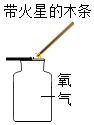
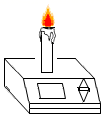
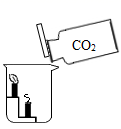
下列实验设计不能达到实验目的是( )
| 选项 | A | B | C | D |
| 实验设计 | | | | |
| 实验目的 | 证明分子不断运动 | 验证氧气已收集满 | 验证质量守恒定律 | 比较CO2与空气的密度 |
A . A
B . B
C . C
D . D
欲测定Cu-Zn
合金及 Cu-Ag 合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器。
-
(1) 你认为能测出铜的质量分数的是合金。
-
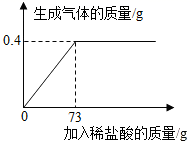
(2) 取该合金的粉末 50g 加入该稀盐酸充分反应,所加稀盐酸与生成气体的质量关系如图所示。请计算该合金中铜的质量分数,生成气体的质量。
2015年10月5日,中国女科学家屠呦呦因创制新型抗疟药一青蒿素(C15H22O5),根据青蒿素的化学式回答:
-
(1) 青蒿素中碳原子与氧原子的原子个数比。
-
(2) 青蒿素中碳元素的质量分数是。(精确到0.1%)
2020年2月4日,中国工程院院士李兰娟的研究团队发现:达芦那韦(化学式:  )能显著抑制新冠肺炎病毒复制。下列关于达芦那韦的说法正确的是( )
)能显著抑制新冠肺炎病毒复制。下列关于达芦那韦的说法正确的是( )
 )能显著抑制新冠肺炎病毒复制。下列关于达芦那韦的说法正确的是( )
)能显著抑制新冠肺炎病毒复制。下列关于达芦那韦的说法正确的是( )
A . 属于无机化合物
B . 达芦那韦由75个原子构成
C . 由  五种元素组成
D . 氢元素的质量分数最大
五种元素组成
D . 氢元素的质量分数最大
 五种元素组成
D . 氢元素的质量分数最大
五种元素组成
D . 氢元素的质量分数最大
小明同学在学习了氧气的性质时,发现铁丝在空气中不能燃烧,但在氧气中能燃烧。了解到物质在空气中燃烧实际上是与其中的氧气发生了反应,氧气的浓度越大燃烧越旺盛,他心中产生了一个疑问:铁丝燃烧所需氧气最低浓度是多少?他想进行探究,需要收集不同浓度的氧气,若要得到氧气浓度约为80%的气体,假设他选用250mL的集气瓶,留集气瓶容积1/5水用于性质实验,请回答下列问题:
-
(1) 铁丝在氧气中的燃烧现象:。
-
(2) 铁丝燃烧的文字表达式:。
-
(3) 他该在250mL的集气瓶中约装多少体积的水来收集氧气?(通过列式计算,结果保留整数)
如图是某汽车尾气处理过程中发生的一个反应,下列有关说法正确的是( )
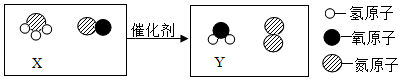
A . 上述反应中共有3种氧化物
B . 该反应中X和Y的质量比是17:27
C . 该反应中两种反应物的化学计量数之比是1:1
D . 该反应前后,化合价发生了变化的元素是N和H
化学来源于生活,学好化学能解决生活中的很多问题。
-
(1) 水的硬度过高会给生活和生产带来很多麻烦,家庭生活中通常用方法将硬水转化为软水。
-
(2) 石墨具有良好的导电性,常用来做。
-
(3) 氢动力汽车有一种是以氢气作为燃料的汽车,是名副其实的“绿色燃料”汽车。该汽车能实现排放出的尾气对空气无任何污染,其原因是(用化学方程式表示);工业上可以用甲醇(CH3OH)与水蒸气在加热及有催化剂的条件下制取氢气:
 ,生成物中碳元素的化合价为。
,生成物中碳元素的化合价为。
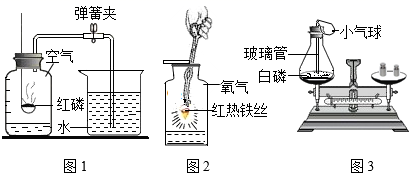
化学是以实验为基础的学科。下列是初中化学中的一些重要实验,请回答下列问题。
-
(1) 图1:红磷在空气中燃烧的化学方程式为;测定空气中氧气体积分数时,打开止水夹后观察到的现象是,该实验得出的结论是氧气约占1/5,若测量结果偏小的原因可能是(答1条)。
-
(2) 图2:集气瓶内放少量水的目的是。该实验的具体操作是把光亮的细铁丝盘成螺旋状,点燃铁丝末端绑的木条,最后缓慢插入集气瓶中,该反应的化学方程式为。
-
(3) 图3:某化学小组同学验证质量守恒定律的实验。装置中小气球的作用是,反应结束后,能得出质量守恒定律实验结论的现象是(填序号)。
a.白磷燃烧产生大量白烟 b.气球先变大后变小 c.反应前后天平始终平衡
位于我省的“中国天眼”FAST,其“眼镜片”由金刚砂(SiC)制造。生产SiC的化学方程式为SiO2+3C SiC+2CO↑,消耗C的质量为36kg时,理论上可生产SiC的质量为多少?
SiC+2CO↑,消耗C的质量为36kg时,理论上可生产SiC的质量为多少?
 SiC+2CO↑,消耗C的质量为36kg时,理论上可生产SiC的质量为多少?
SiC+2CO↑,消耗C的质量为36kg时,理论上可生产SiC的质量为多少?
甲、乙、丙、丁在反应前后的质量关系如图所示,下列说法不正确的是( )
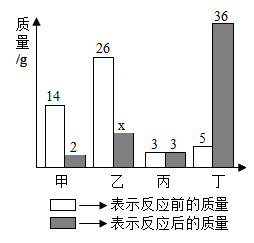
A . x值为7
B . 丁为生成物
C . 丙为不参加反应的杂质
D . 参加反应的甲和乙的质量比为12:19
镁在空气中燃烧,不仅能与氧气反应生成氧化镁,还能与氮气反应生成氮化镁(Mg3N2)。12g镁在空气中燃烧,生成物的质量可能为( )
A . 8g
B . 18g
C . 28g
D . 38g
科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图。下列说法错误的是( )
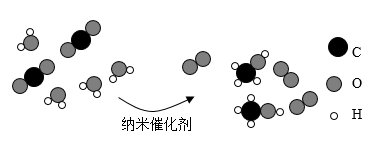
A . 催化剂的化学性质在反应前后没有发生变化
B . 生成物 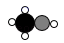 的化学式是
的化学式是  C . 两种反应物的质量比为3:4
D . 两种生成物的分子个数比为2:3
C . 两种反应物的质量比为3:4
D . 两种生成物的分子个数比为2:3
 C . 两种反应物的质量比为3:4
D . 两种生成物的分子个数比为2:3
C . 两种反应物的质量比为3:4
D . 两种生成物的分子个数比为2:3
已知向饱和食盐水中通入氨气得到饱和氨盐水,饱和氨盐水能与CO2发生反应:
 。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
 。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下: 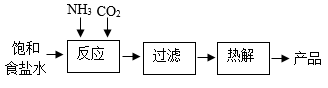
-
(1) 常温时,饱和氨盐水的pH(填“=”“<”或“>”)7.反应时,溶液中生成的NH4Cl中所含原子团的名称是。
-
(2) 过滤时,若过滤后滤液仍浑浊,其原因可能是(任写一条)。
-
(3) 热解时,NaHCO3分解得到纯碱、水和一种使澄清石灰水变浑浊的气体,该反应的化学方程式为。
铅“青金也”,能很好阻挡射线侵害,常用于医院防护,常用方铅矿(主要成分是PbS)制得。
I、古希腊人的焙烧熔炼法炼铅,其过程可简要表示为:
①焙烧:2PbS+3O2  2PbO+2SO2
2PbO+2SO2
②还原:高温时,用 C 还原 PbO 制得 Pb 和 CO2
II、现代湿法炼铅主要流程如下:
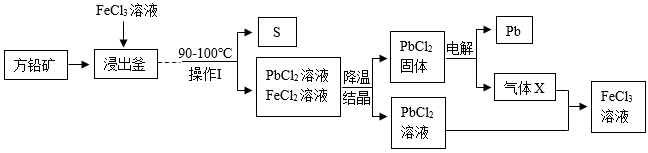
-
(1) 写出焙烧熔炼法炼铅中还原阶段反应的化学方程式。
-
(2) 操作 Ⅰ 的名称是。
-
(3) 写出湿法炼铅流程中气体 X 的化学式是。
-
(4) 对比以上两种炼铅方法,湿法炼铅的优点是(写一点)。
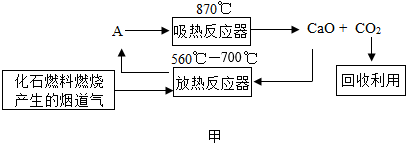
高效的CO2捕集和封存技术会为我国2060年实现“碳中和”目标作出巨大贡献。将CO2从排放物中分离出来的方法主要分为物理吸收法和化学吸收法。物理吸收主要是用甲醇(液体)、活性炭沸石等。化学吸收主要使用氨水、钙基吸收剂等。用氨水(NH3·H2O)吸收时,温度控制在30℃左右,采用喷氨技术吸收CO2生成碳酸氢铵;钙基吸收过程如图甲所示:

分离后的CO2可以用来制取甲醇(CH3OH)。2020年10月,中科院李灿院士团队的全球首套“千吨级液态太阳燃料合成示范项目”在兰州通过国家现场考核。其技术路径是:第一步就是采用光伏发电把光变成能量;第二步就是电解水制氢;第三步在固溶体双金属氧化物催化剂作用下二氧化碳加氢产生甲醇(CH3OH)和水。这一模拟自然光合作用的“液态阳光”生产甲醇技术,将是我国实现碳达峰、碳中和的一个重要路径,并为全球应对气候变化提供切实可行的中国方案、中国智慧。
-
(1) 用甲醇作溶剂吸收CO2 , 为提高吸收率应采用的温度和压强条件是 (填字母序号)。A . 高温、高压 B . 高温、低压 C . 低温、高压 D . 低温、低压
-
(2) 活性炭、沸石等可作吸收剂,是因为具备的结构特点是。
-
(3) 采用喷氨技术吸收CO2生成NH4HCO3过程中控制在30℃左右进行,温度不宜太高的原因是。
-
(4) 钙基吸收过程,放热反应器中发生反应的化学方程式是。
-
(5) “千吨级液态太阳燃料合成示范项目”技术路径第三步中发生反应的化学方程式为。
现有Fe2O3和CuO的混合物mg,在高温条下用足量的CO还原,得到金属混合物2.4g。将生成的CO2气体用足量的澄清石灰水全部吸收后,产生白色沉淀5.0g,则m的数值为( )
A . 3.2
B . 3.8
C . 4.6
D . 7.4
最近更新