摩尔质量及相关计算 知识点
摩尔质量及相关计算 知识点题库
①O3能吸收紫外线。与O3互为同素异形体的物质化学式是。
②SO2是一种大气污染物。SO2中S元素化合价是,S、O原子个数比是;SO2的摩尔质量为g/mol;1mol SO2中约含个S原子。
③大气中的CO2使地球保持温暖。将过多CO2转化为甲醇(CH3OH)等燃料的过程属于(选填“物理”、“化学”)变化;CH3OH由种元素组成。
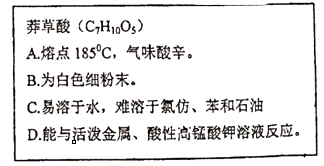
①莽草酸是由种元素组成;其摩尔质量是。
②莽草酸中氢、氧两种元素的质量比为。
③0.1mol莽草酸中含氢原子的个数为。
④如图信息中描述莽草酸物理性质的有。
 即分子或原子的相对质量
即分子或原子的相对质量 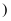 例如:1摩尔水中的水分子个数为6.02×1023个,1摩尔水的质量为18g。
例如:1摩尔水中的水分子个数为6.02×1023个,1摩尔水的质量为18g。
-
(1) 1摩尔水中氢原子数目是个。
-
(2) 1摩尔水中氧元素质量为g。
①燃烧废纸属于(选填“物理”“化学”)变化。废纸回收再利用可减少资源的浪费。
②某种易拉罐的材质中含有铝。铝的金属活动性(选填“>”“<”)铁。氧化铝中铝元素的化合价为。以下垃圾属于金属的是(选填编号)。
a.厨余垃圾 b.铜导线 c.过期药品 d.废气衣物
③生物全降解餐盒主要以淀粉为原料,可减少对环境的影响。淀粉属于(选填“有机”“无机”)物,淀粉可转化为葡萄糖(C6H12O6)。葡萄糖含有种元素,每摩尔葡萄糖分子中含摩尔碳原子,葡萄糖的摩尔质量为。
 B .
B . 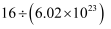 C .
C .  D .
D . 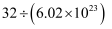
-
(1) 如图所示,在“树”上开出了5朵美丽的“花朵”。请按要求填写处符合要求的化学符号或化学符号所表示的含义:
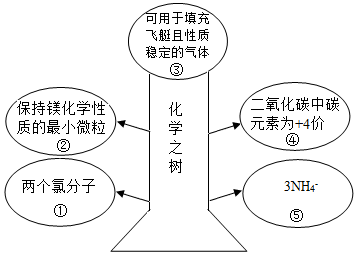
①;②;③;④;⑤。
-
(2) 二氧化硫是一种气体:
①
 由种元素组成,硫原子与氧原子的个数比为,氧原子与硫原子的物质的量比为,氧元素的质量分数为。
由种元素组成,硫原子与氧原子的个数比为,氧原子与硫原子的物质的量比为,氧元素的质量分数为。②
 的摩尔质量为,
的摩尔质量为, 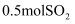 分子个数为,含氧原子的个数为。
分子个数为,含氧原子的个数为。 -
(3) 关于反应
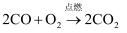 的读法或意义中,正确的是________。
A . 一氧化碳加氧气点燃等于二氧化碳 B . ―氧化碳和氧气在点燃条件下反应生成二氧化碳 C . 每2个一氧化碳分子与1个氧分子反应生成2个二氧化碳分子 D . 2g一氧化碳和1 g氧气在点燃条件下反应生成2 g二氧化碳
的读法或意义中,正确的是________。
A . 一氧化碳加氧气点燃等于二氧化碳 B . ―氧化碳和氧气在点燃条件下反应生成二氧化碳 C . 每2个一氧化碳分子与1个氧分子反应生成2个二氧化碳分子 D . 2g一氧化碳和1 g氧气在点燃条件下反应生成2 g二氧化碳
①15%的氯化钠溶液具有消毒作用,其中溶剂是,配置100g该溶液,需要氯化钠g。配置过程中会导致溶液质量分数偏大的可能原因是(写出一条即可)。
②对氯化钠溶液进行焰色反应,火焰呈色;滴加硝酸银溶液,观察到生成白色沉淀,请写出该反应的化学方程式。
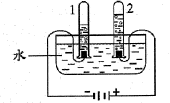
③下图电解水实验揭示了水的组成。实验中得到氢气的试管是(选填“1”“2”)。反应的化学方程式为。2mol水中约含个水分子。
④  、
、  、
、  在不同溶剂中的溶解度如下表所示。
在不同溶剂中的溶解度如下表所示。
表1  、
、  、
、  分别在水中的溶解度(g/100g水)
分别在水中的溶解度(g/100g水)
| t/℃ | | | |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 122 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
表2常温下,  、
、  、
、  分别在100g乙醇中最多溶解的质量
分别在100g乙醇中最多溶解的质量
| | | | |
| 最多溶解的质量(g) | 17.3 | <0.01 | 0.1 |
根据表1和表2提供的数据回答下列问题
Ⅰ.  在水中的溶解度随温度升高而(选填“增大”“减小”)。
在水中的溶解度随温度升高而(选填“增大”“减小”)。
Ⅱ.20℃时,饱和食盐水中溶质质量分数为。
Ⅲ.常温下,将  通入饱和
通入饱和  的乙醇溶液中,反应的方程式为,可观察到的现象。
的乙醇溶液中,反应的方程式为,可观察到的现象。
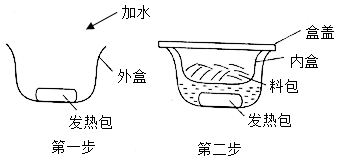
请回答:
-
(1) 发热包发热的原理用化学方程式表示:。
-
(2) 焙烧硅藻土、活性炭都有疏松多孔的结构,能起到作用。
-
(3) 发热包中若含有 0.1molNa2CO3 , 则其中碳原子为个。
-
(4) 自热火锅的内、外盒都由聚丙烯塑料材质制成,使用完毕,应将它们放入垃圾桶。(填字母序 号)
A 可回收 B 干垃圾 C 湿垃圾 D 有害垃圾
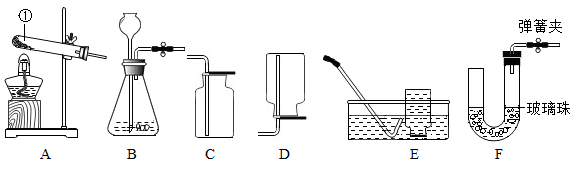
-
(1) 仪器①的名称是。
-
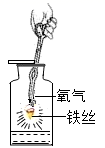
(2) 若用 A 装置制氧气,完全反应后,试管中剩余的固体药品是。
-
(3) 实验室用双氧水制氧气的发生装置应选择装置(填上图装置字母),化学方程式为:。研究显示O2的体积分数大于 36%时可使带火星的木条复燃,因此,氧气验满时采用带火星的木条复燃的方法(填“可靠”或“不可靠”),为了收集一瓶较纯净的氧气最好选择装置(填上图装置字母)。
-
(4) 图 F 所示的装置可以替代启普发生器制取二氧化碳。
I、该装置右侧放的药品是,左侧放的药品是。
II、使用该装置制取气体应满足的条件是。
III、请简述使该装置中反应停止的原理:。
-
(5) 实验室用 100g 的大理石与足量的稀盐酸制取二氧化碳,充分反应后生成 0.5mol 二氧化碳气体,请问参加反应的碳酸钙质量为多少克?(根据化学方程式列式计算)
①可燃冰是CH4与H2O在特殊条件下形成的物质。CH4的摩尔质量为,1molCH4中约含有个碳原子,含有g氢元素。
②水可以做制氢气的原料,图一是电解水的实验装置,请书写电解水的化学方程式,b中气体的化学式是;b中气体约是a中气体体积的倍。图二中,可观察到的现象是。
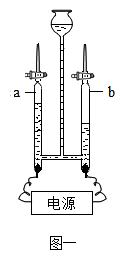
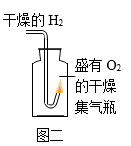
③水是实验室中常用的物质,请说出实验中水的作用。
| |
| |
|
①空气常新。空气是一种(选填“混合物”或“纯净物”),其中体积分数为21%的气体是(填写气体的化学式),该气体的用途是。(写一点即可)
②绿水长流。天然水中含有许多杂质,模拟自来水厂净水过程:其中吸附用到的物质是,除去异味、色素或有毒气体等:加氯的作用是。
③能源转型。天然气作为最具潜力的清洁能源,其主要成分是甲烷(CH4),属于(选填“有机”或“无机”)物,0.2mol甲烷分子中约含个碳原子。
-
(1) 防毒面具中使用了活性炭,这是利用了活性炭的作用。
-
(2) 草木灰是重要的化肥,其主要成分是碳酸钾,检验碳酸钾中的钾元素的方法是。
-
(3) 甲烷在自然界的分布很广,在空气中燃烧后,其反应的微观示意图如下:
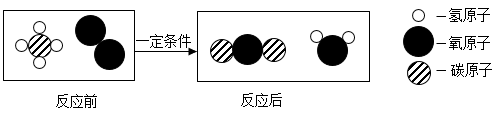
Ⅰ、甲烷的摩尔质量为,2mol甲烷分子中约含有个分子。
Ⅱ、反应过程中的甲烷和氧气的物质的量之比为。