硫酸盐 知识点题库
亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:

-
(1) SO2对环境的危害主要是形成。
-
(2) 用Na2CO3溶液能吸收SO2的原因是。
-
(3) 查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为(填化学式)。

-
(4) 实验时,“反应II”中加入NaOH溶液的目的是(用化学方程式表示)。
-
(5) 获得的Na2SO3产品久置后质量变重,主要原因是。
唐代中药学著作《新修本草》中,有关于“青矾”的记录为“本来绿色,新出窟未见风者,正如琉璃,……,烧之赤色”。据此推测,“青矾”的主要成分为()
A . CuSO4·5H2O
B . FeSO4·7H2O
C . KAl(SO4)2·12H2O
D . ZnSO4·7H2O
填写下列物质的化学式。
重晶石 明矾
用下列装置验证SO2的某些性质(加热及夹持装置略去)。

-
(1) 装有浓硫酸的仪器名称是。
-
(2) 铜与浓硫酸反应的化学方程式是。
-
(3) 能验证SO2具有氧化性的实验现象是。
-
(4) 装有BaCl2溶液的试管中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀的化学式分别是,。
-
(5) 写出SO2显示还原性并生成白色沉淀的总的离子方程式。
-
(6) 能验证SO2具有酸性氧化物的通性的实验现象。若通入过量的SO2 , 则其总反应的离子反应方程式是。
下列说法不正确的是( )
A . 石灰石、纯碱、石英可作为制备水泥的主要原料
B . 燃煤烟气的脱硫过程可以得到副产品石膏和硫酸铵
C . 硫酸钡可作高档油漆、油墨、塑料、橡胶的原料及填充剂
D . 在催化剂作用下,用玉米、高粱为原料经水解和细菌发酵可制得乙醇
硫代硫酸钠(Na2S2O3),又名大苏打、海波,它是无色透明的单斜晶体,熔点48℃。硫代硫酸钠(Na2S2O3)可作为照相业的定影剂,反应原理为AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr。
-
(1) Ⅰ.为了从废定影液中提取 AgNO3 , 设计如下实验流程。

“沉淀”步骤中生成 Ag2S 沉淀,检验沉淀完全的操作是。
-
(2) “反应”步骤中会生成淡黄色固体,该反应的化学方程式为。
-
(3) “过滤 2”的溶液获取 AgNO3晶体的操作是蒸发浓缩、冷却结晶、、、干燥。
-
(4) Ⅱ.下图是实验室模拟工业制备 Na2S2O3 的装置图。

依据图示回答下列问题:
装置 A 中盛放亚硫酸钠固体的玻璃仪器名称是,装置 B 的作用是。
-
(5) 分液漏斗中如直接用 98%的浓硫酸,烧瓶中固体易产生“结块”现象,使反应速率变慢。产生“结块”现象的原因是。
-
(6) 设置 K1导管的目的是为了防止拆除装置时造成空气污染。请简述操作方法。
-
(7) 硫代硫酸钠还可用于除去鞣制皮革时过量的重铬酸盐,将其还原成 Cr3+ , 理论上处理1mol Cr2O72-需要 Na2S2O3的质量为。
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
|
实验 |
试剂 |
现象 |
|
|
滴管 |
试管 |
||
|
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4溶液 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
| 0.1 mol·L−1 Al2(SO4) 3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
-
(1) 经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:。
-
(2) 经检验,现象Ⅱ的棕黄色沉淀中不含SO42− , 含有Cu+、Cu2+和SO32−。
已知:Cu+
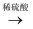 Cu +Cu2+ , Cu2+
Cu +Cu2+ , Cu2+  CuI↓(白色) +I2。
CuI↓(白色) +I2。①用稀硫酸证实沉淀中含有Cu+的实验现象是。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
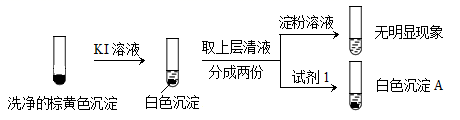
a.白色沉淀A是BaSO4 , 试剂1是。
b.证实沉淀中含有Cu2+和SO32−的理由是。
-
(3) 已知:Al2(SO4) 3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42− , 该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.被Al(OH) 3所吸附;
ii.存在于铝的碱式盐中。
对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
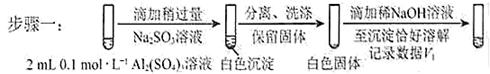
步骤二:(按上图形式呈现) 。
-
(4) 根据实验,亚硫酸盐的性质有。盐溶液间反应的多样性与有关。
北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是( )
A . 胆矾的化学式为CuSO4
B . 胆矾可作为湿法冶铜的原料
C . “熬之则成胆矾”是浓缩结晶过程
D . “熬胆矾铁釜,久之亦化为铜”是发生了置换反应
加入适量的硫酸溶液,可使溶液中下列离子数量显著减少的是( )
A . Cl-
B . Ba2+
C . NO3-
D . Na+
-
(1) 用大苏打(硫代硫酸钠)和硫酸溶液发生反应时溶液变浑浊的时间,也可研究外界条件对化学反应速率的影响。写出相应反应的化学方程式。
-
(2) 已知大苏打溶液与
 反应时,
反应时,  转移
转移  电子。该反应的离子方程式是。
电子。该反应的离子方程式是。
最近更新



