硫化氢 知识点题库
-
(1) 实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体.
①该反应的化学方程式为 .
②多余的H2S气体可用 溶液来吸收,不能用燃烧的方法处理H2S气体的理由是
-
(2) 用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:
2FeCl3+H2S=S↓+2FeCl2+2HCl,废吸收液经电解可循环使用.
①该反应中H2S显 (填字母).
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是 .
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为
-
(3)
已知:H2S在高温下分解生成硫蒸气和H2 . 现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示.表示H2的曲线是 (填“A”、“B”或“C”).
②生成硫蒸气的分子式为



 和
和  的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图: 
请回答:
-
(1) 三颈瓶中出现淡黄色沉淀,溶液呈强酸性,用一个化学方程式表示。
-
(2) 若通入水中的
 已过量,设计实验方案检验。
已过量,设计实验方案检验。
-
(1) 小方拟用H2O2与H2S反应,则氧化剂与还原剂的物质的量之比为。
-
(2) 小明结合已有知识,计划选用Cl2与H2S反应。在讨论设计实验方案时,小组同学提出两种方案:
方案I:用干燥Cl2与H2S反应
方案II:用潮湿的Cl2与H2S反应
小组同学设计了以下实验装置并动手实验、验证方案:
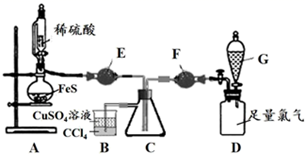
①证明以上装置气密性良好的具体操作是。
②仪器E的名称是。
③装置B的作用是。(答2点)
实验序号
实验操作
实验现象
结论
I
滴加稀硫酸,使H2S充满C瓶④ , 再打开G中的旋塞,缓慢通入Cl2至过量⑤。
C中有淡黄色固体产生,Cl2通入过量,淡黄色固体不消失。
淡黄色固体为单质硫,不会与过量的氯气反应。
II
撤去E、F装置,在C中加入少量水,先向C瓶通入H2S,再通入Cl2至过量。
C中看到淡黄色浑浊,通入Cl2过量,淡黄色沉淀消失⑥。
有水存在时,淡黄色固体会与过量氯气进一步反应。
④E中的试剂是。先通H2S排出装置中的空气,证明H2S已充满的现象是 (用离子方程式表示)。
⑤G中的试剂是。通过什么现象判断氯气已过量?。
⑥分析与讨论:实验II中黄色沉淀消失是S元素转变成了 (填离子符号),证明推测合理的实验操作和现象是:。
实验结论:-2→0硫元素的转化,氧化剂的选择、用量和反应环境均会影响结果。

 溶液褪色
D . e、f均为二元强酸
溶液褪色
D . e、f均为二元强酸
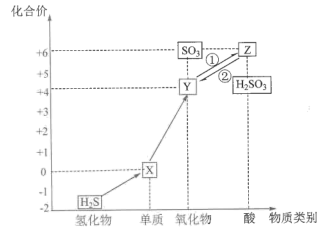
 气体混合能实现转化①
气体混合能实现转化①
选项 | 试剂 | 制备的气体 |
A | 氯酸钾、浓盐酸 | Cl2 |
B | 铜、浓硫酸 | SO2 |
C | 浓硫酸、硫化亚铁 | H2S |
D | 稀硝酸、锌 | H2 |



