探究碳酸钠与碳酸氢钠的性质 知识点题库
向某碳酸钠溶液中逐滴加1 mol·L─1的盐酸,测得溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法中正确的是 ( )
A . Oa段反应的离子方程式与ab段反应的离子方程式相同
B . 该碳酸钠溶液中含有1mol Na2CO3
C . b点的数值为0.6
D . b点时生成CO2的物质的量为0.3 mol
用下列装置不能达到有关实验目的是( )
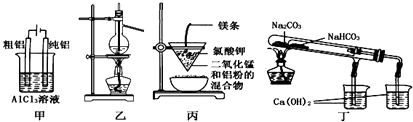
A . 用甲图装置电解精炼铝
B . 用乙图装置蒸馏海水
C . 用丙图装置可制得金属锰
D . 用丁图装置验证NaHCO3和Na2CO3的热稳定性
下列叙述中正确的是( )
A . 向NaHCO3溶液中滴加澄清石灰水,不会产生沉淀
B . 等质量NaHCO3和Na2CO3分别与足量盐酸反应,生成的CO2在同温同压下体积相同
C . 向Na2CO3溶液中缓慢通入等物质的量的HCl,生成的CO2与原Na2CO3的物质的量之比为1:2
D . 向Na2CO3饱和溶液中通入CO2 , 有晶体析出
X、Y、Z、W四种物质的转化关系.下列组合中不符合该关系的是( )

A . A
B . B
C . C
D . D
下列关于碳酸钠和碳酸氢钠的比较中不正确的是( )
A . 二者在水中的溶解度不同,碳酸氢钠的溶解度小于碳酸钠
B . 二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠
C . 二者都能与盐酸反应放出二氧化碳气体,等质量时生成CO2的物质的量一样多
D . 二者在一定条件下可以相互转化
某学习小组的同学按下列实验流程制备Na2CO3 , 设计的部分装置如图所示。

下列叙述正确的是( )
A . 若X为浓氨水,Y为生石灰,则可用装置甲制取NH3
B . 反应①可在装置乙中发生,反应②可在装置丁中发生
C . 可用装置丙进行过滤操作
D . 将母液蒸干灼烧后可得到NH4Cl固体
下列鉴别Na2CO3和NaHCO3两种白色粉末的方案不能达到预期目的的是( )
A . 分别向等物质的量的白色粉末中加入足量盐酸,充分反应后,比较产生气体的体积
B . 分别向等物质的量的白色粉末中加入等体积、等浓度的稀盐酸,比较生成气体的快慢
C . 分别用图示装置进行实验,观察澄清石灰水是否变浑浊 D . 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
D . 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
 D . 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
D . 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2 , 再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:

-
(1) 原NaOH溶液的物质的量浓度为。
-
(2) 曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是,其物质的量之比为。
-
(3) 曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况下)的最大值为mL。
-
(4) 硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)=2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是。
加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl的物质的量的关系如下图(忽略CO2的溶解和HCl的挥发)。

则下列分析都正确的组合是( )
①Ⅰ图对应溶液中的溶质为NaHCO3
②Ⅱ图对应溶液中的溶质为Na2CO3和NaHCO3 , 且二者的物质的量之比为1:1
③Ⅲ图对应溶液中的溶质为NaOH和Na2CO3 , 且二者的物质的量之比为1:1
④Ⅳ图对应溶液中的溶质为Na2CO3
A . ①②
B . ①③
C . ②④
D . ②③
关于相同物质的量浓度的NaHCO3溶液和Na2CO3溶液,下列说法错误的是( )
A . 溶液中所含离子的种类相同
B . 溶液的pH相同
C . 都能与盐酸反应放出CO2气体
D . 都能使澄清石灰水变浑浊
下列关于金属及其化合物说法错误的是( )
A . 氧化铝用作耐火材料
B . 小苏打用于食品膨松剂
C . 纯碱用于中和胃酸过多
D . 氧化铁可用作涂料
下列方法不能用于鉴别Na2CO3和NaHCO3固体的是( )
A . 分别取两种固体各1g,滴入几滴水振荡,用手触摸试管底部
B . 分别取等质量的固体与足量稀盐酸充分反应,加热、蒸干、灼烧、称重
C . 分别取两种固体溶于水,滴加BaCl2稀溶液溶液,观察是否生成沉淀
D . 分别将少量的两种固体溶于水,加入Ca(OH)2溶液,观察是否生成沉淀
下列实验中,实验操作能达到实验目的的是 ( )
| 选项 | 实验操作 | 实验目的 |
| A | 将炽热的木炭与浓硝酸混合所得气体通入澄清石灰水中 | 验证碳的氧化产物为CO2 |
| B | 向饱和碳酸钠溶液中通入二氧化碳 | 探究Na2CO3和NaHCO3溶解度相对大小 |
| C | 向某溶液中滴加BaCl2溶液和稀硝酸 | 检验原溶液中是否含SO |
| D | 向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 | 验证淀粉已水解 |
A . A
B . B
C . C
D . D
下列过程不涉及化学反应的是( )
A . 用含NaHCO3的干粉灭火剂灭火
B . 用活性炭口罩防护空气中的粉尘等有害物质
C . 向95%酒精中加生石灰蒸馏来制取无水酒精
D . 含活性炭、细铁、食盐及蛭石等的暖手宝,在被使用时会发热
下列有关实验装置进行的相应实验,能达到实验目的的是( )

A . 用图1所示装置制取干燥的氨气
B . 图2装置可用于制取少量纯净的CO2气体
C . 用图3所示装置将溶液定容到100 mL
D . 图4装置可用于比较碳酸钠和碳酸氢钠的热稳定性,大试管A中装碳酸钠固体,小试管B中装碳酸氢钠固体
下列鉴别等浓度的碳酸钠和碳酸氢钠溶液方法正确的是( )
A . 分别取少量溶液于试管中,滴入几滴酚酞溶液,溶液红色深旳是碳酸钠;溶液红色浅的是碳酸氢钠
B . 分别取少量溶液于试管中,滴入几滴澄清石灰水,产生沉淀的是碳酸钠;不产生沉淀的是碳酸氢钠
C . 分别取适量溶液于试管中,逐滴滴入适量盐酸,先产生气泡的是碳酸氢钠;后产生气泡的是碳酸钠
D . 分别取少量溶液于试管中,加入适量氢氧化钠溶液,产生沉淀的是碳酸钠;不产生沉淀的是碳酸氢钠
下列图示方法能完成相应实验的是( )
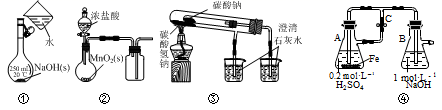
A . 用图①配制一定物质的量浓度的NaOH溶液
B . 用图②在实验室制取Cl2
C . 用图③探究碳酸氢钠和碳酸钠的热稳定性
D . 用图④制备少量Fe(OH)2并能较长时间看到其白色
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图中I~IV所示。

-
(1) 只根据图I、II所示实验,能够达到实验目的是(填装置序号)。
-
(2) II所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的装有(填化学式)。
-
(3) 图III、IV所示实验均能鉴别这两种物质,与实验III相比,实验IV的优点是(填选项序号)___________。A . IV比III复杂 B . IV比III安全 C . IV可以做到用一套装置同时进行两个对比实验,而III不行
-
(4) 若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)。
有关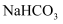 和
和 的性质,以下说法不正确的是( )
的性质,以下说法不正确的是( )
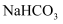 和
和 的性质,以下说法不正确的是( )
的性质,以下说法不正确的是( )
A . 热稳定性较好的是 B . 可用澄清石灰水鉴别
B . 可用澄清石灰水鉴别 溶液和
溶液和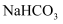 溶液
C . 相同温度下,等物质的量浓度的溶液中分别滴入酚酞,红色较浅的是
溶液
C . 相同温度下,等物质的量浓度的溶液中分别滴入酚酞,红色较浅的是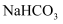 D . 1g碳酸钠固体和1g碳酸氢钠固体中分别加入几滴水后,测得温度较高的是
D . 1g碳酸钠固体和1g碳酸氢钠固体中分别加入几滴水后,测得温度较高的是
 B . 可用澄清石灰水鉴别
B . 可用澄清石灰水鉴别 溶液和
溶液和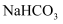 溶液
C . 相同温度下,等物质的量浓度的溶液中分别滴入酚酞,红色较浅的是
溶液
C . 相同温度下,等物质的量浓度的溶液中分别滴入酚酞,红色较浅的是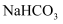 D . 1g碳酸钠固体和1g碳酸氢钠固体中分别加入几滴水后,测得温度较高的是
D . 1g碳酸钠固体和1g碳酸氢钠固体中分别加入几滴水后,测得温度较高的是
最近更新




