饱和溶液与不饱和溶液相互转变 知识点题库
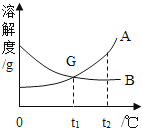
如图为甲、乙两种物质的溶解度曲线,请回答下列问题:
(1)20℃时,为使接近饱和的甲物质溶液变为饱和溶液的方法是:(任写一种方法即可);
(2)40℃时,乙物质的溶解度是 g.此温度下,该饱和溶液中乙物质的质量分数是 .(精确到0.1%)
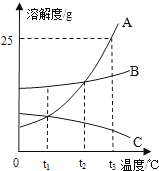
A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
(1) ℃时,A、B两种物质在100g水中达到饱和状态时溶解的质量相等;
(2)若B中混有少量的A,最好采用的方法提纯B;
(3)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:①加入C物质;②恒温蒸发溶剂;③;
(4)t3℃时将20g A物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是 ;
(5)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是 .
A、B两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题.
(1)现有常温下B的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可行的方法有 .
(2)现有一杯t1℃时含A、B两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作方法是 .
(3)下列说法正确的是 .
①t2℃时,A的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
②将t2℃A、B的饱和溶液分别降温至t1℃,此时两溶液中的质量分数相等;
③在t1℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等;
④在t2℃时,用等量的A、B分别配制成两种饱和溶液,测得其质量依次为m1g和m2g,则m1<m2 .
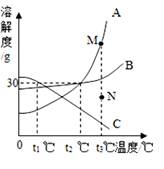
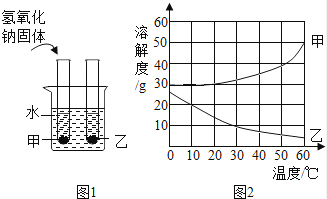
甲、乙两物质的溶解度曲线如图2所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯里,然后向烧杯中加入适量的氢氧化钠固体,搅拌至完全溶解(如图1),此时对相应变化的判断正确的是( )
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 | 39.8 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
-
(1) 60℃时,向两个分别盛有25g NaCl和NH4Cl的烧杯中,各加入50g的水,充分溶解后,为饱和溶液的是溶液.
-
(2) 若采用一种操作方法,将上述烧杯中的剩余固体全部溶解,使其变为了不饱和溶液.对此有下列的四种说法,其中正确的是 (选填字母).A . 采用的是升高温度的方法 B . 采用的是增加溶剂的方法 C . 溶质的质量保持不变 D . 溶液的质量一定增加.
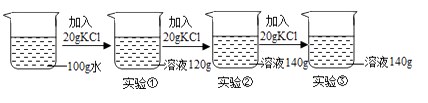
-
(1) 实验③所得溶液的质量分数是。3 次实验所得溶液质量分数由小到大的关系 是。
-
(2) 实验②的溶液是否为饱和溶液?(填“是”“不是”或者“无法判断”)。
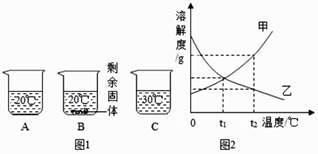
-
(1) 烧杯中的溶液一定属于饱和溶液的是(填序号)。
-
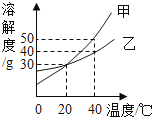
(2) 在图 2 中,能表示硝酸钾溶解度曲线的是(填“甲”或“乙”)。
-
(3) 要使烧杯 B 中剩余固体继续溶解,可采用的方法是(填一种即可)。
-
(4) 依据图 2 的分析判断,若分别将 100g 甲、乙的饱和溶液从 t2℃降温到 t1℃,对所得溶液的叙述正确的是 (填序号)。A . 甲、乙都是饱和溶液 B . 所含溶剂的质量:甲<乙 C . 溶液的质量:甲>乙 D . 溶质的质量分数:甲>乙
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
|
溶解度/g |
27.6 |
31.0 |
34.0 |
37.0 |
x |
42.6 |
45.5 |
小明为测定x的值,取4份40℃的水各50g,分别进行实验,并记录数据如下表.
|
实验编号 |
实验1 |
实验2 |
实验3 |
实验4 |
|
KCl质量/g |
5 |
15 |
25 |
35 |
|
溶液质量/g |
55 |
65 |
70 |
70 |
请回答下列问题.
-
(1) 要使实验2的溶液达到饱和,可采取的方法是.
-
(2) 小明现要配制质量分数为30%的KCl溶液100g,为达实验目的其主要操作是.
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度/g |
氯化钠 |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
硝酸钾 |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
|
-
(1) 要使20℃的氯化钠不饱和溶液变成饱和溶液,可采用的方法。(写出一种即可)
-
(2) 当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法是。