有关化学式的计算和推断 知识点题库
某金属元素R,它的氢氧化物的相对分子质量为m,它的氯化物的相对分子质量为n。则该金属元素R的化合价为。
帕拉米韦氯化钠注射液是治疗H7N9亚型禽流感的有效药物之一,帕拉米韦的化学式为C15H28NxO4。试计算:
-
(1) 帕拉米韦的相对分子质量为328,则x的数值为;
-
(2) 32.8 g的帕拉米韦中氧元素的质量为 g(写出计算过程结果精确到0.1 g)。
丙酸钠是一种常用的食品添加剂,其化学式为C3H5OxNa;已知该化合物中碳元素与氧元素的质量比为9:8,请计算:
-
(1) 丙酸钠由 种元素组成;
-
(2) X=;
-
(3) 该物质的相对分子质量是 。
高致病性禽流感病毒正威胁着人类的健康和安全,对抗禽流感病毒是人类的重大课题。“达菲”是目前世界上对抗禽流感病毒的良药。生产“达菲”的主要原料是莽草酸,莽草酸的化学式为[C7H10O5],请根据信息回答:
-
(1) 莽草酸由种元素组成;一个莽草酸分子中共含有个原子;
-
(2) 莽草酸属于(填“单质”或“化合物”);
-
(3) 莽草酸中氢、氧元素质量比为;
-
(4) 174g莽草酸中含有g碳元素。
有机物是自然界物质中的一个大家族。
-
(1) 下列是生活中常见的物质:①尿素[CO(NH2)2]②纯碱(Na2CO3)③酒精(C2H5OH)
④葡萄糖(C5H12O5),属于有机物的是(选填序号)。
-
(2) 食醋是生活中常用的调味品,其主要成分是乙酸(CH3COOH)在乙酸分子中碳、氢、氧的原子个数比是 。
-
(3) 一定质量的某有机化合物X与8克氧气恰好完金反应,生成8.8克二氧化碳和1.8克水。X中各元素的质量比为。
在FeO、Fe.2O3、和CaCO3的混合物中,已知铁元素的质量分数为56%,则CaCO3的质量分数可能是( )
A . 5%
B . 15%
C . 25%
D . 35%
下列含铁的化合物中,铁元素质量分数最高的是( )
A . Fe(OH)3
B . Fe2O3
C . FeSO4
D . Fe3O4
新冠疫情期间,医院对苯酚(化学式C6H6O)、甲基苯酚(化学式C7H8O)等杀菌消毒物质的需求量大增。甲基苯酚质量分数为50%的溶液俗称来苏尔水,对粘膜和皮肤有腐蚀作用,需稀释后再使用。请回答下列问题:
-
(1) 94g苯酚与g甲基苯酚中含有的氧元素质量相同
-
(2) 某医院住院部对医疗器械进行消毒需1000g 2%的来苏尔水,其中含有甲基苯酚的质量为多少?
由于新冠肺炎疫情影响,学校为每个班级配备了消毒片,该消毒片加水活化后可杀灭物体表面、空气中的细菌等微生物。相关信息如图所示:


-
(1) 二氧化氯(ClO2)中氯元素的化合价为价。
-
(2) 实验室制备二氧化氯的化学方程式为:2NaClO2+Cl2=2ClO2+2X,请写出X的化学式。
-
(3) 教室课桌椅、讲台等高频接触表面,可用有效氯250-500mg/L的含氯消毒液进行喷洒消毒。有效氯可定量表示消毒效果,ClO2中有效氯的计算方式为:5×消毒片中氯元素质量+溶液体积。某同学在1升水中放入5片该消毒片,并充分溶解,请通过计算说明是否符合消毒要求?(消毒片中除ClO2外其他成分不含氯元素)
含硫的物质在实验室或工业生产过程中可出现下列图示的转化:


-
(1) 实验室中,点燃少量单质硫于充满氧气的集气瓶中燃烧,产生漂亮的蓝紫色火焰,生成物质A.A是工业排放物中一种主要的空气污染物,也是酸雨形成的主因之一.根据你学过的知识可将A转化成Na2SO3 , 你提供的试剂是.
-
(2) 在硫酸工业中,将A在一定条件下与空气中的物质反应得到B,B与水结合得到硫酸.B与A的组成元素相同,B中硫元素与硫酸中硫元素化合价相同,写出A转化成B的化学方程式:.
-
(3) 上述物质转化过程中,属于化合反应的是(填序号).
-
(4) 若回收工业排放物A 32吨,理论上可生产硫酸 吨.
某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每一步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( )

小资料:碱石灰的主要成分是氧化钙和氢氧化钠
A . 一定没有二氧化碳
B . 可能含有甲烷和氢气
C . 可能只有甲烷
D . 可能含有氢气和一氧化碳
等质量的H2、O2、N2所含分子数最多的是,各取它们的一个分子,则质量大小的排列顺序为.
仙居杨梅享誉全国,春季需要给杨梅适当的补充氮肥,小柯和爸爸一起去买化肥。农资店里有多种氮肥,价格不一。最后,爸爸在硝酸铵[NH4NO3]和尿素[CO(NH2)2]两种氮肥之间纠结,这两种氮肥的每千克售价分别为4.0元和5.0元,不知道买哪一种更好。于是小柯就用自己所学的科学知识帮爸爸做了正确的选择。请问小柯选择了哪一种氮肥?他的依据是什么?请通过计算说明。
绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。

-
(1) 菱肉中的钙、磷、铁等元素是以(填“单质”或“化合物”)的形态存在;
-
(2) 该纤维素中C、H、O元素的质量比(最简比) ;
-
(3) 查阅资料获悉菱肉制成的菱粉质细爽滑,为淀粉中之佳品。求菱叶产生3.6千克淀粉[有机物(CH2O)n]的同时,光合作用产生氧气多少千克?
(已知光合作用的化学方程式为:nCO2+nH2O=(CH2O)n+nO2:条件忽略)
使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是;质量相等的CO2和CO中,氧元素的质量比是 。
在江南,有句俗语叫做“清明螺赛肥鹅”,螺蛳之所以鲜美是因为螺肉内含有谷氨酸等多种增鲜物质,已知谷氨酸的化学式为C5H9NO4 , 请回答以下问题。
-
(1) 该物质是由种元素组成。
-
(2) 该物质中碳、氧元素的质量比是 。
-
(3) 14.7克谷氨酸中氧元素的质量与多少克Ca(OH)2中氧元素的质量相等?(要求写出计算过程)
吸烟对人体是有害的,特别是未成年人吸烟更有害。因为吸烟时,肺里会吸入一种易溶于水的剧毒物质尼古丁,又名烟碱,其化学式是C10H14N2。求:
-
(1) 尼古丁中各元素的质量比;
-
(2) 尼古丁中碳元素的质量分数(结果保留1位小数);
-
(3) 162克尼古丁中碳元素的质量与多少克二氧化碳中碳元素的质量相等?
我国将力争2060年前实现碳中和,CO2的捕捉可减少碳排放。
-
(1) 下左图是利用NaOH溶液“捕捉”(吸收)CO2部分流程图:


①操作①的名称是。
②捕捉室中NaOH溶液常喷成雾状,优点是。
-
(2) CaO固体也可以捕捉回收CO2 , 化学方程式为CaO+CO2
 CaCO3。研究表明CaC2O4⋅H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4⋅H2O进行加热,固体质量随温度变化如上右图。
CaCO3。研究表明CaC2O4⋅H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4⋅H2O进行加热,固体质量随温度变化如上右图。 ①写出400~600℃范围内分解反应的化学方程式: (CaC2O4⋅H2O的相对分子质量:146)。
②据图分析,CaO捕捉CO2的反应温度应(填“高于”或“低于”)800℃。
模型可以反映客观现象,简单明了地表示事物。根据下图模型回答问题。

-
(1) 乙炔是一种简单的有机物,其分子结构模型如图甲所示,乙炔中碳、氢两种元素的质量比为
-
(2) 尿素(
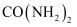 )是一种常见的化肥,图乙是尿素中各元素质量分数的模型,则图中的B表示的是元素。
)是一种常见的化肥,图乙是尿素中各元素质量分数的模型,则图中的B表示的是元素。
-
(3) 若乙炔分子和尿素分子
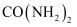 的个数相同,则它们所含碳原子的个数比。
的个数相同,则它们所含碳原子的个数比。
过氧化氢(H2O2)和水(H2O)在一定条件下都可以制取氧气,但两者性质完全不同。请回答:
-
(1) 过氧化氢和水中氧元素的化合价分别是。
-
(2) 小科同学通过比较过氧化氢和水的化学式就得出“过氧化氢的含氧量(氧元素的质量分数)是水的2倍“的结论。请你通过计算说明小科的结论是否正确。
-
(3) 小科用如图装置进行氧气的制取,该装置的圆底烧瓶中放入50毫升水的目的是。

最近更新



