有关化学式的计算和推断 知识点题库
下列是计算氢氧化钙[Ca(OH)2]相对分子质量的式子,其中正确的是( )
A . 40+16+1=57
B . 40+2×(16+1)=74
C . 40×16+1=640
D . 40×2×16×1=1280
我国科学家屠呦呦发现的青蒿素(化学式:C15H22O5),是一种用于治疗疟疾的药物,挽救了全球数百万人的生命,因而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素发现之前最热门的抗疟药物之一。回答下列问题。
-
(1) 一个青蒿素分子中含有个原子。
-
(2) 青蒿素中的氢元素与氧元素的质量比是。
-
(3) 14.1克青蒿素中含有碳元素的质量和多少克磺胺中含有碳元素的质量相等?
三氧化二碳【化学式(C2O3)】通常情况下是一种无色无味的气体,可溶于水、与水反应生成草酸,且常温下不稳定,其他的化学性质与一氧化碳相似。下列有关三氧化碳说法错误的是( )
A . C2 O 3中碳元素的化合价为+4价
B . 三氧化碳具有还原性
C . 在空气中燃烧的产物为二氧化碳
D . 与氢氧化钠溶液反应可生成盐
现有一份双氧水溶液,它由m个H2O分子和n个H2O2分子混合构成。(以下三空答案均用含字母m和n的式子表示)
-
(1) 该溶液中一共含有个氧原子。
-
(2) 该溶液中氢元素与氧元素的质量比为。
-
(3) 该双氧水溶液溶质的质量分数为。
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16克放入烧杯,把80克稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应).请计算:
|
序号 |
第一次 |
第二次 |
第三次 |
第四次 |
|
加入稀盐酸的质量/克 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
11 |
6 |
2.8 |
n |
-
(1) 如表中n的数值为 。
-
(2) 样品中碳酸钙的质量分数为 。
-
(3) 小明同学计算所用盐酸的溶质质量分数,计算过程如下:
解:设盐酸的溶质质量分数为x
CaCO3+
2HCl=CaCl2+H2O+CO2↑
100
73
13.2g
80x
100:73=13.2:80x
x=12%
小明的计算过程中存在明显错误,请你通过列式计算进行纠正?
金秋十月,余姚大岚的柿子挂满了枝头。林子味道爽口,甜而不腻,它的营养价值非常丰富一含多种维生素、人体所需的微量元素,但同时它又含有大量的鞣酸(C76H52O46)物质,在胃酸的作用下与其他食物中的钙、锌、镁、铁等矿物质凝结成大小不等的块状,不被人体所吸收,所以柿子不宜多食。
-
(1) 成熟的柿子吃起来甜甜的,这种甜性物质主要存在于细胞的。(填细胞结构名称)
-
(2) 鞣酸中碳、氢、氧三种元素的原子个数比为。
-
(3) 鞣酸中质量分数最大的元素是。(填元素符号)
健康的身体需要洁净的饮用水,明矾晶体(化学式KAl(SO4)2·12H2O)是一种常用的净水剂,它由种元素组成,其中元素质量分数最小的是元素。
某物质可能含有铁的氧化物中的一种或两种,实验测得其中铁元素的质量分数为75%,则该物质可能为( )
A . FeO
B . Fe3O4和Fe2O3的混合物
C . Fe2O3
D . FeO和Fe2O3的混合物
已知FeO、Fe2O3 和Fe3O4组成的混合物中,铁元素和氧元素的质量比为21∶8,则混合物中Fe2O3、FeO和Fe3O4三种物质的质量比可能是( )
A . 18∶20∶5
B . 9∶20∶33
C . 2∶3∶5
D . 40∶18∶31
为了了测定某品牌食用纯碱中碳酸钠的质量分数,小明取10克食用纯碱样品和足量的稀硫酸,进行如图甲实验,实验前后,均需往装置中缓慢通一会儿氮气.(样品中其他成分不与稀硫酸反应)

-
(1) 实验前,先往A装置通入一会儿氮气的目的是;
-
(2) 小金想用碱石灰(氢氧化钠固体和生石灰的混合物)来代替B装置中浓硫酸的吸水作用,小科认为不可以,其理由是;
-
(3) 根据乙图分析,判断反应生成的二氧化碳已被完全吸收的依据是;
-
(4) 下列情况会造成碳酸钠的质量分数偏大的是A . 稀硫酸换为浓盐酸 B . 反应结束后忘记通氮气 C . 样品中的碳酸钠没有反应完 D . 外界空气通过导管进入C 装置
阅读材料并回答问题:
材料一:中国人首先发明火箭这一事实被世界所公认。宋朝时出现的爆竹是原始的喷气式火箭;明朝时出现的“火龙出水”火箭是近代火箭的始祖;明朝时万户进行了最早的火箭升空试验(如图甲所示),成为载人飞行先驱。
材料二:2020年11月24日,长征五号遥五运载火箭(如图乙所示)成功发射嫦娥五号探测器,开启中国首次地外天体采样返回之旅。从1970年4月,长征一号运载火箭成功发射东方红1号卫星开始到现在,我国火箭研究与应用处于世界领先水平。
材料三:现代火箭的飞行原理与万户的升空试验原理基本相同。现代火箭大多是利用喷气发动机(如图丙所示)升空的,而喷气发动机是利用燃料在燃烧室中燃烧,燃气经喷管向后高速喷出,从而获得向前的动力。

-
(1) 如图甲所示,万户升空试验所用火箭的燃料为“黑火药”,黑火药爆炸的原理为:2KNO3+S+3C=X+N2↑+3CO2↑,其中反应物硝酸钾属于(选填“酸”“碱”或“盐”)物质X的化学式。
-
(2) 如图乙所示,火箭上升过程中与大气摩擦产生大量的热,这是通过的方式改变物体的内能;火箭以液态氢做燃料主要原因是氢气的大。
-
(3) 汽油机的冲程工作时的原理跟如图丙所示的喷气发动机燃烧室工作时的原理一致。
茶叶中含有一种物质儿茶素(C15H14O6),它有降低血脂、抑制动脉硬化等作用。下列关于儿茶素的说法正确的是( )
A . 儿茶素由3种原子组成
B . 儿茶素的相对分子质量是290克
C . 一个儿茶素分子中含有35个原子
D . 儿茶素中碳氧元素的质量比为15:6
小明在学习了元素和物质的知识后,进行了梳理,其中正确的是( )
A . 铁元素的质量分数由高到低:FeO、Fe2O3、FeS
B . 钙的化合物在水中的溶解性由大到小:CaCl2、CaCO3、Ca(OH)2
C . 氮元素的化合价由高到低:HNO3、NH3、NO
D . 空气中主要气体的体积分数由大到小:O2、N2、CO2
莽草酸(C7H10O5)是制取抗流感药物”达菲”的原料,试计算。
-
(1) 莽草酸的相对分子质量为。
-
(2) 克莽草酸含碳元素的质量为168g。
-
(3) 对1岁以上的儿童推荐按照下列”体重一剂量表”服用”达菲”:
体重
小于等于15kg
15~23kg
23~40kg
大于40kg
每次用量
30mg
45mg
60mg
75mg
假如患病儿童的体重是20kg,在治疗过程中,需每天服用”达菲”药片(每粒药片含“达菲”75mg)2次,一个疗程5天,那么该患儿一个疗程共服用粒。
易拉罐的主要成分是铝镁合金(已知其他杂质不溶于酸也不与稀硫酸反应),为了测定易拉罐铝镁合金中两种元素的质量比,小科开展了如图甲的实验,实验中生成沉淀的质量与滴入氢氧化钠溶液的质量的关系如图乙所示。
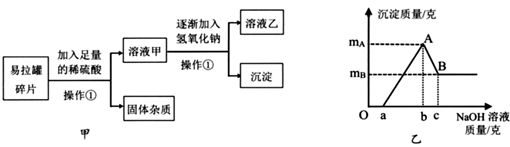
资料:氢氧化铝是一种白色沉淀,可与氢氧化钠反应:Al(OH)3+NaOH=NaAlO2+2H2O,氢氧化镁不与氢氧化钠反应。
-
(1) 从图可知,当滴入氢氧化钠溶液克时,溶液乙中有且只有一种溶质(填化学式)。
-
(2) 根据实验数据,该易拉罐中铝元素和镁元素的质量比为(用mA和mB表示)
新装修房间中往往会含有较多的甲醛,人体长期摄入超标的甲醛会对健康造成影响。甲醛的化学式为HCHO,请回答下列问题:
-
(1) 甲醛由种元素组成。
-
(2) 甲醛中碳、氢、氧元素的质量比为。(填最简整数比)
-
(3) 计算甲醛中氢元素的质量分数。(结果精确到0.01%)
某赤铁矿石(主要成分为氧化铁)中含铁56%,求此赤铁矿石中氧化铁的纯度(质量分数)。
黑火药由硝酸钾、硫黄和木炭组成。爆炸时主要反应的化学方程式为2KNO3+S+3C  K2S +N2↑+3CO2↑。下列有关理解不正确的是( )
K2S +N2↑+3CO2↑。下列有关理解不正确的是( )
 K2S +N2↑+3CO2↑。下列有关理解不正确的是( )
K2S +N2↑+3CO2↑。下列有关理解不正确的是( )
A . K2S中S元素的化合价为-2价
B . N2中“2”表示两个氨原子
C . “3CO2"表示 3个二氧化碳分子
D . KNO3中K,O元素的质量比为13 : 16
-
(1) 某正三价金属与氧元素形成的化合物中氧元素质量分数为 30%,则该金属的相对原子质量为;
-
(2) 元素R可与氧形成多种化合物,其中RO中含氧53.33%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。
2022年4月19日,一头抹香鲸在浙江省宁波市象山县一片海域附近搁浅。
-
(1) 抹香鲸因体内分泌有香料“龙涎香”而得名。龙涎香醇(化学式:C30H52O ) 是龙涎香的主要成分,其碳、氢的元素的质量比为。
-
(2) 抹香鲸搁浅死亡的主要原因是搁浅后,抹香鲸没了海水的散热帮助,会迅速升温导致生理机制崩溃而死。正常情况下,当抹香鲸体内温度升高时,为保持体温恒定,体表血管会呈现图状态来降温。
最近更新



