制取氧气的装置、步骤、收集与注意事项 知识点题库
根据下列实验装置图,回答问题:

-
(1) 实验仪器的名称:a;b.
-
(2) 实验室用高锰酸钾制取氧气的化学方程式为:,发生装置应该选用,该装置有一处不足,请改正:.要收集到较纯净的氧气,应该选用装置,若用该装置收集的氧气也不纯,原因可能是.
某校化学兴趣小组学习了气体的制取和收集后,对相关知识进行总结,请你一起参与,并完成下面题目内容:

-
(1) 写出下列仪器名称:a ,b .
-
(2) 若用D装置收集氧气,则氧气应从 口通入 (填“c”或“d”).
-
(3) 装置B可用于制取CO2,实验室制取二氧化碳的化学方程式为 .
-
(4) 若用装置E收集CO2并测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是: .
如图是初中化学实验室常见气体的制取装置:
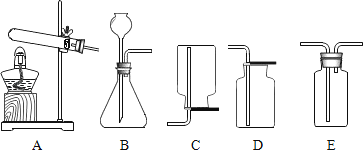
-
(1) 实验室制取氧气的原理之一是 (用化学方程式表示),此原理对应的发生装置是 (填序号〕.用D装置收集氧气,验满的方法是;
-
(2) 收集二氧化碳应选择的装置为 (填序号).理由是 , 欲收集一瓶干燥的二氧化碳,还需选用E装置,则E中应装入的药品是 .
a.取5~6只集气瓶,用量筒分别测出它们的容积并标记;
b.向集气瓶中分别装入其总容积的10%、20%、30%、40%、50%的水,并用毛玻璃盖住,依次编号为1、2、3、4、5。
c.在反应容器中加入一定量的MnO2和H2O2使其反应,分别用排水法将上述1~5号瓶中的水排出。
d.将带火星的木条依次插入1~5号瓶中,观察并记录现象如下表:
集气瓶号 | 1 | 2 | 3 | 4 | 5 |
木条火星状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
-
(1) 写出上述方法制取氧气的化学方程式 ;
-
(2) 假定空气的成分只体积比为4:1的氮气和氧气,则用排水法得到氧气后,2号瓶中氧气的体种分数约为;
-
(3) 若要得到更精确的数据,你认为下一步应如何操作?
-
(4) 实验结果表明用“使带火星的木条是否复燃”的方法来检验集气瓶中氧气是否集满的方法是否可靠?。
【药品】①氯酸钾 ②水 ③过氧化氢 ④二氧化锰⑤高锰酸钾
【装置】

-
(1) 写出A图中a仪器的名称。
-
(2) 小聪同学选择药品①和④制取气体,则他应选用的发生装置是_(填字母序号),该气体的验满方法是。若用该发生装置制取氧气,则应选用的收集装置是(填字母序号)或E。
-
(3) 小亮同学用装置A制取氧气,他选择了E做收集装置,则气体应从(填“b”或“c”)端通入。
 B . 干燥氧气
B . 干燥氧气 C . 收集氧气
C . 收集氧气 D . 检验氧气
D . 检验氧气

-
(1) 指出下列编号仪器的名称:a、b.
-
(2) 实验室加热氯酸钾和二氧化锰的混合物制取氧气的化学方程式为.
-
(3) 实验室制取二氧化碳时可选用的发生装置是.
-
(4) 氨气(NH3)是一种无色、有刺激性气味,密度比空气小,极易溶于水的气体,若选用F装置收集氨气,应将氨气从(选填“c”或“d”)通入.
-
(5) 同学们在课外活动中设计了实验装置G.G装置若用于制备氧气,在分液漏斗中盛放的药品是.
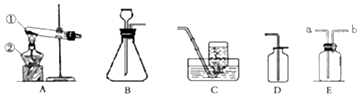
-
(1) 写出图中有标号仪器的名称:①;②.
-
(2) 用双氧水和二氧化锰来制取氧气时,可选用的发生装置是(填序号),二氧化锰的作用为,若用装置E收集氧气,气体由端进入,若将装置中充满水,用排水法收集氧气,气体由端进入.
-
(3) 若用A来制取氧气时,选择合适的药品,其化学方程式为.
-
(4) B装置还可以用来制取气体,化学方程式为.

-
(1) 上图B图中用于添加液体药品的仪器名称是;如果用高锰酸钾制取氧气,应选用的发生装置是,为了保证该实验的顺利进行发生装置中还应.
-
(2) 实验室制取二氧化碳的化学反应方程式是;
B、C装置都可以作为制取二氧化碳的发生装置,与B装置相比,C装置(多孔隔板用来放置块状固体)的优点是.
-
(3) 实验室常用甲酸(液态)和浓硫酸混合加热制取CO,如果用A装置作为气体发生装置,应对A装置作怎样的改进.

-
(1) 指出装置中的至少两处错误:①②
-
(2) 若将氯酸钾和二氧化锰 换成高锰酸钾来制取氧气,并将此装置按正确的方法组装后,还需添加一步操作才能加热制取氧气,这步操作是:.
-
(3) 由于氧气密度比空气大,所以可用收集;由于氧气,所以可用排水法收集.用排水法收集时,当时才可开始收集.集满氧气的集气瓶应(填“正立”或“倒立”)在桌上.
-
(4) 某学生在加热氯酸 钾和二氧化锰制氧气时,错把高锰酸钾当成二氧化锰装入试管中,①是否有氧气迅速放出?②为什么?①;②.
-
(5) 实验室用高锰酸钾制取氧气,实验结束后,发现水槽内的水变成了紫红色,原因可能是.做该实验试管口略向下倾斜的原因是.


-
(1) 写出仪器名称:Ⅰ.;Ⅱ.。
-
(2) 实验室可用二氧化锰与过氧化氢制取氧气。若要较好地控制产生氧气的速度,应选用装置 (填编号)。
-
(3) 用D装置收集氧气,操作的正确顺序为 (填编号)。
a.当出现连续、均匀的气泡时,将导管伸入集气瓶口,气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面正放
若用E装置进行排空气法收集氧气,气体应从 (填“a”或“b”)端通入。
若E装置的瓶中装满水,用排水法收集氧气,氧气应从 (“a”或“b”)端通入。
方法一:H2O2  H2O+O2
H2O+O2
方法二:KMnO4  K2MnO4+MnO2+O2
K2MnO4+MnO2+O2
-
(1) 两种方法涉及的化学反应都是反应。
-
(2) 如图是实验室制取、干燥和收集气体的装置图。仪器A的名称是,现用方法一制取一瓶干燥的氧气,请按气体流向,用导管的编号将装置连接好。(浓硫酸具有吸水性,可作干燥剂)


【提出问题】水是如何减缓该反应速度的呢?
【建立假设】水可以降低H2O2溶液浓度,从而减缓反应速度
【实验方案】他利用如图装置,在相同条件下,分别用30毫升的1%、3%和7%的H2O2溶液进行实验, 观察并比较。
【实验结论】加水降低了H2O2溶液的浓度, 使反应速度变慢。
【交流反思】
-
(1) 为了更好地比较反应的快慢,需控制三次实验中滴加H2O2溶液的相同。
-
(2) 判断产生氧气的速度时,可以通过观察产生气泡的快慢,还可以比较。
-
(3) 【继续探究】针对提出的问题,他又利用如图装置,用3%的H2O2溶液分别在0℃、20℃和60℃的条件下进行实验。进行该实验所基于的假设是。

-
(1) 实验室用高锰酸钾制氧气的文字表达式是,应选择的收集装置是(填字母),如果选用如图2装置收集氧气,气体应从(填“a”或“b”)端导入。
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气的文字表达式为。某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气。实验中,同学们发现不能得到平稳的氧气气流,大家提出从两个方面加以改进:
一是把发生装置由B改为C,其理由是;
二是将过氧化氢溶液加水稀释,溶液的稀释需要经过计算、量取、搅匀三个步骤。
如果把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,需加水的质量为g;在稀释过程中,除了烧杯外,还需要用到的仪器有(填序号)。
①量筒②药匙③试管 ④酒精灯⑤滴管⑥玻璃棒

①装置气密性的检查。②在B塑料瓶中加入两片平菇,在A塑料瓶中加入17 mL质量分数为5%的过氧化氢溶液,然后依次打开弹簧夹K2、K1。过氧化氢溶液进入B塑料瓶与平菇接触,立即产生大量气体。③使用气体收集装置进行氧气收集,每隔5 s记录一次,根据数据绘制出如图乙曲线。回答下列问题:
-
(1) 容器B中所发生反应的化学方程式是。约15s后产生的气体量不再增加,原因是。
-
(2) 若用排水法收集氧气,则下列3种操作中,合理的是 (填字母,下同)。
 A . A B . B C . C
A . A B . B C . C -
(3) 若将步骤②中B瓶中的平菇数量改成三片,其余条件与操作均相同,得到的曲线图与之前的实验对比,下列图中符合事实的是 。
 A . A B . B C . C D . D
A . A B . B C . C D . D

-
(1) 根据发生装置,制取氧气的药品可选 ;A . 高锰酸钾 B . 氯酸钾和二氧化锰 C . 双氧水和二氧化锰
-
(2) 用图示方法收集氧气是因为氧气具有性质;
-
(3) 小红同学先收集一瓶气体,检验它能否使带火星的木条复燃,分析后再依次收集下一瓶气体进行实验。实验结果记录如下表:
实验顺序
第1瓶
第2瓶
第3瓶
第4瓶
第5瓶
第6瓶
氧气含量
60%
40%
30%
50%
35%
32.5%
带火星的木条
复燃
复燃
不复燃
复燃
复燃
不复燃
【交流评价】小明认为实验中有一瓶氧气无需收集进行实验,请指出是哪一瓶并说明理由。
【实验结论】继续实验,最终得出使带火星木条复燃的氧气含量的最小值约为33%。



