水的净化 知识点题库
(1)水是常见的溶剂,将下列生活中少量的物质分别放入水中,不能形成溶液的是 .
A、食盐 B、纯碱 C、植物油 D、蔗糖
(2)电解水产生氢气和氧气,证明水是由 组成的.
(3)天然水中含有许多杂质,净化水的方法有:①过滤 ②蒸馏 ③加明矾吸附沉降 ④消毒杀菌 ⑤活性炭层吸附.要把天然水净化成生活用的自来水,将所选用的净化方法按净化过程排序(填序号) .
(4)区别净化后的自来水是硬水还是软水,可用到的物质是 .
-
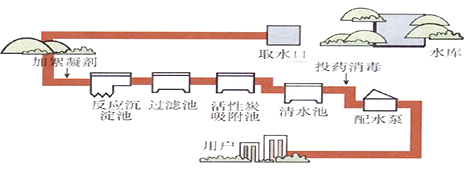
(1) 通入氯气的目的是
-
(2) 自来水作锅炉中用水的危害是:
-
(3) 如何检验自来水是硬水还是软水?.
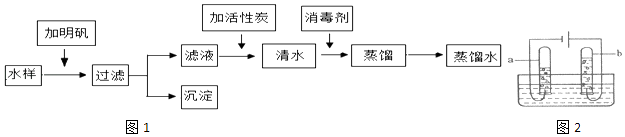
请回答下列问题:
-
(1) 取水后加入明矾的作用是.
-
(2) 向滤液中加入活性炭,利用其性,除去水样中的色素和异味,这是利用了活性炭的性质.为检验此时的清水是否是硬水,可以用检验.
-
(3) 消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化.高铁酸钠中铁元素的化合价为.
-
(4) 如图2是水通电分解的示意图.在实验过程中,试管a中产生的气体是,两气体的体积比为.写出该反应的符号表达式:,这个反应说明水是由组成的.
-
(1) 2017年5月18日,南海可燃冰试采成功,可燃冰主要含有甲烷水合物.甲烷充分燃烧的化学方程式是
-
(2) 渔民常在这一带从事捕鱼作业,鱼肉中含量最多的基本营养素是 (填序号)A . 蛋白质 B . 糖类 C . 油脂 D . 维生素
-
(3) 科学研究证明,水在光照和TiO2作催化剂的条件下,能分解为氢气和氧气,反应的化学方程式是
-
(4) 河水和海水一样都是混合物.自来水厂利用河水生产饮用水的过程中常用活性炭的性来除去水中的色素和异味.检验饮用水是软水还是硬水,可用来检验.
-
(1) 检验某地下水是硬水还是软水,可用的物质是。
-
(2) 为了降低水的硬度,要建议农民在饮用前要将水。
-
(3) 自来水生产过程中,可用方法除去水中不溶性杂质,同时还必须进行消毒。ClO2是一种新型的自来水消毒剂,其中氯元素的化合价为。
-
(4) 保护环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源 的是___(填序号)A . 减少使用化肥农药 B . 工业废水处理达标后排放 C . 使用含磷洗衣粉 D . 生活污水直接排放
-
(1) 自然界中的水都不是纯水,净水时需加入使悬浮物质絮凝沉淀。
-
(2) 欲除云水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是.
-
(3) 生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是。
-
(1) 【作出猜想】联想到所学的化学知识,辰辰猜想可能是氮肥厂排出的废水污染了井水。
他猜想的依据是。
-
(2) 【表达交流】请你根据上述信息帮助辰辰归纳污染物的化学性质:
①;
②。
-
(3) 【设计实验】为了验证猜想,辰辰设计了如下实验方案:
①从氮肥厂取来氮肥作为样品;
②取适量样品放入玻璃杯中,加入井水充分溶解。将所得溶液分为2份;
③一份加入碱性洗衣粉,搅拌后闻气味;另一份加热后闻气味。
【反思评价】辰辰的实验方案存在着问题,你认为应怎样改进?。
【获得结论】辰辰通过改进后的实验,确认是氮肥厂排出的废水污染了井水。
-
(4) 【探究启示】目前该村村民还需饮用井水,请你提出一条简便的处理方法:。
-
(1) 关于水的认识错误的是(填字母序号)_______________。A . 自然界的水是纯净物 B . 自然界的水是取之不尽、用之不竭的 C . 工业废水和生活污水的任意排放会造成水体污染 D . 地球上的总水储量很大,但淡水资源并不充裕
-
(2) 净化水的方法有:①过滤 ②加明矾吸附沉降 ③蒸馏 ④消毒杀菌 ⑤活性炭吸附 其中净化程度最高的方法是(填序号)。要将混有泥沙的天然水净化成生活用的自来水,将所选用的方法按净化过程排序(填序号)。自来水消毒方法有多种,次氯酸钙[Ca(ClO)2]是常用的消毒剂,次氯酸钙中含有的金属元素是(填元素符号)。
-
(3) 下图所示的3个实验:
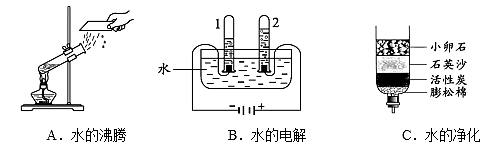
A中水发生了 (填“物理”或“化学”)变化;
B中试管1、2内得到的气体分别为(按顺序用化学式表示);该反应的化学方程式是。教材中设计该实验的主要目的是。要达到该实验目的,可能的实验及推理过程如下:
①氢气和氧气由水产生分解反应而得到 ②水由氢元素和氧元素组成
③氢气由氢元素组成,氧气由氧元素组成 ④化学变化过程中元素的种类不变
⑤组装好装置,接通直流电源,观察到两极产生大量气泡
⑥检验产生的气体知,分别为氢气和氧气 ⑦水分子间有间隔
请将需要的实验及推理过程按顺序完成下列排序(填序号):⑤→⑥→→①→→②。
-
(4) C中净化水的方法有两种,它们分别是 、。某同学用此净水器将浑浊的珠江水进行净化,他所得到的净化水属于(填“混合物”或“纯净物”)。
-
(5) 区分硬水和软水可用;下列方法中可软化硬水的是(填序号)
A.沉淀
B.过滤
C.煮沸
D.吸附
E.蒸馏
-
(1) 自然界中的水都不是纯水,利用沉淀、、吸附和蒸馏等方法可以净化水。
-
(2) 有些村庄打深井取用地下水,可用区分地下水是软水还是硬水,常用的方法来降低水的硬度。
-
(3) 小明同学为了探究水的组成,邀请你一起参加水的电解实验,发现两极上都有气泡冒出,其中正极与负极上的气体体积之比约为1:2,经检验,正极上产生的气体是,负极上产生的气体是。得出水是由两种元素组成的结论。此反应的文字表达式为.
-
(4) “节约用水,从我做起。”请你任举一例生活中节约用水的措施:。
-
(1) 海堤树林茂密,让人清新呼吸。
①树林中的绿色植物通过光合作用,吸收(填化学式),放出O2 , 将能转化为化学能。
②树林中富含抗氧化防衰老的负氧离子。一种负氧离子(O2-)的一个原子团是由一个O2分子俘获了空气中一个自由电子形成的微粒,每个O2-中共含有个电子。
-
(2) 滩涂花海飘香,使人流连忘返。
①鲜花的香味在空气中扩散,是大量的带有香味的分子的结果。
②培育鲜花的某种营养液呈蓝色,可能由KNO3、Ca(NO3)2、CuCl2中的一种或几种物质配制而成,其中Ca、N的元素质量比为1:1,则该营养液中含有种溶质。从均衡植物所需营养元素的角度分析,营养液中还需补充(填元素符号)。
-
(3) 大海资源丰富,引人不断探索。
从海水中可以提取粗盐(含少量泥沙和CaCl2、MgSO4等可溶性杂质)。小明利用如图流程进行除杂,得到精盐。
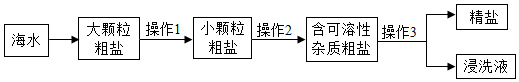
①操作1需要在(填字母序号)中进行。
A.研钵 B.量筒 C.烧杯 D.广口瓶
②操作2的步骤为溶解、过滤、、结晶,过滤操作中玻璃棒的作用是。
③操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的(填“饱和”或“不饱和”)溶液。
④在农业生产上,常用质量分数为16%的NaCl溶液选种。小明称取实验制得的精盐16g,加入盛有84mL蒸馏水的烧杯里(实验条件下,水的密度为1g•mL-1),完全溶解。配制所得的NaCl溶液的浓度低于16%,原因是。
⑤若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:BaCl2溶液、(填化学式)溶液、Na2CO3溶液。允分反应后过滤,加入过量稀盐酸,搅拌、煮沸。
-
(1) 采取操作,可除去污水中的碎菜叶、碎塑料薄膜及泥沙;
-
(2) 用物质,可除去污水的臭味;
-
(3) 把生活污水回收处理,进行在利用的目的是
-
(1) Ⅰ.节約用水
下列图标是我国“国家节水标志”的是(填字母)。

-
(2) Ⅱ.水的净化
天然水净化为自来水的主要流程如下:

“沉降池”中可用明矾作混凝剂,其化学式为KAl(SO4)n·12H2O,n的值为。
-
(3) “吸附池”中常用(填物质名称)吸附色素和异味。
-
(4) “消毒池”中常用液氢作消毒剂,发生了反应:
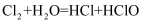 ,若用自来水直接配制硝酸银溶液会产生氯化银白色沉淀。写出盐酸与硝酸银溶液反应的化学方程式:。
,若用自来水直接配制硝酸银溶液会产生氯化银白色沉淀。写出盐酸与硝酸银溶液反应的化学方程式:。
-
(5) Ⅲ.废水处理
废水中氨氮(以NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的NH3 , 发生的反应为:
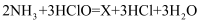 。X的化学式为,若废水碱性过强(pH>10),NH3的去除率会显著降低,原因是。
。X的化学式为,若废水碱性过强(pH>10),NH3的去除率会显著降低,原因是。
-
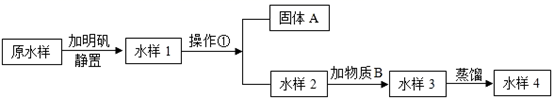
(1) 操作①的名称是,该操作需要用到的玻璃仪器有烧杯、玻璃棒、。如果经过操作①后,所得水样依然浑浊,可能的原因有(答1点)。
-
(2) 为除去水样2中的一些异味和色素,加入的物质B是,利用的是该物质的性质(填“物理”或“化学”)。
-
(3) 这几种净化水的方法程度最高的是,经过此方法出来的水是(填序号)
A 纯净物 B 混合物 C 单质 D 氧化物
-
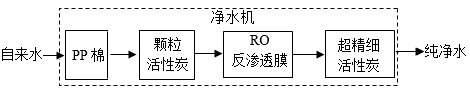
(1) 净水机中,PP棉净水相当于实验室的操作。实验室进行该操作需要用到的玻璃仪器有烧杯、漏斗和,某同学进行该操作后所得滤液仍然浑浊,可能的原因是(写出1点即可)。
-
(2) 该净水机(选填“能”或“不能”)降低自来水的硬度。
-
(3) 颗粒活性炭可去除异味和余氯,是因为活性炭具有良好的性。

-
(1) 如图1所示,过氧化氢溶液在催化剂二氧化锰的作用下,迅速分解放出大量氧气,在此过程中可以观察到的实验现象是产生大量气泡,(写出气球和红墨水的变化)。请写出硫在氧气中燃烧时的现象是,放出热量。
-
(2) 我国水资源丰富,但分布不均,有些村民把地下水作为生活用水,生活中可用的方法降低水的硬度。家用净水器中用除去水中的色素和异味。
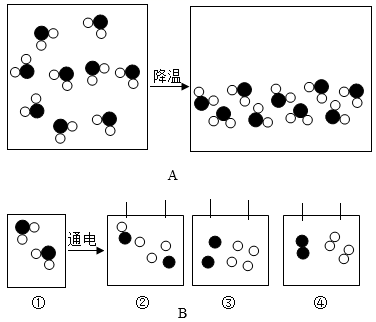
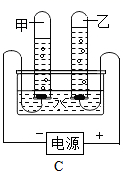
I.如图A、B分别是水蒸气液化,水通电分解的微观变化示意图,C图为电解水实验图:
请回答下列问题:
-
(1) 从微观角度分析可得图A中水分子本身没有改变,只是发生改变,分析图B可知,是化学变化中最小粒子。
-
(2) 图C是小明同学探究水的组成实验,实验结束后试管中产生的气体具有可燃性,若负极产生的气体体积为16mL,则正极产生的气体体积为mL。
-
(3) 该实验发生反应的化学方程式为。
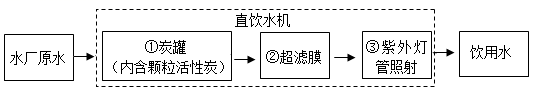
II.净水机可以将水厂原水直接净化为饮用水,其中处理流程如下图所示:
-
(4) 步骤①中固体具有作用,②中超滤膜可起到过滤不溶性杂质的作用,实验室过滤操作需要的玻璃仪器有玻璃棒、烧杯、。其中玻璃棒的作用是。
-
(5) 高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂,K2FeO4中铁元素的化合价是。
-
(1) Ⅰ.节约用水
下列图标是我国“国家节水标志”的是___________(填选项序号)。
A . B .
B .  C .
C .  D .
D . 
-
(2) Ⅱ.水的净化
天然水净化为自来水的主要流程如下:

“沉降池”中可用明矾作絮凝剂,其化学式为KAl(SO4)n·12H2O,n的值为。
-
(3) 漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙(Ca(ClO)2),次氯酸钙可发生如下反应:
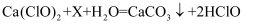 ,则X的化学式为。
,则X的化学式为。
-
(4) 自然界中的水一般要净化后才能使用,在沉降、过滤、吸附、蒸馏等净水方法中,单一操作相对净化程度最高的是。
-
(5) Ⅲ.保护水资源
保护水环境,珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是___________(填选项序号)。
A . 工业废水直接浇灌作物 B . 生活中禁止使用含磷洗衣粉 C . 实验室中的废液集中回收处理 D . 农药、化肥的施用会造成水体污染,应该禁止施用Ⅳ.水的组成
-
(6) 为了探究水的组成,某同学做了水的电解实验,如图所示。

用化学方程式表示其实验原理,实验开始后发现两极都有气泡冒出,试管1中的气体是。电解水实验能够证明水的组成,其结论是。



