还原反应及其应用 知识点
主要应用是冶炼金属
还原反应及其应用 知识点题库
芯片是“智能家电”的核心部件,它是以高纯度单质硅为材料制成的。制取高纯硅的化学方程式为:①SiO2+2C Si(粗)+2CO↑ ②Si(粗)+3HCl
Si(粗)+2CO↑ ②Si(粗)+3HCl SiHCl3+H2 ③SiHCl3+H2
SiHCl3+H2 ③SiHCl3+H2 Si(纯)+3HCl。下列说法错误的是()
Si(纯)+3HCl。下列说法错误的是()
-
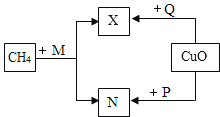
(1) 写出下列物质的化学式
XM
NP
-
(2) CuO与P反应的化学方程式为在该反应中,氧化铜失去氧而变成单质铜,这种含氧化合物里的氧被夺去的反应叫做反应.
 Si+2CO↑中,作还原剂的是( )
Si+2CO↑中,作还原剂的是( )
 2Fe+3CO2 , CO在这个反应中将Fe2O3还原为Fe,在反应中作还原剂.
2Fe+3CO2 , CO在这个反应中将Fe2O3还原为Fe,在反应中作还原剂.(1)请你分析上述反应,还原剂(CO)中元素化合价在化学反应前后的变化情况,归纳出化学反应中还原剂所含元素化合价变化的规律是
(2)请根据你得出的规律,判断反应:Fe+CuCl2=FeCl2+Cu中的还原剂是
久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究.
【提出猜想】根据铜锈的组成元素推测,铜生锈可能是铜与空气中的二氧化碳、水等物质反应的结果.
【实验设计】兴趣小组同学取打磨光量的铜丝,设计了如图所示的四个实验.

-
(1) 【现象分析】若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现.
①实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是.
②B瓶与D瓶中的现象对比,可以得出的结论是.
-
(2) 【实验结论】由上述四个实验可分析得出,铜生锈是铜与空气中的共同作用的结果.
-
(3)
【拓展探究】以锈蚀严重的废铜屑为原料,回收制取纯铜.
查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑
Cu2(OH)2CO3
 2CuO+H2O+CO2↑如图是该兴趣小组设计的两种回收铜的实验方案:
2CuO+H2O+CO2↑如图是该兴趣小组设计的两种回收铜的实验方案: 
【分析评价】①步骤Ⅱ反应过程中发生了还原反应的物质是(填化学式).
②步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是.
③步骤Ⅴ过程发生反应的化学方程式为.
④同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一(填“>”或“=”或“<”)方案二.以上两种方案中,方案二优越于方案一,理由是(任答一点).
元素化合价发生改变的反应都是氧化还原反应.例如:2  + 3
+ 3
![]() 2
2 ,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( )
,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( )
根据化合价是否发生变化分析,下列反应属于氧化还原反应的是( )
 2MgO
B . 2KClO3
2MgO
B . 2KClO3  2KCl+3O2↑
C . CaCO3
2KCl+3O2↑
C . CaCO3  CaO+CO2↑
D . H2+CuO
CaO+CO2↑
D . H2+CuO  Cu+H2O
E . CuO+2HCl═CuCl2+H2O
F . NaOH+HCl═NaCl+H2O
Cu+H2O
E . CuO+2HCl═CuCl2+H2O
F . NaOH+HCl═NaCl+H2O
 2CO
B . 2HClO═2HCl+O2↑
C . C+H2O
2CO
B . 2HClO═2HCl+O2↑
C . C+H2O  CO+H2
D . Al2O3+6HCl═2AlCl3+3H2O
CO+H2
D . Al2O3+6HCl═2AlCl3+3H2O
 Fe3O4+4H2中的还原剂是( )
Fe3O4+4H2中的还原剂是( )
 2Cu+CO2↑反应中,还原剂是( )
2Cu+CO2↑反应中,还原剂是( )
-
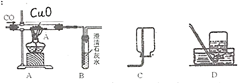
(1) 为避免一氧化碳污染空气并回收利用一氧化碳,B装置应连接C、D哪个装置?
-
(2) 实验进行一段时间后,玻璃管A中出现的现象有什么?写出该反应化学方程式
-
(3) 在这个反应里,如何体现还原反应的概念?请说明

-
(1) 二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得。用合成气制二甲醚时,还产生了一种可参与大气循环的、常温下为液态的氧化物,写出该反应的化学方程式:。
-
(2) 合成气在冶炼铁的生产过程中所起的作用是。
 气体中燃烧:
气体中燃烧:  ,该反应中的还原剂是( )
,该反应中的还原剂是( )
 B .
B .  C .
C . 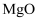 D . C
D . C
 CO+H2 , 在这个反应中,下列分析不正确的是( )
CO+H2 , 在这个反应中,下列分析不正确的是( )
-
(1) 化学反应中有些反应没有明显现象,需要设计实验证明化学反应是否发生。将下列实验中的A与(填“B”或“C”)归为一类,理由是:。


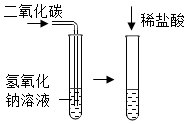
A
B
C
-
(2) 凡是有元素化合价升降的化学反应都是氧化还原反应。元素化合价升高为还原剂,元素化合价降低的为氧化剂。下列反应中,氧化反应与还原反应在同一元素中进行的是。
A

B

C
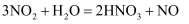
-
(1) 认识文物:青铜是铜与锡的合金。青铜硬度(填“大于”或“小于”)钝铜。
-
(2) 文物锈蚀:汉代铁剪锈透斑斑(如图所示),其锈蚀是铁与空气中的发生化学反应的结果。

-
(3) 文物修复:含六偏磷酸钠【化学式为(NaPO3)6】的敷贴可使青铜器表面附着的土壤硬结物软化清除,该物质中磷元素的化合价为。去除文物上铁锈的步骤之一是将铁锈的主要成分(Fe2O3)用氢气在一定温度下还原成氧化亚铁,该反应的化学方程式为。
-
(1) 饺子是中国的传统美食之一,制作饺子的原料有小麦粉,小麦物中富含的营养素是,馅料中常添加铁强化酱油,铁元素属于人体所需的(填“常量”或“微量”)元素。
-
(2) 久置的铁锅出现锈蚀是铁与空气中的发生化学反应所致。
-
(3) 使用硬水会给生活和生产带来许多麻烦,生活中常用的方法降低水的硬度。
-
(4) 我国古代将炉甘石、赤铜和木炭粉混合加热到800℃,得到一种外观似金子的铜和锌的合金,其中涉及到的化学反应之一是:
 , 该反应中化合价升高的元素是,发生还原反应的物质是(填化学式)。
, 该反应中化合价升高的元素是,发生还原反应的物质是(填化学式)。



