固体溶解度的概念 知识点
固体溶解度的概念
固体的溶解度的定义是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,用字母s表示,其单位是"g/100g溶剂",例如"g/100g水"。
注意事项:固体溶解度有四要素:1、条件:一定温度;
2、标准:100g溶剂;
3、状态:达到饱和;
4、质量:单位。
固体的溶解度的定义是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,用字母s表示,其单位是"g/100g溶剂",例如"g/100g水"。
注意事项:固体溶解度有四要素:1、条件:一定温度;
2、标准:100g溶剂;
3、状态:达到饱和;
4、质量:单位。
固体溶解度的概念 知识点题库
20℃时,向甲烧杯中加入25g水和25g固体固体A,向乙烧杯中加入25g水和25g固体B(A、B两种物质均不与水反应).充分搅拌后,甲烧杯中固体剩余,乙烧杯中固体全部溶解.请回答下列问题:
-
(1) 20℃时,甲烧杯中溶液(填“一定”或“不一定”,下同) 是饱和溶液;乙烧杯中溶液(填“一定”或“不一定”,下同)是饱和溶液.
-
(2) 20℃时,A的溶解度(填“大于”、“小于”或“等于”)B的溶解度.
-
(3) 20℃时,为判断乙烧杯中溶液是否饱和,除采用实验的方法外,还可以利用题中已有数据和来判断.
一定质量分数的硝酸钾溶液可用做无土栽培的营养液.请通过计算回答:
(1)硝酸钾中钾元素、氮元素、氧元素的质量比是 .
(2)某蔬菜基地欲配制500kg溶质质量分数为8%的硝酸钾溶液,需要硝酸钾 kg,水 kg.
(3)已知在150C时硝酸钾的溶解度为25g,则该温度下硝酸钾的饱和溶液中溶质质量与溶液质量的最简整数比为 .
如图是A,B,C三种物质的溶解度曲线.请回答:

-
(1) t1℃时,A,B,C三种物质的溶解度由大到小的顺序是;
-
(2) t2℃时,A,C饱和溶液的相等;
-
(3) t2℃时,A,B,C三中溶质的饱和溶液,如果由t2℃降温到t1℃,溶液变为不饱和溶液的是;
-
(4) 从溶液中获得A溶质的宜采用的方法是;
-
(5) t2℃时,C的饱和溶液中溶剂和溶液的质量比为.
t℃时,向一支盛有0.15g熟石灰的烧杯中加入50g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体.下列相关叙述正确的是( )
A . 升高温度上层清液变为不饱和溶液
B . t℃时,熟石灰的溶解度为0.3g
C . 烧杯中溶液的质量小于50.15g
D . 上层清液中溶质质量分数大于0.3%
固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线 如图所示.下列说法错误的是( )

A . 物质W能溶解在水和乙醇中
B . t1℃时,物质w在水中的溶解度为mg
C . t2℃时,物质W在水中与在乙醇中的溶解度相同
D . t1℃时物质w的饱和水溶液升温至t2℃有晶体析出
水是重要的溶剂。下列有关水和溶液的说法正确的是( )
A . 凡是均一、稳定的液体都属于溶液
B . 通过沉淀、过滤、吸附、灭菌等净化后,水的硬度能有效降低
C . 要把接近饱和的石灰水溶液变为饱和溶液可蒸发水分或降低温度
D . 氯化钾在20℃时的溶解度为34g,那么20℃时50g水中最多能溶解17gKCl
如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是…( )

A . t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲
B . t2℃时,20g丙能溶解于50g水中形成70g溶液
C . 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D . t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲=丙
根据下表数据,回答问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 25.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
-
(1) 20℃时,将136g饱和NaCl溶液蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为;
-
(2) KNO3溶液中含有少量NaCl,要提纯KNO3 , 采用的方法是(填“蒸发结晶”或“降温结晶”);
-
(3) 若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是_________(填序号)。A . 0~20℃ B . 20~40℃ C . 40~60℃ D . 60~80℃
有关溶质质量分数叙述正确的是( )
A . 某盐酸中氯化氢含量为36%是指100克水中含氯化氢36克
B . 往某溶液中加固体,则溶质质量分数一定变大
C . 一定温度下,饱和溶液的溶质质量分数是定值
D . 溶质的质量分数越大,溶液中的溶质含量越大
20℃时,将等质量的甲、乙两种不与水反应的固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.则下列说法中错误的是()

A . 图1中乙的溶液可能是不饱和溶液
B . 图2中两溶液溶质质量分数一定相等
C . 图3中 M表示的是甲的溶解度曲线
D . 图2中两溶液降温至30℃都会析出晶体
亚硝酸钠(NaNO2)是一种工业用盐,有毒、有咸味,外形与食盐相似。下图是NaNO2、NaCl 的溶解度曲线。请回答下列问题:


-
(1) 根据溶解度曲线,某同学设计了鉴别 NaNO2、NaCl 固体的方案,如上图:
①由此可以判断甲是(填化学式);
②m的取值范围为。
-
(2) 现有一杯125.0g溶质质量分数为20%的NaNO2溶液,若维持温度在20℃,要使该溶液变为饱和溶液,需要加入NaNO2固体g。
-
(3) 根据溶解度曲线,关于NaNO2和NaCl下列说法中正确的是____。A . 20℃时,等质量的两种固体加水配成饱和溶液,所得NaCl溶液的质量大 B . 40℃时,NaNO2溶液的溶质质量分数大于NaCl溶液的溶质质量分数 C . 60℃时,两种物质的饱和溶液降温到 20℃时,NaNO2的溶液中析出晶体较多 D . 除去NaNO2固体中混有的少量NaCl,可以采用降温结晶的方法
如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是()

A . t1℃时,甲、乙两物质的溶解度大小关系:甲>乙
B . t2℃时,等质量的甲、乙溶液中,溶剂的质量一定相等
C . t3℃时,若将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D . 将t1℃时甲、乙的饱和溶液升温至t2℃,所得甲、乙的溶液仍都是饱和溶液
图3是X、Y两种固体物质的溶解度曲线。下列说法中正确的是( )

A . t1℃时X的溶解度大于Y的溶解度
B . t2℃时X的溶解度等于Y的溶解度
C . t3℃时X的饱和溶液降温至t2℃时,变为不饱和溶液
D . t1℃时Y的不饱和溶液升温至t2℃时,变为饱和溶液
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
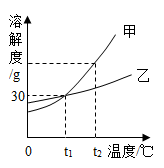
A . 甲物质的溶解度大于乙物质的溶解度
B . 两种物质的溶解度都随着温度的升高而增大
C . t1℃时,60g甲加入到100g水中,充分溶解,得到160g溶液
D . 甲、乙的饱和溶液从t2℃降温到t1℃,析出晶体的质量:甲一定小于乙
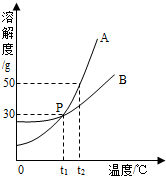
如图是A、B两种固体物质的溶解度曲线。据图回答:
-
(1) P点表示的意义是在t1℃时,A,B两物质的溶解度。(填“相等”或“不相等”)
-
(2) t2℃时A,B两物质溶解度大小顺序是。
-
(3) 把t2℃时等质量A,B两物质的饱和溶液降低到t1℃,析出晶体较多的是。
-
(4) 当A中含有少量B物质时,可采用(填“降温”或“蒸发”)结晶的方法提纯A物质。
20℃时KCl的溶解度是34g/100g水,按如图所示进行操作(整个过程中无溶剂损失)。以下说法正确的是( )
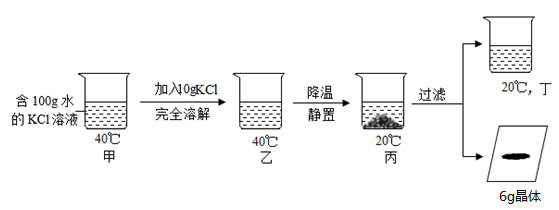
A . 甲和丙都是KCl的饱和溶液
B . 丁中溶液的溶质质量分数为34%
C . 溶液中溶质质量大小的关系是:甲>丙=丁
D . 若乙溶液恰好饱和,则40℃时KCl的溶解度为40g/100g水
如图是A、B、C三种固体物质的溶解度曲线图。请结合图示回答下列问题:

-
(1) t2℃ 时,A,B,C三种物质的溶解度由大到小的关系是。
-
(2) 将A的不饱和溶液转变成饱和溶液的方法是(写一种)。
-
(3) A中含有少量B,分离得到较纯的A的步骤是溶解、、过滤、洗涤、干燥。
-
(4) t3℃ 时,将30 g A物质加入到50 g水中,充分溶解后,所得溶液中溶质的质量分数是。
-
(5) 将t1℃ 时A和C的饱和溶液同时升高一定温度后,所得溶液中溶质的质量分数的大小关系是。
T℃时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:

-
(1) 该温度下,甲、乙、丙三种固体溶解度由大到小的顺序是。
-
(2) 乙溶液在B点属于溶液(填“饱和”或“不饱和”);
-
(3) 将甲的不饱和溶液变为饱和溶液,可用方法是。
-
(4) 该温度下,甲的溶解度为:。
-
(5) 已知乙的溶解度受温度影响较小,丙的溶解度受温度影响较大,当丙中混有少量乙,提纯方法是。
T1℃时,将等质量的KNO3、KCl分别加入到各盛有100.0g水的两个烧杯中,充分搅拌后恢复到T1℃,现象如图1、2所示。下列说法正确的是( )
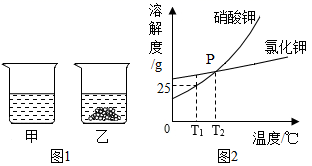
A . 甲中加入的固体是KNO3
B . 甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液
C . 将甲、乙中的物质混合,充分搅拌,一定有固体剩余
D . 若将甲、乙的温度从T1℃升高到T2℃,两溶液中的溶质质量分数不一定相等
溶液在生命活动和生产、生活中起着十分重要的作用。
-
(1) 把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是_____(填序号)。A . 泥土 B . 面粉 C . 蔗糖 D . 香油
-
(2) 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据图回答下列问题。

①t2℃时,a、b、c三种物质的溶解度由大到小的顺序是。
②t1℃时,将25ga物质加入到100g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是(最简整数比)。
③t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是(填序号)。
A.都是饱和溶液
B.析出晶体质量最多的是b
C.溶质质量分数大小关系是:b>a>c
-
(3) 某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为g。
②该同学按下列实验步骤进行:
①计算②称量③量取④(填步骤名称)。
③将50g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水的质量为g。
最近更新



