固体溶解度的概念 知识点题库


-
(1) ℃时,物质A和C的溶解度相等;
-
(2) 等质量的A,B,C三种物质的饱和溶液分别从t2℃降温到t1℃时,溶液质量没有发生改变的是.
-
(3) t2℃时,A物质饱和溶液的溶质质量分数是;(100+b)gA的饱和溶液从t2℃降温至t1℃,溶液的质量为g.

-
(1) 10℃时,10g甲加入50g水中得到溶液(填“饱和”或“不饱和”).
-
(2) 30℃时,等质量的甲乙配成饱和溶液所需水质量大的是(填“甲”或“乙”).
-
(3) 欲从甲、乙混合物中分离出甲物质,可以采用的方法,理由是.
-
(1) 自然界中的水含有许多可溶性和不溶性杂质。长期饮用硬水可能会引起体内结石,生活中常用的方法来降低水的硬度。
-
(2) 氢气被认为是理想的清洁燃料,其燃烧的化学反应方程式为,水是常用的溶剂,配置下列溶液时,可用水做溶剂的是(填序号)。
A.生理盐水 B.医用碘酒
C.高锰酸钾溶液 D.植物油
-
(3) 如图是甲、乙两种固体物质的溶解度曲线。80℃时,请比较等质量的甲、乙两种饱和溶液中所含溶剂的质量甲乙(填“>”、“<”或“=”)。

-
(4) 将40℃时甲与乙的饱和溶液分别升温到80℃时,可析出晶体的是。(填“甲”或“乙”)

| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度/g | 1.68 | 3.73 | 7.3 | 13.4 |



| 温度(℃) | 10 | 20 | 30 | 40 | |
| 溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | |
-
(1) 生活中可用区分硬水和软水。
-
(2) 净水时,利用活性炭的性除去水中的色素和异味。
-
(3) 下花是氯化钠和硝酸钾在不同温度的溶解度请回答。
温度/℃
10
20
30
40
50
60
溶解度/g
NaCl
35.8
36.0
36.3
36.6
37.0
37.3
KNO3
20.9
31.6
45.8
63.9
85.5
110
①根据上表数据分析NaCl与KNO3的溶解度相等的温度在(填字母 )之间。
A.10℃﹣20℃ B.20℃﹣30℃ C.30℃﹣40℃
②若NaCl中混有少量的KNO3 , 提纯NaCl的方法是。
③某同学取NaCl、KNO3中的一种物质,按如图所示进行实验。
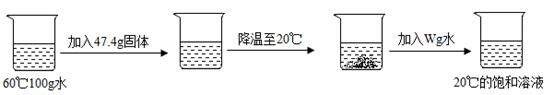
该同学所取的固体物质为,W的值为g。

-
(1) t1℃时,甲物质的溶解度为。
-
(2) 乙中含有少量甲,提纯乙的方法是。
-
(3) 将等质量的乙、丙两种物质分别配成t1℃时的饱和溶液,所需溶剂的质量较少的是。
-
(4) t2℃时,等质量甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液质量的关系是。

-
(1) 过滤时,漏斗中液面必须
-
(2) 蒸发时,用玻璃棒不断搅拌,当时停止加热;实验结束后,用(填仪器名称)将蒸发皿从铁架台取下。
-
(3) 某实验小组粗盐提纯结束后称量精盐,操作如右图所示。

已知室温下NaCl溶解度为36g,请计算:若要将所得精盐全部溶解(杂质忽略不计),至少需要量取mL水。

表:两种物质在不同温度时的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
-
(1) KNO3对应的是图中的物质。
-
(2) 25℃时,向100g水中加入45.8gKNO3 , 充分搅拌后,所得的溶液是溶液(填“饱和”或“不饱和”)。
-
(3) 当甲中含有少量乙时,应采用结晶法提纯甲。


-
(1) 30℃时,100g水中最多溶解g氢氧化钙;
-
(2) 氢氧化钙的溶解度随温度变化的特征是。
-
(3) 在不改变溶质质量分数的情况下,把接近饱和的氢氧化钙溶液变成饱和溶液的方法是。
下表是碳酸钠的部分溶解度数据
|
温度/℃ |
20 |
30 |
40 |
50 |
60 |
80 |
100 |
|
溶解度/g |
21.8 |
39.7 |
48.8 |
47.3 |
46.4 |
45.1 |
44.7 |
-
(1) 由表中数据可知,碳酸钠属于物质(填“易溶”“可溶”“微溶”或“难溶”)。
-
(2) 由表中数据可知,碳酸钠的溶解度随温度升高。
-
(3) 小东同学进行了如下图所示的实验,若使烧杯③中的溶液达到饱和,至少需再加入g碳酸钠;升温至60℃时,烧杯④中会出现的现象是。

-
(4) 20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是(填字母序号),该物质形成的溶液中存在的微粒有。
A.氢氧化钠 B.碳酸钙 C.硝酸铵 D.氯化钠
温度/℃ | 10 | 20 | 60 | 100 | |
溶解度/g | 硝酸钾 | 20.9 | 31.6 | 110 | 246 |
氯化钠 | 35.8 | 36.0 | 37.3 | 39.8 | |
氢氧化钙 | 0.17 | 0.16 | 0.11 | 0.074 | |
资料二同一硝酸钾溶液随温度变化的情况如下图甲所示。

请回答以下问题:
-
(1) 硝酸钾中含有少量氯化钠,提纯硝酸钾的方法是。
-
(2) 图甲中当温度为90℃时,该溶液一定是(填“饱和溶液”或“不饱和溶液”)。
-
(3) 图甲的硝酸钾溶液随温度变化过程中,纵坐标y的量一定不符合如图乙变化情况的是。(不考虑水分的蒸发)
选项
温度变化
纵坐标y的量
A
10 ℃升温到30 ℃
溶剂的质量
B
10 ℃升温到70 ℃
溶质的质量
C
10 ℃升温到70 ℃
溶液的质量
D
10 ℃升温到90 ℃
溶质质量分数
-
(4) 如图丙所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入氢氧化钠后,烧杯A中变浑浊。其原因是。




