酸、碱性废水的处理 知识点
酸、碱性废水的处理 知识点题库
-
(1) “低碳”生活从我做起,所谓“低碳”指什么?
-
(2) 燃放烟花炮竹时,除了会带来噪音污染外,还会带来 等环境问题.
-
(3) 为了我们的青山绿水,请你用学过的知识回答和解决问题,我市锰矿资源丰富,某电解金属锰厂排放的废水中含有硫酸等物质,从经济和可行方面考虑,你认为最好选择什么物质处理该废水中的硫酸?
济宁是山东省重要的煤炭能源基地,矿区废水中Fe2+、Cu2+、Zn2+等严重影响着当地水质,某污水处理厂采用下面工艺(见图)净化这种酸性废水并回收Fe2+、Cu2+、Zn2+三种离子,请读识流程图并回答:

(1)矿区废水经氧化池后在进入沉淀池Ⅰ,目的是 ;
(2)利用氢氧化钠调节沉淀池Ⅰ、沉淀池Ⅱ和沉淀池Ⅲ的pH,目的是;
(3)出水前,中和池中加入硫酸的作用;
(4)若矿区废水中主要含有硫酸盐,请写出沉淀池Ⅲ中发生反应的化学方程式: .
-
(1) 一些同学想将三种溶液一次性鉴别出来.经讨论确定如下四种方案:
①取样,分别滴加石蕊溶液;②取样,分别通入CO2;
③取样,分别测三种溶液的pH;④取样,分别滴加碳酸钠溶液.
你认为以上方案合理的有哪几项?(填选项序号).
-
(2) 另一些同学认为只用酚酞试液也可以以将三种溶液鉴别出来.同学们设计并顺利完成了实验.请你帮他们把实验报告补充完整.
实验步骤
实验现象
结论
步骤1:各取溶液少许于三只试管中,分别滴加几滴酚酞试液,振荡
一支试管中溶液变红,另两支试管中无现象
溶液变红的试管中原溶液是
步骤2:将变红的溶液分成两等份于两只试管中,分别滴加适量的另外两种溶液,振荡滴加的溶液是
滴加的溶液是
滴加的溶液是
-
(3) 实验结束后,同学们将废液倒入废液缸中,经测定废液呈酸性,此废液不可以直接倒入下水道.其原因是(写一条即可).
-
(1) 小艳取少量废水于试管中,向其中加入氢氧化钠溶液,直至生成蓝色沉淀,写出生成蓝色沉淀的化学方程式:.
-
(2)
如图是小艳记录的该工厂处理利用废水的简要流程:
操作Ⅰ的名称是,溶液B中的溶质是.
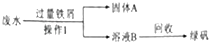
物质 | CaO | CaCO3 | Ca(OH)2 | NaOH |
市场参考价(元/kg ) | 3.5 | 2.5 | 2.8 | 11.5 |
请你从节约资金的角度考虑,处理相同的废水应选择( )
-
(1) 回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的污染.秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为(用最简整数比表示).
-
(2) 造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放.
①检测废水呈碱性的简单方法是 .
②若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可以处理的废水质量是多少?
实验操作 | 实验现象 | 结论 | |
方法一 | 取少量河水样品于试管中,滴加2﹣3滴酚酞溶液 | 若溶液. | 说明河水已被碱性溶液污染 |
方法二 | 在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取河水样品滴到p H试纸上,与校准比色卡比较 | 若读出溶液 pH7 |
你的治理措施是.
第一步:验证废水酸性.往废水中滴加石蕊试液,石蕊变,说明废水呈酸性.
第二步:处理废水.该小组同学设计了以下两个方案.
方案一:用熟石灰处理废水,其反应的化学方程式为.
方案二:用BaCl2处理废水,观察到废水中出现.
经过分析,同学们认为方案二没有达到处理废水的目的,因为处理后的废水中含有较多的.
-
(1) 甲、乙、丙三厂排出的废水中依次含有的废弃物是.
-
(2) 乙、丙两处发生的反应的化学方程式为.



