酸的化学性质 知识点
(2)与活泼金属反应生成盐和氢气
(3)与金属氧化物反应生成盐和水
(4)与碱反应生成盐和水
(5)与盐反应生成新盐和新酸
酸的化学性质 知识点题库
a.盐酸 b.氯化钠 c.熟石灰 d.钛合金
①家庭生活中常用的一种调味品是 ;
②可用来制造人造骨是 ;
③可用于清除金属制品表面锈斑的是 .
-
(1) 打开浓盐酸的试剂瓶,观察到瓶口有,这是因为浓盐酸有性.
-
(2) 根据如图写出反应的化学方程式.

-
(3) 胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式.
-
(1) “洁厕灵”、“漂白精”是家庭常用的两种清洁剂.“洁厕灵”的有效成分是盐酸,可清除污垢,但不能用于清洁大理石制品,理由是(写化学方程式);“漂白精”的有效成分是次氯酸钠(NaClO),能快速漂除衣服污渍.但“洁厕灵”与“漂白精”不能混用,二者若混合易产生一种有毒气体,化学方程式为NaClO+2HCl=NaCl+X+H2O,则X的化学式为
-
(2) 波尔多液是一种农业上的杀菌剂,它由石灰乳与硫酸铜等配置而成.请用化学方程式解释不能用铁制容器来配制波尔多液的原因是,基本反应类型是反应.
-
(1) 氧气、水、二氧化碳、生石灰、小苏打在组成上的共同特点是;
-
(2) 如图是四种粒子的结构示意图,其中与③化学性质相似的是(填序号):
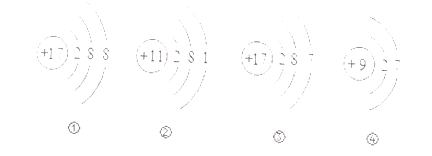
-
(3) 已知同温同压下,气体的体积比等于分子数目比,若空气中其它成分忽略不计,用○表示氮原子,●表示氧原子,图中可粗略表示空气组成的是(填标号):
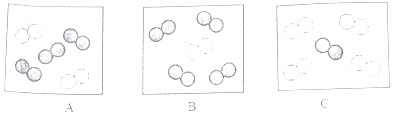
-
(4) 稀盐酸能与某些金属氧化物反应,因此可用于铁制品表面除锈,请写出相关的化学方程式:.
 向一定质量的饱和石灰水中不断加入生石灰
B .
向一定质量的饱和石灰水中不断加入生石灰
B . 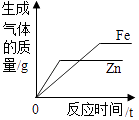 向等质量的锌和铁中滴加足量的质量分数相等的稀盐酸
C .
向等质量的锌和铁中滴加足量的质量分数相等的稀盐酸
C .  用等质量等浓度的过氧化氢溶液在有无催化剂条件下制取氧气
D .
用等质量等浓度的过氧化氢溶液在有无催化剂条件下制取氧气
D . 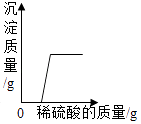 向一定质量的氢氧化钾和硝酸钡的混合溶液中滴加稀硫酸
向一定质量的氢氧化钾和硝酸钡的混合溶液中滴加稀硫酸
-
(1) 在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有产生,反应的化学方程式是。
-
(2) [发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。

[得出结论]镁条与盐酸反应产生白色沉淀与有关。
-
(3) [查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是(用化学方程式表示)。
-
(4) [实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管
操作
现象
结论
A
加入足量盐酸
,白色沉淀
猜想一错误,但这种白色沉淀能溶于盐酸
B
加入足量水
白色沉淀
猜想二错误
C
加入适量稀硝酸
白色沉淀消失
原白色沉淀中含有的离子是:Mg2+、
继续滴加几滴硝酸银溶液
出现大量白色沉淀
 B . 在Na0H溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸
B . 在Na0H溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸  C . 在Na0H溶液中加入CuO,然后向其中逐滴加入稀硫酸
C . 在Na0H溶液中加入CuO,然后向其中逐滴加入稀硫酸  D . 在NaOH 溶液中加入Ba(NO3)2 , 然后向其中逐滴加入稀硫酸
D . 在NaOH 溶液中加入Ba(NO3)2 , 然后向其中逐滴加入稀硫酸 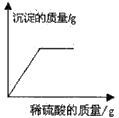
-
(1) 【提出问题】溶液中溶质的成分是什么?
【做出猜想】①只有Na2SO4;
②Na2SO4和两种物质;
③Na2SO4和NaOH两种物质.
-
(2) 【实验验证】
实验操作
实验现象
实验结论
甲同学实验
取适量中和反应后的溶液滴于试管中,将表面打磨后的铝片放入试管的溶液中
铝片逐渐溶解,并有大量气泡冒出
猜想②成立
乙同学实验
取中和反应后的溶液少许于另一试管中,并滴加几滴无色酚酞试液
溶液变色
猜想③成立
丙同学对甲、乙两同学结论不同产生质疑.
【查阅资料】①Na2SO4溶液显中性;②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为2Al+2NaOH+2═2NaAlO2+3H2↑.
-
(3) 【交流反思】①丙同学肯定猜想①(填“成立”或“不成立”);
②丁同学认为猜想②不成立,其理由是;
③该组同学经过充分讨论,一致认为猜想③成立;
④甲同学的实验是;铝片和溶液反应.
-
(1) (查阅资料)Na2SO4溶液呈中性。
(演示实验)将一定量的稀硫酸加入到盛有无色酚酞和NaOH混合溶液的小烧杯中。当看到(填现象),证明它们确实发生了化学反应。
-
(2) (学生板书)该反应的化学方程式:。
-
(3) (提出问题)该烧杯内溶液中的溶质是什么?
(假设猜想)针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
①只有Na2SO4 ②有Na2SO4和H2SO4 ③有Na2SO4和NaOH ④有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想及理由是。
-
(4) (实验探究)
丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有。
-
(5) 为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
实验方案
测溶液的pH
滴加Na2CO3溶液
滴加BaCl2溶液
实验操作



续表:
实验现象
试纸变色,对比比色卡,pH<7
有气泡产生
产生白色沉淀
实验结论
溶液中有H2SO4
溶液中有H2SO4
溶液中有H2SO4
(得出结论)通过探究,全班同学一致确定猜想二是正确的。
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出(实验探究)(2)中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
①实验操作中的错误是。
②实验方案中也有一个是错误的,错误的原因。
-
(6) (反思与拓展)
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑。
②根据所学化学知识,验证烧杯内溶液中的溶质含有H2SO4 , 除以上正确方案外,下列哪些物质单独使用也能完成该实验?(填序号)。①Cu ②CuO ③紫色石蕊溶液 ④AgNO3溶液
③烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是(写一条)。
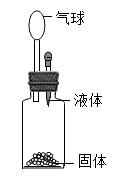
①石灰石和稀盐酸 ②镁和稀硫酸 ③固体氢氧化钠和水 ④生石灰和水

[资料]碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下) (部分)
|
温度/℃ |
0 |
15 |
20 |
30 |
40 |
50 |
60 |
|
碳酸氢钠溶解度/g |
6.9 |
8.72 |
9.6 |
11.1 |
12.7 |
14.45 |
16.4 |
|
碳酸钠溶解度/g |
7.1 |
13.25 |
21.8 |
39.7 |
48.8 |
47.3 |
46.4 |
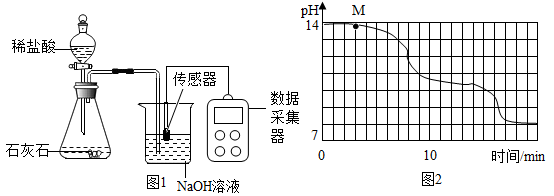
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶于80g水中,而后匀速的通人二氧化碳气体,同时用传感器测定溶液的pH变化如图一所示,并同时用数据采集器记录并绘制图像如图2所示。
[分析与判断]
-
(1) 通过图象分析,小苏打溶液是显(填“酸性”、“中性”或“碱性”),图像中M点处发生的主要化学反应方程式为。
-
(2) 为了确定M处溶液的成分,同学们进行了如下的探究:
[提出猜想]
猜想一:可能是Na2CO3
猜想二:可能是Na2CO3、NaOH
[实验探究]
实验步骤
加入试剂
实验现象
初步实验结论
①
滴入酚酞溶液
猜想二符合题意
②
加入溶液
-
(3) [实验反思]实验过程中,同学们发现18min 后溶液的pH基本不再变化,则此时烧杯中可观察到的现象有。

-
(1) 甲、乙、丙(填“可能”或“不可能”)依次为Mg、NaOH、CO2。
-
(2) 当甲为某种碱时,它与硫酸铜溶液反应能同时生成两种沉淀,则甲的化学式为。
-
(3) 写出硫酸转化为硫酸铜的化学方程式。




