氧气的实验室制法 知识点题库
某中学化学兴趣小组在老师的指导下,实验员提供了如下器材和若干化学药品,进行气体的制备和性质的探究,邀请你一同参加.
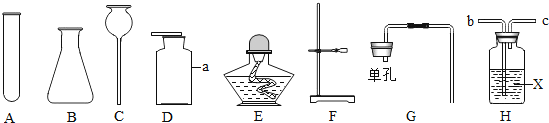
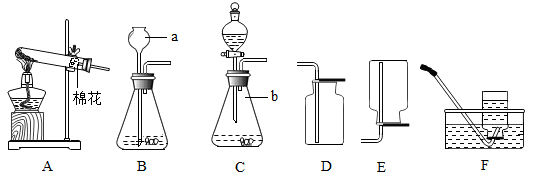
(1)写出图中标号a仪器的主要用途 .
(2)实验室制取少量氢气,且操作相对简易时,发生装置最好选用 (填写字母代号),组装好仪器后,应先 , 再添加药品.
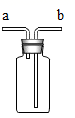
(3)实验室常用过氧化氢溶液制取氧气,该反应的化学方程式是,实验室若要制取干燥的氧气,收集氧气前先将气体通过H装置,H装置中的X是(填“浓盐酸”或“浓硫酸”或“氢氧化钠溶液”),其理由是 , 气体通过H时应从 (填“b”或“c”)端进入.
 B .
B . 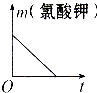 C .
C .  D .
D . 

-
(1) 写出图中标示的仪器名称:①,②.
-
(2) 实验室用KMnO4制取O2 , 应选用的发生装置为(填字母序号,下同),收集装置可选用(写一种即可),取用KMnO4药品时,应选用仪器.写出该反应的文字表达式.
-
(3) 注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至.
②将注射器C连接到装置E的导管口处.
③缓慢拉动注射器C的活塞,观察到,表示装置E的气密性良好.
-
(4) 实验室制备二氧化碳的发生装置应选用如图A~H中的(填序号),所发生反应的文字表达式为
.用图甲所示装置来探究二氧化碳能否与水反应,测试管中的水里应加入的试剂是,所发生反应的文字表达式为.若用图乙装置采用排空气法收集二氧化碳,发生装置应连接导管.(选填“a”、“b”)
-
(1) 同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
实验
30%双氧水的质量(g)
加入水的体积(mL)
二氧化锰质量(g)
收集时间(s)
1
10
40
5
200
2
20
30
5
100
3
30
20
67
①实验时,取用二氧化锰的仪器是(填仪器名称).
②如图所示,发生装置应选用(填编号,下同),此题中气体收集装置应采用的是.

③实验3中,加入的二氧化锰质量为 g.
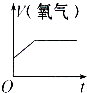
④相同条件下,实验3产生氧气的速率最快,说明.
⑤第三次实验结束后,测得容器中全部剩余物的总质量为50.8g,则该实验生成氧气的质量是 g.
-
(2) 二氧化碳与水反应,在常温下进行的化学方程式为,在叶绿素、光照的条件下发生光合作用生成葡萄糖 (C6H12O6)和氧气的化学方程式为,反应物相同,但产物不同.说明不同,产物不同.


-
(1) 写出图中标号①的仪器名称。实验室用A装置制取氧气,反应物是(填名称)。
-
(2) 写出实验室用B装置制取氧气的化学方程式,该实验若改用装置C制备氧气,其优点是。检验装置C气密性的方法是:关闭弹簧夹后,,则气密性良好。
-
(3) 若用F装置收集CO2 , 气体应从(填“b”或“c”)端通入。
-
(4) 装置G中的气球实验前均已经稍微膨胀;实验前,装置G中分液漏斗的活塞均处于关闭。打开分液漏斗的活塞并轻轻振荡集气瓶,可观察到。

-
(1) 请回答有关问题:
实验步骤
有关问题
①检查气体发生装置的气密性。
检查装置气密性的具体操作及气密性良好的判断依据是。
②向试管中加入少量高锰酸钾粉末,使其平铺于试管底部,按上图所示组装实验装置。在接近试管口的地方放置一小团蓬松的棉花团。
①用药匙或纸槽向试管中加入少量高锰酸钾粉末。
②组装实验装置时,要根据的高度将盛有
药品的试管固定在铁架台上。
③欲调整装置中试管的倾斜角度,应调节图中A、B、C哪个旋钮:旋钮。
④试管口棉花团的作用是。
实验步骤
有关问题
③加热试管,当导管口有连续均匀气泡冒出时,开始收集气体。
①加热试管的方法是。
②发生反应的化学方程式为。
③收集满瓶氧气的操作过程是:等集气瓶中的水排完后,一只手扶稳集气瓶,另一只手首先小心地将导管从瓶口移开,然后,最后把集气瓶正放在桌子上。
④气体收集完毕后,操作B.
操作B是先,再
-
(2) 收集完气体后,测得其纯度明显偏低,其原因可能是 (填字母)。A . 高锰酸钾中混入了二氧化锰 B . 收集前,集气瓶中未注满水 C . 收集后,集气瓶中仍留有水 D . 未见气泡连续均匀冒出时就开始收集
-
(3) 选择排水法收集一瓶氧气,供“铁丝在氧气中燃烧”实验使用的理由是。
-
(4) 加热3.16g高锰酸钾固体一段时间,若高锰酸钾中的氧元素有1/4转化为氧气,则生成的氧气的质量为,剩余固体中氧元素的质量分数为。(精确到0.1%)
-
(5) 林同学称取一定质量高锰酸钾制取一定质量的氧气,将温度控制在250℃加热制O2 , 实验结束时,林同学发现在用高锰酸钾制取氧气的实验中,收集到的O2大于理论产量,针对这一现象,同学们在老师的指导下进行了如下探究:
【提出猜想】依据质量守恒定律,他们做出如下猜想:
猜想Ⅰ:反应生成的MnO2分解放出O2
猜想Ⅱ:反应生成的K2MnO4分解放出O2
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2 , 在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想错误。
②第二组同学取一定质量的K2MnO4在250℃条件下加热,固体质量(填“减轻”或“增重”),得出了猜想Ⅱ正确的结论。
林同学提出:不用测定质量也能验证以上猜想是否正确,林同学选择的实验方法可能是。
-
(6) 【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是K2MnO4分解的生成物K2O对其分解产生影响。为验证此结论,设计如下实验方案:
①分别取K2MnO4固体于两支试管中,一支试管中加入K2O,一支试管中不加K2O。
②加热,用相同规格的集气瓶,用排水法分别收集一瓶气体。③比较所用的时间长短,以确定锰酸钾的分解是否与氧化钾有关系。
该过程中还必须控制相同的变量是 。
-
(1) (猜想)
Ⅰ.氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;
Ⅱ.氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;
Ⅲ.氧化铁是反应的催化剂,反应前后。
-
(2) (实验)用天平称0.2g氧化铁,用试管取5mL 5%的过氧化氢溶液,进行如图实验:
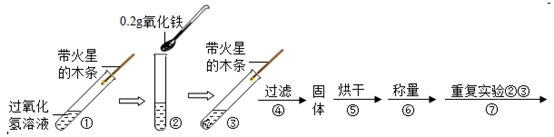
(注:氧化铁不溶于水,过滤可与水分离)
填写如表:
步骤3现象
步骤6结果
步骤7现象
结论
带火星的木条复燃
过氧化氢溶液中,
猜想1、Ⅱ不成立,
猜想Ⅲ成立
-
(3) 步骤①的目的是。
-
(4) 步骤⑦重复实验②、③目的是。
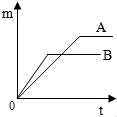 B .
B . 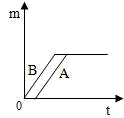 C .
C . 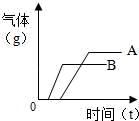 D .
D . 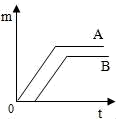
-
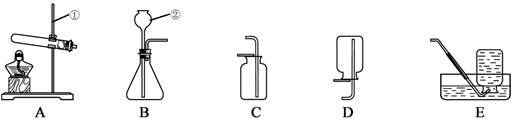
(1) 写出装置图中标号仪器的名称:①,②。
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为,选用的发生装置是(填字母序号)。集满氧气的集气瓶应(填“正”或“倒”)放在桌面上。
-
(3) 写出实验室制取二氧化碳气体的化学方程式。一般不选择E装置收集二氧化碳的原因是。
-
(4) 实验室用高锰酸钾制氧气,可用A作发生装置的原因是。
-
(1) 研究表明:氨气与氢气可在催化剂表面合成氨,下图是合成氨过程的微观示意图,其符合题意的顺序是(填序号)。
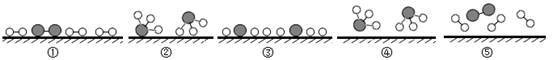
(图中
 表示氮原子,
表示氮原子,  表示氢原子,
表示氢原子,  表示催化剂)
表示催化剂) -
(2) 如下实验装置:
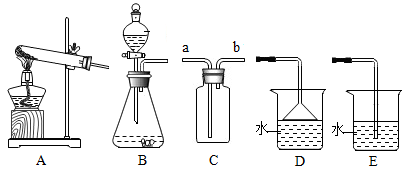
①实验室可采用B装置制取氧气,反应的化学方程式是。
②实验室加热氯化铵和氢氧化钙两种固体可制取氨气,发生装置可选用上图的(填“A”或“B”),若用C装置收集氨气,气体应从(填“a”或“b”)端进入,此时检验氨气是否收集满的方法是。大量氨气泄漏会对环境造成极大危害,某同学设计D、E两种尾气处理装置,你认为最优的是(填 “D”或“E”)装置,理由是。

-
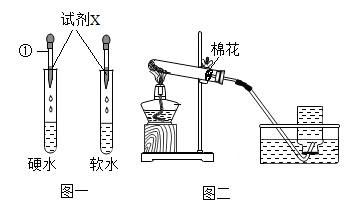
(1) 写出用A装置制取氧气的一个化学方程式。
-
(2) 利用最优的反应原理制取并收集一瓶干燥的氧气,组装装置可以按顺序选用图中的(填字母序号)。
-
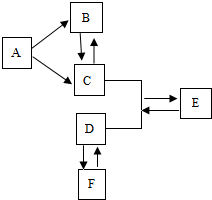
(1) 图一中仪器①加试剂的方法是否正确。
-
(2) 图一是硬水和软水的鉴别,图中试剂X是,加入试剂X后接下来进行的操作是,在进行完该操作后在软水中观察到的现象是。
-
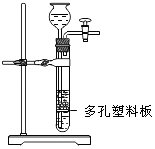
(3) 图二是实验室制取并收集氧气的常用装置,请写出图二试管中发生的化学反应方程式。实验时如果把棉花塞得过多过紧,可能造成的后果是,图中所示方法收集氧气说明氧气具有的一条物理性质是。
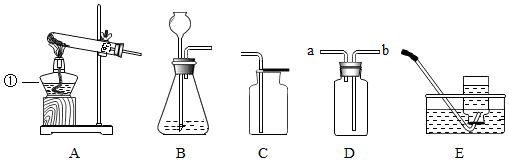
试推断:
-
(1) 物质B的化学式为。
-
(2) 请写出A→C的化学方程式 。
-
(3) E→C+D的基本反应类型是 。
-
(4) 请写出D→F的化学方程式。
-
(1) 图中仪器①的名称。
-
(2) 实验时,先要检查装置的,若用过氧化氢溶液制取氧气,应选用的发生装置是,若用D收集氧气应从口进气。
-
(3) 实验室用高锰酸钾制取氧气且用E装置收集,集满时应在(填“水下”或“水面”)立即用玻璃片将集气瓶的瓶口盖好取出正立。写出该反应的符号表达式。
-
(4) 用C装置收集一瓶氧气,将点燃的蜡烛放入集气瓶中,用玻璃片盖住,观察到蜡烛剧烈燃烧发白光,且瓶壁上有水雾出现,说明有水生成,然后将蜡烛从集气瓶中取出,(填实验步骤和现象),证明蜡烛燃烧还生成了二氧化碳。
-
(1) 写出装置C中标号仪器名称:b;
-
(2) 加热高锰酸钾制取并收集较干燥的氧气,应选择的制取和收集装置(填标号),反应的表达式 ,试管口堵一团棉花的目的是;
-
(3) 若用过氧化氢溶液制氧气,为了控制反应的速率,则应选择的发生装置为(填标号),反应的表达式是,若用B来制取氧气,为防止气体从长颈漏斗中逸出应。
-
(4) 若用上图装置采用排空气法收集氧气则气体应从端(填a或b)通入,若利用排水法收集氧气,则瓶内先注满水,氧气应从端(填a或b)通入;
-
(5) 实验室常用加热氯化铵和熟石灰两种固体混合物的方法制取氨气,已知氨气在通常状况下是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,实验室制取并收集氨气,所选择的发生和收集装置是(填标号)。

-
(1) 写出图中标号X的仪器的名称。
-
(2) 实验室用该装置制取氧气时应选择的药品是:;其化学方程式为:。
-
(3) 除了制取氧气,该装置还可以制取我们学过的哪种气体,请写出反应需要用到的药品。
-
(4) 请写出用该装置收集气体的优点和缺点:。



