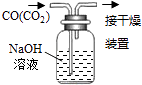
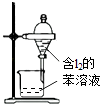
洗气 知识点题库
①Cu ②新制的氯水 ③FeCl2溶液 ④碱石灰 ⑤(NH4)2SO4固体 ⑥KOH固体 ⑦稀硫酸 ⑧SO2
(1)能导电的是 ;属于电解质的是 ;属于非电解质的是 .
(2)碱石灰常用作干燥剂,它不能干燥下列 气体
A.H2 B.NH3 C.Cl2 D.O2 E.SO2
(3)向②溶液中加入KBr溶液后,用CCl4萃取,CCl4层呈棕红色,写出该反应过程的离子方程式标出电子转移方向和数目:
(4)写出实验室检验⑤中的阳离子的操作方法:
掌握仪器名称、 组装及使用方法是中学化学实验的基础,图为实验装置.
组装及使用方法是中学化学实验的基础,图为实验装置.
-
(1) 写出下列仪器的名称:
a. b.
-
(2) 蒸馏烧瓶进行加热时盛液体不要超过烧瓶容量的 ,还需加入几块碎瓷片,其作用是
-
(3) 若利用装置分离四氯化碳和 酒精的混合物,还缺少的仪器是 , 将仪器补充完整后进行实验,温度计水银球的位置在 处.冷凝水由 (填f或g)口通入 (填f或g)口流出.
A.配制0.10mol•L﹣1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2 , 分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
-
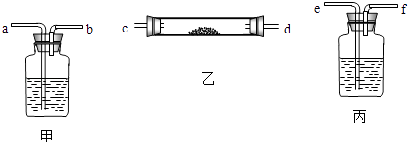
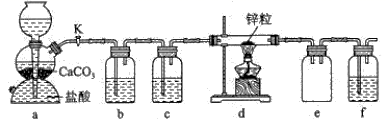
(1) 甲装置的作用是丙装置的作用是
-
(2) 为达到上述①﹣③的目的,用各装置接口的代号,表示出正确的连接顺序..
-
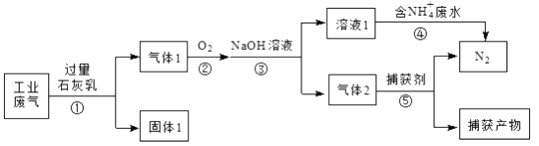
(1) 固体1的主要成分除Ca(OH)2外,还有、(填化学式)。
-
(2) 为使反应①中的有关气体被充分吸收,可采取的措施有:①增大接触面积;②。
-
(3) 已知:
2NO2+2NaOH=NaNO3+NaNO2+H2O
NO2+NO+2NaOH=2NaNO2+H2O
为确保反应③只生成NaNO2 , 理论上应控制NO与O2的物质的量之比为;此时反应④的离子方程式为。若n(NO) :n(O2)=3:1,且NaOH溶液足量,则所得溶液1中NaNO3与NaNO2的物质的量之比为。
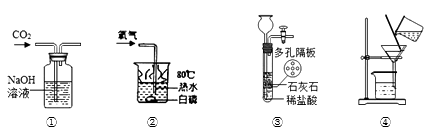
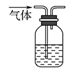 B .
B . 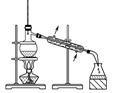 D .
D . 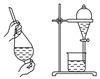
-
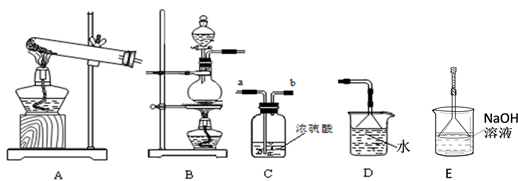
(1) 下列气体中,只能用碱石灰干燥的是_______(填字母)。A . H2 B . Cl2 C . SO2 D . NH3 E . O2
-
(2) 实验室用软锰矿(主要成分是MnO2)与浓盐酸混合加热制得氯气,所选制备装置是,干燥氯气的装置是,尾气处理装置是。
-
(3) 实验室用氯化铵和熟石灰制取氨气,其化学反应方程式为,收集氨气的方法是,检验收集氨气已满的常用方法是(任写一种)。
-
(4) 将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应。生成的氨气在标准状况下的体积是 L,若将这些氨气溶于水配成500ml氨水,该氨水的物质的量浓度是
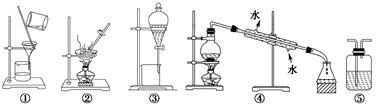
已知:①无水四氯化锡的熔点为-33℃、沸点为114.1℃;②四氯化锡易水解。下列说法正确的是( )
-
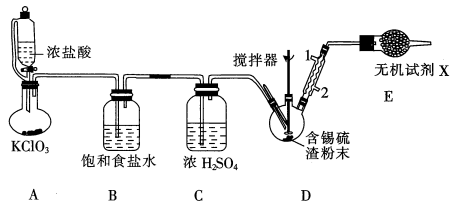
(1) 乙炔水化法:在75℃左右,用
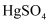 做催化剂,乙炔可水化为乙醛,但
做催化剂,乙炔可水化为乙醛,但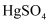 遇到某些特定物质常会发生催化剂中毒而失去催化作用,
遇到某些特定物质常会发生催化剂中毒而失去催化作用, 就是其中一种。实验装置如图所示
就是其中一种。实验装置如图所示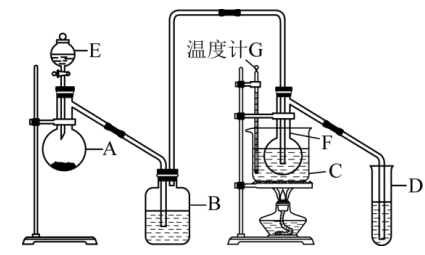
已知:F装置中已按顺序加入了氧化汞、水、浓硫酸。
①实验开始时,仪器A中盛放电石,B中应装。
②仪器D中盛放水,作用是,进一步提纯乙醛的操作是。
③装置图中,所选用温度计G的量程为(填标号)。
A.0~50℃ B.0~100℃ C.0~200℃
④请用化学方程式表示出装置F中的反应:。
-
(2) 乙烯氧化法:将乙烯、氧气和催化剂(
 和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据
和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据物质/项目
乙炔水化法
乙烯氧化法
平衡转化率
乙炔平衡转化率90%左右
乙烯平衡转化率80%左右
日产量
2.5吨(某设备条件下)
3.6吨(相同设备条件下)
从化学反应速率角度分析,在相同设备条件下,选用法制取乙醛快。
分离提纯 | 试剂 | 方法 | |
A | 除去CO2中的HCl | NaOH溶液 | 洗气 |
B | 提取溴水中的溴单质 | CCl4 | 萃取 |
C | 除去NaCl中的Na2CO3 | 盐酸 | 蒸发结晶 |
D | 除去H2O中的Fe3+ | — | 蒸馏 |