尾气处理装置 知识点题库

①H2S ②HCl ③NH3 ④Cl2 ⑤SO2 ⑥C2H4


 B .
B .  C .
C .  D .
D . 
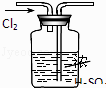 干燥Cl2
B .
干燥Cl2
B .  吸收HCl
C .
吸收HCl
C . 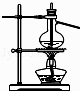 石油的分馏
D .
石油的分馏
D . 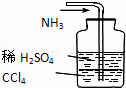 吸收NH3
吸收NH3

 2AlCl3+3H2。以下说法正确的是( )
2AlCl3+3H2。以下说法正确的是( )
 HCl↑+NaHSO4
B . 粗导管d也可换成细导管
C . e中试剂可选用碱石灰、无水氧化钙或五氧化二磷
D . 为了减少HCl的浪费,实验开始时先点燃b处酒精灯
HCl↑+NaHSO4
B . 粗导管d也可换成细导管
C . e中试剂可选用碱石灰、无水氧化钙或五氧化二磷
D . 为了减少HCl的浪费,实验开始时先点燃b处酒精灯
 制取乙酸乙酯
B .
制取乙酸乙酯
B .  吸收NH3
C .
吸收NH3
C .  石油的分馏
D .
石油的分馏
D .  比较盐酸、碳酸、苯酚的酸性强弱
比较盐酸、碳酸、苯酚的酸性强弱
 B . 吸收尾气中的二氧化硫
B . 吸收尾气中的二氧化硫  C . 溶解反应后烧瓶内混合物中的硫酸铜固体
C . 溶解反应后烧瓶内混合物中的硫酸铜固体  D . 加热硫酸铜溶液制备胆矾
D . 加热硫酸铜溶液制备胆矾 
-
(1) I. 甲小组的同学用如图装置制备干燥纯净的Cl2 , 并进行性质实验。

装置A中制取氯气,三种玻璃仪器的名称分别是酒精灯、和,反应的化学方程式为。该反应中盐酸体现了(填字母)。
a.氧化性 b.还原性 c. 酸性 d. 碱性
-
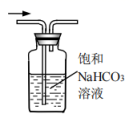
(2) 装置B的作用是。
-
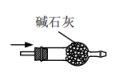
(3) 装置C中盛放的是,目的是除去水蒸气。
-
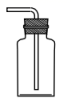
(4) 装置D可以用作不同的用途。
a. 若装置D用于收集Cl2 , 请将图中装置D的导气管补充完整。
b. 若装置D中放入湿润的蓝色石蕊试纸,可以看到的现象是。
-
(5) II. 乙小组的同学用如图所示装置制取氯水并进行相关实验。

实验进行一段时间后,取少量试管①中的溶液,检验其中有Cl-的方法是。
III. 甲、乙两个小组的同学都用到了NaOH溶液,目的是,反应的离子方程式为。


-
(1) 仪器 D 的名称是。安装 F 中导管时,应选用图2中的。
-
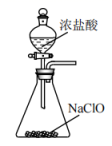
(2) 打开 B 的活塞,A 中发生反应:2NaClO3+4HCl
 2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜 (填“快”或“慢”)。
2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜 (填“快”或“慢”)。
-
(3) 关闭 B 的活塞,ClO2 在 D 中被稳定剂完全吸收生成 NaClO2,此时 F 中溶液的颜色不变,则装置 C 的作用是 。
-
(4) 已知在酸性条件下 NaClO2 可发生反应生成 NaCl 并释放出 ClO2,该反应的离子方程式为,在 ClO2 释放实验中,打开 E 的活塞,D 中发生反应,则装置 F的作用是 。
-
(1) 甲组同学设计下列装置用干燥纯净的氯气制备实验原料漂白粉[已知:3Ca(ClO)2
 Ca(ClO3)2+2CaCl2△H>0]。
Ca(ClO3)2+2CaCl2△H>0]。 
①各仪器接口连接顺序为(气流自左至右,用小写字母表示)。
②装置B中发生反应的离子方程式为 。
③装置A用冰水冷却的目的是。
-
(2) 乙组同学用甲组制得的漂白粉与乙醇溶液反应制备氯仿的实验装置如图。

①装置I需控制温度约为70℃,适宜的加热方式是 ,温度不宜过高,其目的是。
②装置Ⅱ的名称是。
③一定条件下,装置I中漂白粉先与乙醇溶液反应生成Cl2和Ca(OH)2 , 然后Cl2与CH3CH2OH反应生成CCl3CHO,CCl3CHO再与Ca(OH)2反应生成CHCl3和一种盐,CCl3CHO与Ca(OH)2反应的化学方程式为 。
-
(3) 丙组同学用下列方法对乙组制得的粗产品进行提纯。已知浓硫酸能与乙醇混溶。
步骤I.向粗产品中加入适量浓硫酸,搅拌至呈淡咖啡色,分液得有机层;
步骤Ⅱ.用15%的Na2CO3溶液洗涤多次,分液得有机层;
步骤Ⅲ.向有机层中加入少量无水CaCl2。
步骤I中用浓硫酸洗涤的目的是;步骤Ⅱ中证明已洗涤干净的依据是;步骤Ⅲ中加入少量无水CaCl2的目的是 。

|
乙醇 |
溴乙烷 |
液溴 |
|
|
相对分子质量 |
46 |
109 |
160 |
|
状态 |
无色液体 |
无色液体 |
深红色液体 |
|
密度/(g·cm-3) |
0.79 |
1.44 |
3.1 |
|
沸点/℃ |
78.5 |
38.4 |
59 |
-
(1) I.溴乙烷的制备:
反应原理如下:
H2SO4+NaBr
 NaHSO4+HBr↑
NaHSO4+HBr↑ CH3CH2OH+HBr
 CH3CH2Br+H2O
CH3CH2Br+H2O实验装置如图(加热装置夹持装置均省略):

图甲中B仪器的名称,作用为。
-
(2) 若图甲中A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应生成了;F连接导管通入稀NaOH溶液中,其目的主要是吸收等尾气防止污染空气。
-
(3) II.溴乙烷性质的探究。用如图实验装置验证溴乙烷的性质:

在乙中试管内加入10 mL 6 mol·L-1 NaOH溶液和2 mL溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为。
-
(4) 若将乙中试管里的NaOH溶液换成NaOH乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a试管中的水的作用是;若无a试管,将生成的气体直接通入b试管中,则b中的试剂可以为。
①2MoS2+7O2 2MoO3+4SO2
2MoO3+4SO2
②MnO3+2NH3·H2O=(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl
④H2MoO4 MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法中错误的是( )
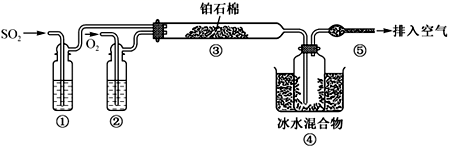
下列说法正确的是( )
选项 | A | B | C | D |
实验 装置 |
|
|
|
|
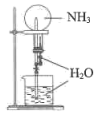
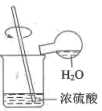
实验 目的 | 氨气溶于水的喷泉实验 | 制备乙酸乙酯 | 收集 | 稀释浓硫酸 |

| 选项 | 实验目的 | X中试剂 | Y中试剂 |
| A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
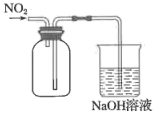
| B | 用Cu与浓硝酸制取并收集纯净干燥的NO2 | 水 | 浓硫酸 |
| C | 用大理石和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| D | 锌和稀盐酸制取并收集纯净干燥的H2 | 水 | 浓硫酸 |
|
|
|
|
A.制备Cl2 | B.除去Cl2中的少量HCl | C.干燥Cl2 | D.收集Cl2 |

 并处理尾气
并处理尾气