气体摩尔体积 知识点题库
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.
该小组设计的简易实验装置如图所示:
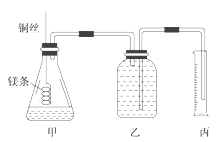
该实验的主要操作步骤如下:
-
(1) ①配制100mL 1.0mol•L﹣1的盐酸溶液;
②用 (填仪器名称并注明规格)量取7.5mL 1.0mol•L﹣1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为 ;
④往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL.
请将上述步骤补充完整并回答下列问题.
-
(2) 步骤①中,配制100mL 1.0mol•L﹣1的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母) .
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
-
(3) 实验步骤⑤中应选用 (填字母)的量筒.
A.100mL B.200mL C.500mL
-
(4) 读数时除恢复到室温外,还要注意
① ,②
-
(5) 忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm= L/mol.
下列叙述正确的是( )
A . 1mol H2O的质量为18g/mol
B . CO2的摩尔质量为44g
C . 3.01×1023个SO2分子的质量为32g
D . 标准状况下,1mol任何物质体积均为22.4L
NA表示阿伏加德罗常数,下列说法正确的是( )
A . 1 mol•L-1NaHCO3溶液中,Na+数目为NA
B . 2.4gMg与足量盐酸完全反应时,失去电子数目为0.1NA
C . 等物质的量的N2和CO所含分子数、原子个数、电子总数均相同
D . 标准状况下,11.2L的水中含有0.5个NA水分子
下列各组物质中,所含原子数相同的是( )
A . 5.6LCH4(标准状况)和17.5g N2
B . 16gO2和24gO3
C . 224mL H2(标准状况)和0.1mol CO2
D . 标准状况下,11.2LH2O和0.5molSO2
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 4.4g由CO2和N2O组成的混合气体中的电子数为2.2NA
B . 密闭容器中0.5molH2与0.5molI2反应生成NA个H-I键
C . 2.4g镁在足量的O2中燃烧,转移的电子数为0.1NA
D . 1L1mol/L碳酸氢钠溶液中的HCO3-数为NA
计算
-
(1) 2.33gBaSO4的物质的量mol。
-
(2) 标准状况下6.72L N2的物质的量mol。
-
(3) 等质量的O2与O3在同温同压下的体积之比。
-
(4) 同温同压同体积的CO2与SO2的质量之比。
-
(5) 同温同压下条件下CO与CO2的密度之比。
常温常压下,等质量的 NH3、Cl2、NO、SO2 分别吹出四个气球,其中所充气体为 NO 的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
-
(1) Ⅰ.在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是。
-
(2) 由A、B两种双原子分子组成的混合气体8.6g,在标准状况下的体积为8.96L,已知A和B的物质的量之比为3∶1,摩尔质量之比为14∶1,则A可能是(写出两种可能的分子式),B的分子式是。
-
(3) 在标准状况下,CO和CO2的混合气体质量36g,体积为22.4L,则CO所占体积是L,CO的质量是g。
-
(4) Ⅱ .标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸密度为1.18 g·cm-3。试计算:
所得盐酸的质量分数和物质的量浓度分别是、。
-
(5) 取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是。
-
(6) 在40.0 mL 0.065 mol·L-1Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过mL。
-
(7) 将不纯的NaOH样品1 g(样品含少量Na2CO3和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到g固体。
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,将m1g锌加入到m2g 20%的盐酸中放出nL H2 , 则转移电子数为nNA/11.2
B . 0.1 mol/L的100mL H2SO3溶液中,含有的离子数约为0.03NA
C . 1molSiO2中含有共价键数是2NA
D . 120 g由NaHSO4和KHSO3固体组成的混合物中含有的阴阳离子总数为5NA
下列说法正确的是( )
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·mol−1
⑥标准状况下,体积相同的气体的分子数相同
A . ①③⑤
B . ④⑥
C . ③④⑥
D . ①④⑥
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移
B . 100mL1 mol·L-1 FeCl3溶液中所含Fe3+的数目为0.1NA
C . 1molSO2与足量O2在一定条件下反应生成SO3 , 共转移2NA个电子
D . 84 gNaHCO3固体含有CO32-离子的数目为NA
C,N,O,S,H都是中学化学中常见的元素。按要求完成下列填空。
-
(1) 0.5 mol CH4的质量为;标准状况下,4.48 L NH3所含分子数为。
-
(2) 等物质的量的CH4、NH3和N2三种气体,所含原子数之比为,等质量的CH4和N2物质的量之比为。
-
(3) 某气态氧化物化学式为RO2 , 在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为,R的相对原子质量为。
-
(4) 在标准状况下,由SO2和CO2组成的混合气体为8.96 L,质量为24 g,该混合气体的平均摩尔质量是,混合气体中CO2的体积分数是。
NA为阿伏加德罗常数的数值。下列说法正确的是( )
A . 标准状况下,11.2 L的SO3中所含原子数为2NA
B . 1 mol Na2O2固体中含离子总数为4NA
C . 1 mol/L的Na2CO3溶液中所含阴离子数大于NA
D . 标准状况下,11.2LCH3Cl含质子数为13NA
设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A . 标准状况下,11.2L三氯甲烷中含有分子数为0.5NA
B . 常温常压下,2gD2O中含有电子数为NA
C . 46gNO2和N2O4混合气体中含有原子数为3NA
D . 1 mol Na完全与O2反应生成Na2O和Na2O2 , 转移电子数为NA
下列说法中正确是( )
A . 1mol/L的NaCl溶液是指此溶液中含有1molNaCl
B . 从1L1mol/L的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol/L
C . 0℃时,1molCl2的体积约为22.4L
D . 1mol/L的CaCl2溶液中,Cl-的物质的量浓度为2mol/L
设N A为阿伏加德罗常数的值,下列说法正确的是( )
A . 1mol FeBr2 与1mol Cl2 完全反应后,转移电子数为 2NA
B . 16.2n g 淀粉[(C6H10O5)n]中含有 0.1 NA葡萄糖单元
C . 将1mol NH3 完全溶于水,所得溶液中 N( NH3•H2O ) +N( NH4+) = NA
D . 若5.6L N2中含有n个氮分子,则NA =4n
下列说法正确的是( )
A . 1mol 任何粒子或物质的质量,其数值都与该粒子的相对原子质量或相对分子质量相等
B . 在 0℃和 101kPa(标准状况)的条件下,1mol 任何物质所占的体积约为 22.4L
C . 如果 1L 水中含有 1mol NaOH,那么这种溶液中NaOH 的物质的量浓度就是 1mol/L
D . 我们通常把 1mol 任何粒子的粒子数叫做阿伏加德罗常数
NA表示阿伏加德罗常数的数值。下列说法正确的是( )
A . 标准状况下,11.2LH2O中原子数目为1.5NA
B . 常温常压下,0.1mol·L-1的氨水中NH4+、NH3、NH3·H2O三种微粒的数目为0.1NA
C . 常温常压下,将1molCl2通入足量水中充分反应转移电子数目小于NA
D . 标准状况下,3.8gNO与NO2混合气体中分子数目为0.05NA
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A . 2 g氢气所含原子数目为NA
B . 在常温常压下,11.2 L氮气所含的原子数目为NA
C . 标准状况下,22.4 L H2O的分子数为1 NA
D . 14 g CO含有分子数为0.5 NA
设NA是阿伏加德罗常数的值。下列说法正确的是( )
A . 22.4L(标准状况)三氧化硫中含有40NA个质子
B . 常温常压下,8g氦气中含有的分子数为NA
C . 常温常压下,28g乙烯和丙烯的混合气体中含有4NA个氢原子
D . 1L1mol·L−1Na2SO4溶液中含有4NA个氧原子
最近更新



