焰色反应 知识点题库
利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩.下列说法中正确的是( )
A . 非金属单质燃烧时火焰均为无色
B . NaCl与Na2CO3灼烧时火焰颜色相同
C . 焰色反应均应透过蓝色钴玻璃观察
D . 只有金属单质灼烧时火焰才有颜色
化学与科技、社会、生产、生活密切相关.下列有关说法不正确的是( )
A . 物质燃烧时产生有色火焰的都是焰色反应的见证
B . 棉花、木材和植物秸秆的主要成分都是纤维素
C . 航天服主要成分由碳化硅陶瓷和碳纤维复合而成,是一种复合材料
D . 天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
为了验证食盐的主要成分,将食盐溶于水,然后进行焰色反应,焰色呈黄色,说明含有 离子;往食盐溶液中加入AgNO3溶液和稀HNO3 , 有白色沉淀产生,说明含有 离子.
下列有关焰色反应的叙述正确的是( )
A . 只有金属的化合物灼烧时才会有不同的颜色
B . 每次实验后,铂丝都要用水洗净
C . 若透过蓝色钴玻璃只看到紫色,说明样品中含钾元素而一定不含钠元素
D . 若样品灼烧呈黄色,判断一定有钠元素,但不能排除含其他金属元素
有关焰色反应的实验操作注意事项的说明有:①钾的焰色要透过蓝色钴玻璃观察;②先将洗净的铂丝灼烧到与原火焰颜色相同,再蘸取被检物质;③每次实验完,均要用盐酸洗净铂丝.其中正确的是( )
A . 只有①
B . 只有③
C . 只有①②
D . 全部
做焰色反应实验用的铂丝,每试验一种样品后都必须进行的操作是( )
A . 用水洗涤2~3次后再使用
B . 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
C . 用滤纸擦干后才可使用
D . 用盐酸洗涤后,经蒸馏水冲洗,方可使用
焰色实验过程中,铂丝的清洗和灼烧与钾焰色实验的观察两项操作如图所示,下列叙述中错误的是( )

A . 每次实验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质
B . 钾的焰色实验要透过蓝色钴玻璃观察
C . 焰色实验是某种金属元素灼烧时所具有的特殊颜色,是化学变化
D . 没有铂丝可用无锈铁丝代替进行实验
按要求填空:
-
(1) 写出新制氯水中含量最多的微粒的化学式(水分子除外)
-
(2) 写出漂白粉中有效成分的名称
-
(3) 描述检验溶液中K+离子的实验操作过程
-
(4) 配平下列化学方程式
()Cu+()HNO3(稀)=()Cu(NO3)2+()NO↑+()H2O
-
(5) 按照物质的分类,次磷酸(H3PO2)属于二元酸,其与足量的NaOH溶液反应的化学方程式为
下列说法正确的是( )
A . 用焰色反应检验Na+之前应用稀硫酸清洗铁丝
B . 将Na单质长时间放置在空气中, 最终得到的白色固体是NaHCO3
C . SiO2不能溶于水生成H2SiO3 , 因此SiO2不是酸性氧化物
D . 盐酸、氨水、碱石灰都是混合物
用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)( )
A . 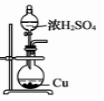 制取二氧化硫气体
B .
制取二氧化硫气体
B . 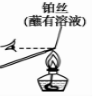 检验溶液中是否有钾离子
C .
检验溶液中是否有钾离子
C . 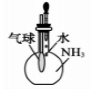 验证氨气极易溶解于水
D .
验证氨气极易溶解于水
D . 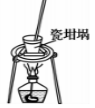 加热氢氧化钠固体
加热氢氧化钠固体
 制取二氧化硫气体
B .
制取二氧化硫气体
B .  检验溶液中是否有钾离子
C .
检验溶液中是否有钾离子
C .  验证氨气极易溶解于水
D .
验证氨气极易溶解于水
D .  加热氢氧化钠固体
加热氢氧化钠固体
某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液,加氢氧化钠溶液过程中无沉淀生成;
②另取少量原溶液,逐滴加入5 mL 0.2 mol·L-1盐酸,产生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失;
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43 g。
下列说法中正确的是( )
A . 该溶液中一定不含Ba2+、Mg2+、Al3+、SiO32-、Cl-
B . 该溶液中一定含有K+、AlO2-、CO32-、Cl-
C . 该溶液是否有K+需做焰色反应实验(透过蓝色钴玻璃片)
D . 可能含有Cl-
根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向NaCl、NaI的混合稀溶液中滴入少量稀 AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| B | 室温下,向溶液X中滴加少量双氧水,再加入KSCN溶液,变红 | 溶液X中一定含Fe2+ |
| C | 用洁净铂丝蘸取溶液Y在火焰上灼烧,火焰呈黄色溶液 | Y中含 Na+不含K+ |
| D | 室温测定浓度均为0.1mol·L-1的CH3COONa溶液和NaNO2溶液的pH, CH3COONa 溶液的pH大 | HNO2 电离出H+的能力比CH3COOH强 |
A . A
B . B
C . C
D . D
下列检验方法及结论正确的是( )
A . 某溶液进行焰色试验时,若火焰呈黄色,则该溶液中含Na+
B . 向某溶液中加入AgNO3溶液,若产生白色沉淀,则该溶液中一定含有Cl-
C . 向某溶液中加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则该溶液中一定含有  D . 向某溶液中加入稀HCl溶液,若产生无色无味气体,则该溶液中一定含有
D . 向某溶液中加入稀HCl溶液,若产生无色无味气体,则该溶液中一定含有 
 D . 向某溶液中加入稀HCl溶液,若产生无色无味气体,则该溶液中一定含有
D . 向某溶液中加入稀HCl溶液,若产生无色无味气体,则该溶液中一定含有 
化学与生产生活等均密切相关,下列有关叙述错误的是( )
A . 《吕氏春秋•别类编》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特征
B . 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也",该方法应用了焰色反应
C . “墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”具有胶体的性质
D . 我国预计2020年发射首颗火星探测器太阳能电池帆板的材料是二氧化硅
下列有关化学现象和化学概念表述正确的是( )
A . 浓硫酸和浓盐酸长期暴露在空气中浓度都会降低,且原理相同
B . Fe(OH)3胶体做电泳实验时,由阴极区红色加深可知 Fe(OH)3胶体带正电荷
C . 某次焰色试验火焰为黄色,不能说明该物质中一定不含 K+
D . 0.5 mol Fe和含1 mol HNO3的稀溶液充分反应后,滴入 KSCN溶液,溶液变红
焰色试验过程中,铂丝的清洗和灼烧与钾焰色试验的观察两项操作如图所示,下列叙述中错误的是( )
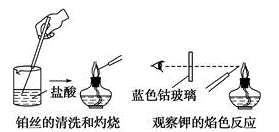
A . 焰色试验是某种金属元素灼烧时所具有的特殊颜色,是化学变化
B . 每次试验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质
C . 钾的焰色试验要透过蓝色钴玻璃观察
D . 没有铂丝可用无锈铁丝代替进行试验
某化学兴趣小组的同学探究KI的性质。
-
(1) 通过反应实验可以验证KI中K元素的存在。
-
(2) ①根据碘元素的化合价可推知KI有性。
②与KI反应,能体现上述性质的试剂有(填序号)
a.Fe2+ b.Fe3+ c.Br- d.Cl2
-
(3) 兴趣小组的同学们猜测:Cu2+有可能氧化I- , 为了验证,他们做了如下实验。(已知:CuI为不溶于水的白色沉淀)
操作
现象

溶液分层,上层显紫色,有白色沉淀生成
结论:Cu2+能氧化I-。写出反应的离子方程式。
-
(4) ①同学们依据(3)的结论推测:Ag+能氧化I- , 原因为。
他们做了如下实验进行探究
实验一:
操作
现象

生成黄色沉淀
②发生反应的化学方程式为。
实验二:
操作
现象
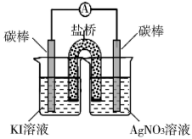
3分钟后KI溶液开始变黄,随后溶液黄色加深,取出该烧杯中溶液滴入盛有淀粉溶液的试管,溶液变蓝。
③甲同学认为根据上述实验现象不能说明Ag+能氧化I- , 原因是。乙同学在上述实验基础上进行了改进,并得出结论:Ag+能氧化I-。发生反应的离子方程式为。
④由以上两个实验得出的结论为。
下列实验操作或说法不正确的是( )
A . 可通过观察镁片和铝片与同浓度盐酸反应的剧烈程度比较Mg和Al的金属性强弱
B . 配制500mL某浓度的稀盐酸,定容时仰视读数,导致所配溶液浓度偏低
C . 焰色试验时需用稀硫酸洗净铂丝,并在火焰上灼烧至无色
D . 丝绸与棉布可以通过燃烧闻气味的方法进行鉴别
下列说法错误的是( )
A . 原子光谱可用于鉴定氢元素
B . 电解法可用于冶炼铝等活泼金属
C . 分馏法可用于提高石油中乙烯的产量
D . 焰色试验可用于区分NaCl和KCl
生活中处处有化学,下列叙述正确的是( )
A . 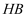 铅笔芯的成分为二氧化铅
B . 碳酸氢钠可做食品膨松剂
C . 青铜和黄铜是不同结构的单质铜
D . 焰火中红色来源于钠盐灼烧
铅笔芯的成分为二氧化铅
B . 碳酸氢钠可做食品膨松剂
C . 青铜和黄铜是不同结构的单质铜
D . 焰火中红色来源于钠盐灼烧
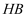 铅笔芯的成分为二氧化铅
B . 碳酸氢钠可做食品膨松剂
C . 青铜和黄铜是不同结构的单质铜
D . 焰火中红色来源于钠盐灼烧
铅笔芯的成分为二氧化铅
B . 碳酸氢钠可做食品膨松剂
C . 青铜和黄铜是不同结构的单质铜
D . 焰火中红色来源于钠盐灼烧
最近更新



