硅酸的性质及制法 知识点题库
下列各实验中,先产生沉淀,然后沉淀又溶解的是 ( )
①向饱和碳酸钠溶液中通入CO2至过量
②向氯化铝溶液中逐滴加入氢氧化钠溶液至过量
③向AgNO3溶液中逐滴加入氨水至过量
④向硅酸钠溶液中逐滴加入盐酸至过量
①向饱和碳酸钠溶液中通入CO2至过量
②向氯化铝溶液中逐滴加入氢氧化钠溶液至过量
③向AgNO3溶液中逐滴加入氨水至过量
④向硅酸钠溶液中逐滴加入盐酸至过量
A . ①②
B . ①③
C . ①④
D . ②③
下列有关物质的性质和应用均正确的是( )
A . NH3能氧化氮氧化物,可用于汽车尾气净化
B . 瓷坩埚能耐高温,可用于加热分解石灰石
C . Fe在O2中的燃烧产物可用于制红色涂料
D . Mg (OH)2分解吸热且生成高熔点固体,可用作阻燃剂
以下六种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③Na2SiO3 ④Na[Al(OH)4]⑤Na2CO3⑥NH3和NaCl,分别持续通入CO2 , 最终得到沉淀或析出晶体的是( )
A . ①③④⑥
B . ②③④⑥
C . ③④⑤⑥
D . ②③④⑤
下列说法不正确的是( )
A . “西气东输”就是将新疆等地的天然气通过管道输到长江三角洲
B . 乙烯和苯是来自石油和煤的两种有机物,它们都能发生加成反应
C . 糖类、油脂和蛋白质是基本营养物质,它们都是天然高分子化合物
D . 乙烯和氯乙烯都可以通过聚合反应得到高分子材料
露置于空气中一段时间后的水玻璃会浑浊.向此浑浊溶液中加入稀盐酸,会生成白色沉淀,同时伴随有气泡产生.用化学方程式解释产生上述现象的原因:
(1)溶液变浑浊:
(2)生成白色沉淀:
(3)产生气泡:
向硅酸钠溶液中滴加盐酸制硅胶的方程式是
请回答:
-
(1) NaOH的电子式为.
-
(2) 工业上常用焦炭还原二氧化硅制备粗硅,用化学方程式表示.
-
(3) FeSO4溶液与稍过量的NH4HCO3溶液混合,有FeCO3白色沉淀生成和明显的无色气泡现象,写出相关离子方程式.
-
(4) 完成以下氧化还原反应的离子方程式:
() Cr2O2﹣7+() H2O2+()═() Cr3++()H2O+().
将足量CO2气体通入硅酸钠溶液中,然后加热蒸干,再在高温下充分反应,最后所得的固体物质是( )
A . Na2SiO3
B . Na2CO3、Na2SiO3
C . Na2CO3、SiO2
D . SiO2
下列各组物质不能按( 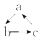 “
“  ” 表示反应一步完成)关系转化的是 ( )
” 表示反应一步完成)关系转化的是 ( )
 ” 表示反应一步完成)关系转化的是 ( )
” 表示反应一步完成)关系转化的是 ( )选项 | a | b | c |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | Fe | Fe(OH)3 | Fe2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A . A
B . B
C . C
D . D
下列物质转化在给定条件下每一步都能实现的是()
A . Si 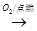 SiO2
SiO2 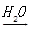 H2SiO3
B . Mg(OH)2
H2SiO3
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq) 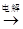 Mg
C . Al2O3
Mg
C . Al2O3  AlCl3(aq)
AlCl3(aq) 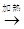 无水AlCl3
D . CH3CHO
无水AlCl3
D . CH3CHO 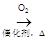 CH3COOH
CH3COOH  CH3COOCH3
CH3COOCH3
下列选用的除杂方法错误的是(括号内为杂质)()
A . CO2(HCl)通过足量的饱和碳酸钠溶液、干燥
B . SiO2(H2SiO3)加热,使H2SiO3分解
C . Cl2(HCl)通过足量的饱和氯化钠溶液、干燥
D . FeCl2溶液(FeCl3)加过量的Fe粉、过滤
下列说法正确的是( )
A . CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
B . 检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可
C . 在粗硅的制取中,2C+SiO2  Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
 Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A . CO2溶于水形成碳酸,SiO2难溶于水
B . 高温下SiO2与碳酸盐反应生成CO2
C . CO2通入可溶性硅酸盐中析出硅酸沉淀
D . HCl通入可溶性碳酸盐溶液中放出气体,氯化氢通入可溶性硅酸盐溶液中生成沉淀
下列物质的转化在给定条件下能实现的是( )
①盐卤(含MgCl2) 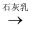 Mg(OH)2
Mg(OH)2  MgCl2溶液
MgCl2溶液  无水MgCl2
无水MgCl2
②铝土矿  AlO2-
AlO2- 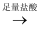 Al(OH)3
Al(OH)3 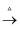 Al2O3
Al2O3
③NH3 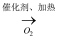 NO
NO  NO2
NO2  HNO3
HNO3
④NaCl溶液  Cl2
Cl2 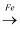 无水FeCl2
无水FeCl2
⑤S  SO3
SO3  H2SO4
H2SO4
⑥SiO2  Na2SiO3溶液
Na2SiO3溶液  H2SiO3
H2SiO3
A . ③⑥
B . ③⑤⑥
C . ①④⑤
D . ①③⑥
下列叙述正确的是( )
A . 因为Na2CO3+SiO2  Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B . 碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C . 二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D . 二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B . 碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C . 二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D . 二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
 Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B . 碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C . 二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D . 二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B . 碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C . 二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D . 二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
下列叙述错误的是( )
A . 硅在自然界中主要以单质形式存在
B . 硅是应用最为广泛的半导体材料
C . 高纯度的硅可用于制造计算机芯片
D . 二氧化硅可用于生产玻璃
下列物质之间的转化都能一步实现的是( )
A . H2S→S→SO3→H2SO4
B . Si→SiO2→H2SiO3→Na2SiO3
C . FeS2→SO2→Na2SO3→Na2SO4
D . N2→NH3→NO2→HNO3→NO2
利用元素在元素周期表中的“位构性”关系,我们可以预测陌生元素及其化合物的性质。下列有关铝、硅元素及其化合物的叙述正确的是( )
A . 氢氧化铝既能溶于盐酸又能溶于NaOH溶液
B . 二氧化硅属于酸性氧化物,不能与任何酸反应
C . 铝属于活泼金属,其化合物中一定存在离子键
D . 硅酸是一种弱酸,可由二氧化硅与水化合制得
下列物质间的转化,能通过化合反应一步直接实现的是( )
A . S→SO3
B . Fe→FeCl3
C . Na2CO3→Na2SiO3
D . SiO2→H2SiO3
高纯硅广泛应用于信息技术和新能源技术等领域。一种高纯硅的制备工艺流程如下,下列说法正确的是( )
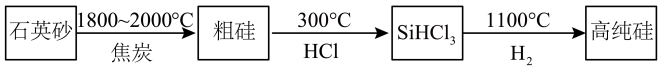
A . 石英砂的主要成分是硅酸盐
B . 加入焦炭发生的化学方程式为: C . 高纯硅的制备发生的反应是
C . 高纯硅的制备发生的反应是 D . 二氧化硅是酸性氧化物,能与水反应生成硅酸
D . 二氧化硅是酸性氧化物,能与水反应生成硅酸
 C . 高纯硅的制备发生的反应是
C . 高纯硅的制备发生的反应是 D . 二氧化硅是酸性氧化物,能与水反应生成硅酸
D . 二氧化硅是酸性氧化物,能与水反应生成硅酸
最近更新



