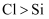碘与人体健康 知识点题库
-
(1) 日本9级大地震导致的福岛核泄漏,引起了人们核辐射恐慌,大量抢购碘片.此次泄露的物质之一为放射性的131I,一旦被人体吸入会引发甲状腺疾病,服用含稳定性碘的碘片能阻断90%放射性碘在甲状腺内的沉积.但世界卫生组织指出碘片防辐射效果有限且用碘需遵医嘱.碘是人体生命活动的必需元素,根据人体中含量属于 ,过多摄入有可能引发 疾病.
-
(2)
食品安全(food safety)指食品无毒、无害,符合应当有的营养要求,对人体健康不造成任何急性、亚急性或者慢性危害.“双汇瘦肉精事件”和“染色馒头事件”的发生,引起了民众对食品安全的担忧.
①瘦肉精,学名盐酸克伦特罗,其结构为
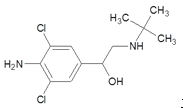 其分子式为 ,该物质能发生
其分子式为 ,该物质能发生 A.水解反应 B.消去反应 C.加成反应 D.酯化反应 E.加聚反应
②食品添加剂是指用于改善食品品质、延长食品保存期、便于食品加工和增加食品营养成分的一类化学合成或天然物质.上海多家超市出售染色馒头 被曝随意加化学药品.在玉米馒头的标签上,消费者能看到白砂糖和维生素C,可实际上,添加了甜蜜素、山梨酸钾、柠檬黄等物质.它们分别属于哪一类添加剂,甜蜜素 、山梨酸钾 、柠檬黄 .
配料表 | 精制海盐、碘酸钾(KIO3) |
含碘量 | 20~40mg/kg |
储藏方法 | 密封避光、防潮 |
食用方法 | 烹调时待食品熟后加入碘盐 |
-
(1) 碘酸钾属于哪类物质? (填:“纯净物”、“混合物”、“单质”、“氧化物”).
-
(2) 根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时
-
(3) 我国规定,食盐含碘量为每千克食盐含碘0.035克,相当于每千克食盐含碘酸钾 克.
请回答下列问题:
-
(1) 成人如果长期缺碘,会引起的病症是 (填字母).
A.佝偻病 B.甲状腺肿大 C.夜盲症
-
(2) 在瘦肉、胡萝卜、海带中,富含碘元素的是
-
(3) 用盐酸酸化的碘化钾淀粉溶液可检验食盐中是否含有碘酸钾,反应的化学方程式为:5KI+KIO3+6HCl═6KCl+3I2+3H2O则此反应中的氧化剂是 (填化学式),检验加碘盐时可观察到的实验现象是
-
(1) 有些学生从小偏食,不爱吃水果、蔬菜造成营养缺乏、发育不良,这主要是由于摄取的(选填脂肪、维生素或蛋白质)不足引起的.
-
(2) 生活中应合理地摄取人体必需的元素,体内元素不足会引起甲状腺肿疾病.
-
(3) 糖类、油脂和蛋白质都是人体所必需的营养物质,等质量的上述物质提供能量最多的是;蛋白质最终在人体人转化为;请写出葡萄糖在人体内发生氧化反应的化学方程式:.
①Cl2——做消毒剂 ②AgBr——制胶卷,感光纸 ③AgI——人工降雨
④加碘食盐——预防甲状腺肿大 ⑤淀粉——检验I2的存在 ⑥NaClO——漂白纺织物
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 加CCl4 , 振荡、静置 | 上层溶液显紫色 | 原溶液中有I2 |
| C | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| D | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
回答下列问题:
-
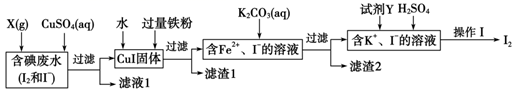
(1) 检验含碘废水中是否含有I2 , 常用的试剂是。
-
(2) X是一种常见的有刺激性气味的气体,通入X气体的主要目的是。
-
(3) 分离滤渣1各成分最简便的方法是;滤渣2在潮湿的空气中能被氧化为红褐色物质,故发生反应的化学方程式为。
-
(4) 试剂Y是一种绿色氧化剂,其化学式为;操作I包括。
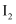 C .
C . 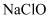 的水溶液可用于防疫消毒
D . 用灼烧并闻气味的方法区别纯棉织物和纯毛织物
的水溶液可用于防疫消毒
D . 用灼烧并闻气味的方法区别纯棉织物和纯毛织物
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度,将水样与 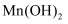 碱性悬浊液(含有
碱性悬浊液(含有 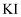 )混合,反应生成
)混合,反应生成 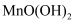 ,实现氧的固定。
,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化, 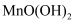 被
被 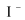 还原为
还原为  ,在暗处静置
,在暗处静置  ,然后用标准
,然后用标准  溶液滴定,生成的
溶液滴定,生成的 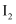 反应为:
反应为:  。
。
回答下列问题:
-
(1) 取水样时应尽量避免扰动水体表面,这样操作的主要目的是。
-
(2) “氧的固定”中发生反应的化学方程式为。
-
(3)
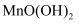 被
被  还原为
还原为  的离子反应方程式。
的离子反应方程式。
-
(4) 取
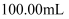 水样经固氧、酸化后,用
水样经固氧、酸化后,用  溶液滴定,以淀粉溶液作指示剂,终点现象为.若消耗
溶液滴定,以淀粉溶液作指示剂,终点现象为.若消耗  溶液的体积为
溶液的体积为 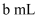 ,则水样中溶解氧的含量为
,则水样中溶解氧的含量为 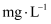 。
。
-
(5) 上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏(填“高”或“低”)。
配料表
| 氯化钠(NaCl) | ≥98 0%(以NaCl计) |
| 酸钾(KIO3) | (35土15)m g/kg (以I计) |

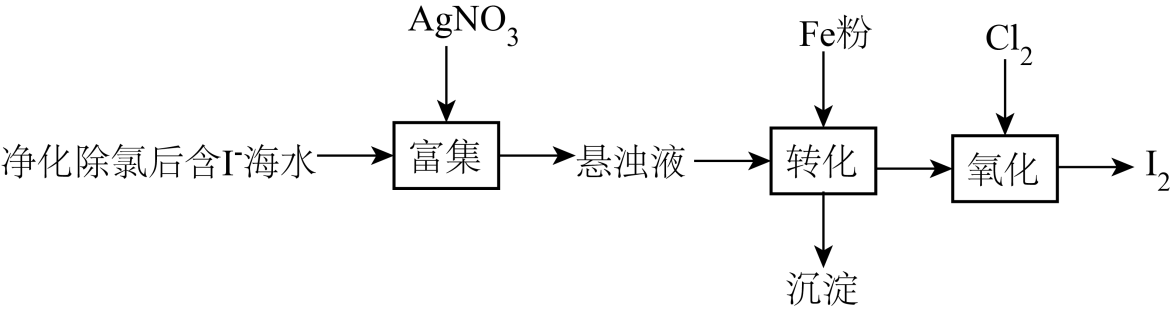
下列说法正确的是:( )
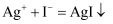 B . 转化反应为
B . 转化反应为 , 说明
, 说明 的还原性大于
的还原性大于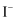 C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
选项 | 实验操作 | 现象 | 结论 |
A | 向 |
|
|
B | 向含有 | 产生白色沉淀 |
|
C | 将稀盐酸滴入硅酸钠溶液中,充分振荡 | 产生白色沉淀 | 非金属性: |
D | 向某食盐溶液中滴加淀粉溶液 | 溶液不变色 | 该食盐不是加碘盐 |
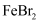 溶液中加入少量氯水,再加
溶液中加入少量氯水,再加 萃取
萃取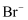 的
的 的
的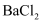 溶液中通入气体
溶液中通入气体