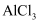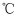金属冶炼的一般原理 知识点题库
化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中正确的是 ( )
A . 氯碱工业中阳极得到氢氧化钠和氢气
B . 电镀铜时,电镀液中c(Cu2+)基本保持不变
C . 工业上用电解熔融态氧化镁的方法得到金属镁
D . 海水中含有钾元素,只需经过物理变化就可以得到钾单质
下列制备金属单质的方法或原理正确的是( )
A . 在高温条件下,用H2还原MgO制备单质Mg
B . 在通电条件下,电解熔融Al2O3制备单质Al
C . 在通电条件下,电解饱和食盐水制备单质Na
D . 加强热,使CuO在高温条件下分解制备单质Cu
下列各工业生产中,石灰石、生石灰、熟石灰都不能作为原料的是( )
①炼铁 ②用生铁炼钢 ③从海水中提取镁 ④铝的冶炼 ⑤制水泥 ⑥制玻璃 ⑦制漂白粉 ⑧制硫酸
A . ④⑧
B . ⑤⑥
C . ①②③
D . ⑤⑥⑦
物质的用途错误的是( )
A . 草酸可用于提炼稀有金属
B . 苯酚可用于制造酚醛树脂
C . 浓硫酸可用于实验室制取HCl(g)
D . 氯化铵溶液可用于除去金属表面油污
下列说法正确的是( )
A . 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收
B . 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
C . 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛
D . 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同
化学与生产、生活密切相关.下列叙述错误的是( )
A . 光导纤维遇强碱会“断路”
B . 从海带中提取碘的过程涉及氧化还原反应
C . 钠可把钛、锆、铌、钽等金属从其熔融卤化物里还原出来
D . 绿色化学的核心是应用化学原理对环境污染进行治理
下列金属冶炼的反应原理,错误的是( )
A . 2NaCl(熔融)  2Na+Cl2↑
B . MgO+H2
2Na+Cl2↑
B . MgO+H2  Mg+H2O
C . Fe3O4+4CO
Mg+H2O
C . Fe3O4+4CO  3FeO+4CO2
D . 2HgO
3FeO+4CO2
D . 2HgO  2Hg+O2↑
2Hg+O2↑
 2Na+Cl2↑
B . MgO+H2
2Na+Cl2↑
B . MgO+H2  Mg+H2O
C . Fe3O4+4CO
Mg+H2O
C . Fe3O4+4CO  3FeO+4CO2
D . 2HgO
3FeO+4CO2
D . 2HgO  2Hg+O2↑
2Hg+O2↑
工业上用铝土矿(主要成分为Al2O3 , 含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )

A . 试剂X可以是氢氧化钠溶液,也可以是盐酸
B . 反应①、过滤后所得沉淀为氢氧化铁
C . 图中所示转化反应都不是氧化还原反应
D . 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
下列说法正确的是( )
A . 侯氏制碱法的原理是将CO2通入氨的NaCl饱和溶液中,使 NaHCO3析出, NaHCO3受热分解生成Na2CO3 , NaHCO3和Na2CO3在食品工业上都有着广泛的应用
B . 石灰乳与海水混合,过滤得Mg(OH)2 , 将其溶于盐酸,再蒸发结晶得到MgCl2 , 电解熔融MgCl2可得到金属镁
C . 利用2Al+4BaO  3Ba+Ba(AlO2)2可制取Ba,是因为铝的还原性强于钡
D . 陶瓷、砖瓦、玻璃、水泥都是重要的硅酸盐产品,其制备过程中都需要石灰石做原料
3Ba+Ba(AlO2)2可制取Ba,是因为铝的还原性强于钡
D . 陶瓷、砖瓦、玻璃、水泥都是重要的硅酸盐产品,其制备过程中都需要石灰石做原料
 3Ba+Ba(AlO2)2可制取Ba,是因为铝的还原性强于钡
D . 陶瓷、砖瓦、玻璃、水泥都是重要的硅酸盐产品,其制备过程中都需要石灰石做原料
3Ba+Ba(AlO2)2可制取Ba,是因为铝的还原性强于钡
D . 陶瓷、砖瓦、玻璃、水泥都是重要的硅酸盐产品,其制备过程中都需要石灰石做原料
下列描述中,不符合生产实际的是( )
A . 电解熔融的氧化铝制取金属铝
B . 在镀件上电镀锌,用锌作阳极
C . 电解法精炼粗铜,用纯铜作阳极
D . 电解饱和食盐水制烧碱,阳极室产生氯气
工业上以钒钛磁铁矿为原料,在炼铁的同时还可以制备钒的最高价氧化物V2O5 , 其主要流程如下:

已知:①VO3-+2H+  VO2++H2O
VO2++H2O
②NH4VO3微溶于冷水,易溶于热水,不溶于乙醇
-
(1) 高炉炼铁应用的冶炼方法是_______(填标号)A . 热分解法 B . 热还原法 C . 电解法
-
(2) 钒渣中的V2O3在焙烧时转化为Ca(VO3)2 , 写出该反应的化学方程式。
-
(3) Ca(VO3)2难溶于水但能溶于稀硫酸,试用平衡移动原理分析其原因,浸出液中含钒物质的化学式为。
-
(4) 沉钒过程有气体生成,其反应的离子方程式为。
-
(5) 过滤后用乙醇代替水来洗涤沉淀的原因是。
-
(6) 煅烧NH4VO3时,固体质量随温度变化的曲线如图所示。加热到200℃时,得到的固体物质化学式为,300~350℃放出的气态物质化学式为。

化学在金属矿物和海水资源的开发利用过程中具有重要的意义和作用。按要求回答下列问题。
-
(1) 在工业生产中金属冶炼的原理错误的是
A 电解熔融的 NaCl 来制取 Na
B 电解熔融的 AlCl3 来制取 Al
C CO 还原 Fe2O3 制取 Fe
D 铝热反应原理制锰:4Al+3MnO2
 3Mn+2 Al2O3
3Mn+2 Al2O3 -
(2) 下图是从海水中提取溴的简单流程:

提取溴的过程中,经过 2 次 Br-
 Br2 转化的目的是
Br2 转化的目的是 -
(3) 吸收塔中发生反应的离子方程式是
-
(4) 海带中富含碘元素,实验室从海带中提取 I2 的途径如下图所示:

①步骤 I 灼烧海带至灰烬时所用的主要仪器名称是 。
②步骤 IV 向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式 。
③步骤 V 加入萃取剂 M 为 ,步骤 VI 从 I2 的有机溶液获得 I2 可以用 的方法。
下列冶炼方法错误的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。B是形成化合物种类最多的元素,A、C能形成两种液态化合物  和
和  。C、F同主族,D元素在同周期中原子半径最大。E元素的周期序数与主族序数相等。回答下列问题:
。C、F同主族,D元素在同周期中原子半径最大。E元素的周期序数与主族序数相等。回答下列问题:
 和
和  。C、F同主族,D元素在同周期中原子半径最大。E元素的周期序数与主族序数相等。回答下列问题:
。C、F同主族,D元素在同周期中原子半径最大。E元素的周期序数与主族序数相等。回答下列问题:
-
(1) G元素在周期表中的位置为,C、D、E三种元素的简单离子的半径由大到小顺序为(用离子符号表示)。
-
(2) 物质R由A、B两种元素组成,R的产量可以用来衡量一个国家的石油化工发展水平,则R的电子式为。将R通入溴的四氯化碳溶液中,发生反应的化学方程式为。
-
(3) M、N是由A、C、D、F四种元素组成的两种化合物,M、N溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:。
-
(4) E是一种用途很广的材料。工业上制备E的化学方程式为:,将E单质与氧化铁高温加热制取铁,制取1mol的铁转移的电子数为。
-
(5) 向
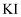 溶液中通入适量的G单质后,再滴加一定量的CCl4 , 振荡静置后的现象为,该反应的离子方程式为。
溶液中通入适量的G单质后,再滴加一定量的CCl4 , 振荡静置后的现象为,该反应的离子方程式为。
下列金属的冶炼方法与工业上冶炼铝的方法相同的是( )
A . Fe2O3+3CO  2Fe+3CO2
B . 2Ag2O
2Fe+3CO2
B . 2Ag2O  4Ag+O2↑
C . Fe+CuSO4=FeSO4+Cu
D . 2NaCl(熔融)
4Ag+O2↑
C . Fe+CuSO4=FeSO4+Cu
D . 2NaCl(熔融)  2Na+Cl2↑
2Na+Cl2↑
 2Fe+3CO2
B . 2Ag2O
2Fe+3CO2
B . 2Ag2O  4Ag+O2↑
C . Fe+CuSO4=FeSO4+Cu
D . 2NaCl(熔融)
4Ag+O2↑
C . Fe+CuSO4=FeSO4+Cu
D . 2NaCl(熔融)  2Na+Cl2↑
2Na+Cl2↑
下列关于资源综合利用的说法错误的是( )
A . 煤的气化、液化都是化学过程,可得到清洁的燃料和多种化工原料
B . 苯最初是在煤气灯中发现的,但苯主要是由石油催化重整得到的
C . 工业上常利用Al与Fe2O3在高温下的反应大量冶炼Fe单质
D . 从海水中提取溴和碘都必须经过氧化反应
下列变化过程不属于金属冶炼的是( )
A . 电解氧化铝
B . 铁在氧气中燃烧
C . 金属氧化物与焦炭在高温下反应
D . 高温下CO还原CuO
钛(  )及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为
)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为  ,含少量V、
,含少量V、 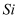 和
和 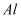 的氧化物杂质)为原料,制备金属钛的工艺流程如下:
的氧化物杂质)为原料,制备金属钛的工艺流程如下:
 )及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为
)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为  ,含少量V、
,含少量V、 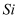 和
和 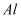 的氧化物杂质)为原料,制备金属钛的工艺流程如下:
的氧化物杂质)为原料,制备金属钛的工艺流程如下:

已知“降温收尘”后,粗  中含有的几种物质的沸点:
中含有的几种物质的沸点:
|
物质 |
|
|
|
|
|
沸点/ |
136 |
127 |
57 |
180 |
回答下列问题:
-
(1) 已知
 ,
, 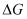 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略  、
、 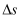 随温度的变化。若
随温度的变化。若 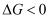 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断:  时,下列反应不能自发进行的是______________。
时,下列反应不能自发进行的是______________。
 A .
A .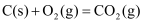 B .
B . 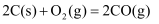 C .
C .  D .
D . 
-
(2)
 与C、
与C、  在
在  的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
物质


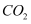

分压/





①该温度下,
 与C、
与C、  反应的总化学方程式为;
反应的总化学方程式为;②随着温度升高,尾气中
 的含量升高,原因是。
的含量升高,原因是。 -
(3) “除钒”过程中的化学方程式为;“除硅、铝”过程中,分离
 中含
中含  、
、 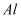 杂质的方法是。
杂质的方法是。
-
(4) “除钒”和“除硅、铝”的顺序(填“能”或“不能”)交换,理由是。
-
(5) 下列金属冶炼方法与本工艺流程中加入
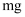 冶炼
冶炼  的方法相似的是______________。
A . 高炉炼铁 B . 电解熔融氯化钠制钠 C . 铝热反应制锰 D . 氧化汞分解制汞
的方法相似的是______________。
A . 高炉炼铁 B . 电解熔融氯化钠制钠 C . 铝热反应制锰 D . 氧化汞分解制汞
化学要研究如何合理、高效地利用金属矿物。下列金属的冶炼方法与工业上冶炼铝相同的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列说法正确的是( )
A . 工业上镁、铝都是用电解其熔融氯化物制得
B . 可利用铝热反应冶炼铁、铬、锰、钴等高熔点金属
C . 蛋白质、油脂、糖类均能发生水解反应
D . 煤的干馏指将煤在空气中加强热使之分解的过程,工业上也叫做煤的焦化
最近更新