еҢ–еӯҰз”өжәҗж–°еһӢз”өжұ зҹҘиҜҶзӮ№йўҳеә“
й«ҳй“Ғз”өжұ жҳҜдёҖз§Қж–°еһӢеҸҜе……з”өз”өжұ пјҢдёҺжҷ®йҖҡй«ҳиғҪз”өжұ зӣёжҜ”пјҢиҜҘз”өжұ иғҪй•ҝж—¶й—ҙдҝқжҢҒзЁіе®ҡзҡ„ж”ҫз”өз”өеҺӢгҖӮй«ҳй“Ғз”өжұ зҡ„жҖ»еҸҚеә”дёәпјҡ3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOHпјҢдёӢеҲ—еҸҷиҝ°дёҚжӯЈзЎ®зҡ„жҳҜ
3Zn(OH)2+2Fe(OH)3+4KOHпјҢдёӢеҲ—еҸҷиҝ°дёҚжӯЈзЎ®зҡ„жҳҜ
пјҲ1пјүе®ҢжҲҗдёӢеҲ—е…ідәҺз”Ізғ·пјҲCH4пјүзҮғж–ҷз”өжұ зҡ„еЎ«з©әпјҡ
в‘ з”Ізғ·дёҺж°§ж°”еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡ
в‘Ўе·ІзҹҘзҮғж–ҷз”өжұ зҡ„жҖ»еҸҚеә”ејҸдёәCH4+2O2+2KOHв•җK2CO3+3H2OпјҢз”өжұ дёӯжңүдёҖжһҒзҡ„з”өжһҒеҸҚеә”дёәCH4+10OHп№Јп№Ј8eп№Јв•җCO32п№Ј+7H2OпјҢиҝҷдёӘз”өжһҒжҳҜзҮғж–ҷз”өжұ зҡ„ пјҲеЎ«вҖңжӯЈжһҒвҖқжҲ–вҖңиҙҹжһҒвҖқпјүпјҢеҸҰдёҖдёӘз”өжһҒдёҠзҡ„з”өжһҒеҸҚеә”ејҸдёәпјҡ
в‘ўйҡҸзқҖз”өжұ дёҚж–ӯж”ҫз”өпјҢз”өи§ЈиҙЁжә¶ж¶Ізҡ„зўұжҖ§ пјҲеЎ«вҖңеўһеӨ§вҖқгҖҒвҖңеҮҸе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқпјү
в‘ЈйҖҡеёёжғ…еҶөдёӢпјҢз”Ізғ·зҮғж–ҷз”өжұ зҡ„иғҪйҮҸеҲ©з”ЁзҺҮ пјҲеЎ«вҖңеӨ§дәҺвҖқгҖҒвҖңе°ҸдәҺвҖқжҲ–вҖңзӯүдәҺвҖқпјүз”Ізғ·зҮғзғ§зҡ„иғҪйҮҸеҲ©з”ЁзҺҮпјҺ
пјҲ2пјүжҚ®жҠҘйҒ“пјҢжңҖиҝ‘ж‘©жүҳзҪ—жӢүпјҲMOTOROLAпјүе…¬еҸёз ”еҸ‘дәҶдёҖз§Қз”ұз”ІйҶҮе’Ңж°§ж°”д»ҘеҸҠејәзўұеҒҡз”өи§ЈиҙЁжә¶ж¶Ізҡ„ж–°еһӢжүӢжңәз”өжұ пјҢз”өйҮҸжҳҜзҺ°з”Ёй•Қж°ўз”өжұ е’Ңй”Ӯз”өжұ зҡ„10еҖҚпјҢеҸҜиҝһз»ӯдҪҝз”Ё1дёӘжңҲе……з”өдёҖж¬ЎпјҺеҒҮе®ҡж”ҫз”өиҝҮзЁӢдёӯпјҢз”ІйҶҮе®Ңе…Ёж°§еҢ–дә§з”ҹзҡ„CO2иў«е……еҲҶеҗёж”¶з”ҹжҲҗCO32п№Ј
в‘ иҜҘз”өжұ еҸҚеә”зҡ„жҖ»зҰ»еӯҗж–№зЁӢејҸдёә
в‘Ўз”ІйҶҮеңЁ жһҒеҸ‘з”ҹеҸҚеә”пјҲеЎ«жӯЈжҲ–иҙҹпјүпјҢз”өжұ еңЁж”ҫз”өиҝҮзЁӢдёӯжә¶ж¶Ізҡ„pHе°Ҷ пјҲеЎ«йҷҚдҪҺжҲ–дёҠеҚҮгҖҒдёҚеҸҳпјүпјҺ
|
|
|
|
В AпјҺй”Ңй”°з”өжұ | В BпјҺж°ўж°§зҮғж–ҷз”өжұ | В CпјҺй“…и“„з”өжұ | В DпјҺй•Қй•үз”өжұ |
 В В CdпјҲOHпјү2+2NiпјҲOHпјү2 пјҢ дёӢеҲ—жңүе…ій•Қй•үз”өжұ зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В пјү
В В CdпјҲOHпјү2+2NiпјҲOHпјү2 пјҢ дёӢеҲ—жңүе…ій•Қй•үз”өжұ зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲВ В пјү


 CdпјҲOHпјү2+2NiпјҲOHпјү2жңүе…іиҜҘз”өжұ зҡ„иҜҙжі•жӯЈзЎ®зҡ„пјҲ пјү
CdпјҲOHпјү2+2NiпјҲOHпјү2жңүе…іиҜҘз”өжұ зҡ„иҜҙжі•жӯЈзЎ®зҡ„пјҲ пјү

 2Al(OH)3вҶ“+3Cl2вҶ‘+3H2вҶ‘
C . еӣҫ1дёӯз”өи§ЈиҙЁжә¶ж¶Ізҡ„pHеўһеӨ§
D . еӣҫ1дёӯзҡ„a з”өжһҒеҸҚеә”ејҸдёәпјҡCH4-8e-+8OH-=CO2+6H2O
2Al(OH)3вҶ“+3Cl2вҶ‘+3H2вҶ‘
C . еӣҫ1дёӯз”өи§ЈиҙЁжә¶ж¶Ізҡ„pHеўһеӨ§
D . еӣҫ1дёӯзҡ„a з”өжһҒеҸҚеә”ејҸдёәпјҡCH4-8e-+8OH-=CO2+6H2O
-
пјҲ1пјү жұҪиҪҰеҸ‘еҠЁжңәе·ҘдҪңж—¶дјҡеј•еҸ‘N2е’ҢO2еҸҚеә”з”ҹжҲҗNOпјҢе…¶еҸҚеә”иҝҮзЁӢдёӯзҡ„иғҪйҮҸеҸҳеҢ–еҰӮдёӢпјҡ
еҸҚеә”
N2(g)вҶ’2N(g)
O2(g)вҶ’2O(g)
N(g)пјӢO(g)вҶ’NO(g)
еҸҚеә”зғӯ
в–іH1
в–іH2
в–іH3
зғӯйҮҸеҖјkJ/mol
945
498
630
в‘ в–іH10пјҢв–іH30гҖӮпјҲеЎ«вҖң>вҖқжҲ–вҖң<вҖқпјү
в‘ЎN2пјҲgпјү+O2пјҲgпјү=2NOпјҲgпјүв–іH=kJВ·mol-1гҖӮ
-
пјҲ2пјү еҲ©з”Ёз”Ізғ·еӮ¬еҢ–иҝҳеҺҹж°®ж°§еҢ–зү©гҖӮе·ІзҹҘпјҡ
CH4пјҲgпјү+4NO2пјҲgпјү=4NOпјҲgпјү+CO2пјҲgпјү+2H2OпјҲgпјүв–іH=-574kJВ·mol-l
CH4пјҲgпјү+4NOпјҲgпјү=2N2пјҲgпјү+CO2пјҲgпјү+2H2OпјҲgпјүAH=-1160 kJВ·mol-l
H2OпјҲlпјү=H2OпјҲgпјүв–іH=+44kJВ·mol-l
CH4дёҺNO2еҸҚеә”з”ҹжҲҗN2е’ҢH2O(l)зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸдёәгҖӮ
-
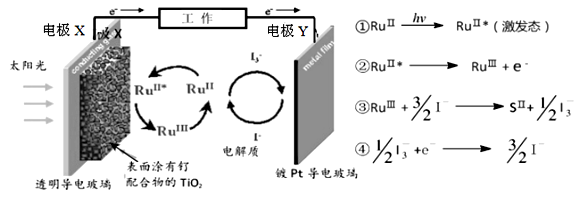
пјҲ3пјү жҪңиүҮдёӯдҪҝз”Ёзҡ„ж¶Іж°®-ж¶Іж°§зҮғж–ҷз”өжұ е·ҘдҪңеҺҹзҗҶеҰӮеӣҫжүҖзӨәпјҡ

в‘ з”өжһҒaеҗҚз§°жҳҜгҖӮ
в‘Ўз”өи§ЈиҙЁжә¶ж¶ІдёӯOH-зҰ»еӯҗеҗ‘移еҠЁпјҲеЎ«вҖңз”өжһҒaвҖқжҲ–вҖңз”өжһҒbвҖқпјүгҖӮ
в‘ўз”өжһҒbзҡ„з”өжһҒеҸҚеә”ејҸдёәгҖӮ
-
пјҲ4пјү еҸҜйҖҡиҝҮNH3дёҺNaClOеҸҚеә”жқҘеҲ¶еҫ—зҒ«з®ӯзҮғж–ҷиӮјпјҲN2H4пјүгҖӮиҜҘеҸҚеә”зҡ„еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸжҳҜгҖӮ


иҜ·еӣһзӯ”пјҡ
-
пјҲ1пјү з”Іжұ жҳҜжұ пјҢйҖҡе…ҘO2зҡ„дёҖжһҒз”өжһҒеҸҚеә”ејҸдёәпјҢиҜҘз”өжұ зҡ„жҖ»еҸҚеә”ж–№зЁӢејҸдёәгҖӮ
-
пјҲ2пјү д№ҷжұ дёӯAз”өжһҒеҗҚз§°дёәжһҒпјҢз”өжһҒеҸҚеә”ејҸдёәгҖӮдёҖж®өж—¶й—ҙеҗҺжә¶ж¶Ізҡ„pH(еЎ«вҖңеўһеӨ§вҖқгҖҒвҖңеҮҸе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқ)гҖӮ
-
пјҲ3пјү еҪ“д№ҷжұ дёӯB(Ag)жһҒзҡ„иҙЁйҮҸеўһеҠ 5.40 gж—¶пјҢз”Іжұ дёӯзҗҶи®әдёҠж¶ҲиҖ—O2mL(ж ҮеҮҶзҠ¶еҶөдёӢ)гҖӮ


-
пјҲ1пјү з”Ізғ·ж°ҙи’ёж°”еӮ¬еҢ–йҮҚж•ҙжҳҜеҲ¶еӨҮй«ҳзәҜж°ўзҡ„ж–№жі•д№ӢдёҖпјҢе·ІзҹҘеңЁеҸҚеә”еҷЁдёӯеӯҳеңЁеҰӮдёӢеҸҚеә”иҝҮзЁӢпјҡ
в… .

в…Ў.

ж №жҚ®дёҠиҝ°дҝЎжҒҜиҜ·еҶҷеҮәз”Ізғ·ж°ҙи’ёж°”еӮ¬еҢ–йҮҚж•ҙзҡ„зғӯеҢ–еӯҰеҸҚж–№зЁӢејҸпјҡ
гҖӮ
-
пјҲ2пјү жҹҗж°ўж°§зҮғж–ҷз”өжұ д»ҘзҶ”иһҚжҖҒзҡ„зўій…ёзӣҗдёәз”өи§ЈиҙЁпјҢе…¶дёӯ
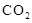 еҸӮдёҺз”өжһҒеҸҚеә”гҖӮе·ҘдҪңж—¶иҙҹжһҒзҡ„з”өжһҒеҸҚеә”дёә
еҸӮдёҺз”өжһҒеҸҚеә”гҖӮе·ҘдҪңж—¶иҙҹжһҒзҡ„з”өжһҒеҸҚеә”дёә  гҖӮеҰӮеӣҫжүҖзӨәпјҢж №жҚ®зӣёе…ідҝЎжҒҜеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
гҖӮеҰӮеӣҫжүҖзӨәпјҢж №жҚ®зӣёе…ідҝЎжҒҜеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
в‘ жӯЈжһҒзҡ„з”өжһҒеҸҚеә”дёәпјӣ
в‘ЎеҪ“з”Іжұ дёӯAз”өжһҒзҗҶи®әдёҠж¶ҲиҖ—H2зҡ„дҪ“з§Ҝдёә448 mLпјҲж ҮеҮҶзҠ¶еҶөпјүж—¶пјҢд№ҷжұ дёӯCгҖҒDдёӨз”өжһҒиҙЁйҮҸеҸҳеҢ–йҮҸд№Ӣе·®дёәgгҖӮ

 +2e-=Zn+4OH-
B . е……з”өж—¶пјҢй”ҢжқҝдҪңдёәйҳҙжһҒпјҢй”Ңжқҝйҷ„иҝ‘жә¶ж¶ІзўұжҖ§еўһејә
C . з”өжұ дёӯзҰ»еӯҗдәӨжҚўиҶңжҳҜйҳізҰ»еӯҗдәӨжҚўиҶң
D . ж”ҫз”өж—¶пјҢжҜҸж¶ҲиҖ—22.4 mLO2 пјҢ еӨ–з”өи·ҜиҪ¬з§»з”өеӯҗж•°зәҰдёә2.408Г—1021дёӘ
+2e-=Zn+4OH-
B . е……з”өж—¶пјҢй”ҢжқҝдҪңдёәйҳҙжһҒпјҢй”Ңжқҝйҷ„иҝ‘жә¶ж¶ІзўұжҖ§еўһејә
C . з”өжұ дёӯзҰ»еӯҗдәӨжҚўиҶңжҳҜйҳізҰ»еӯҗдәӨжҚўиҶң
D . ж”ҫз”өж—¶пјҢжҜҸж¶ҲиҖ—22.4 mLO2 пјҢ еӨ–з”өи·ҜиҪ¬з§»з”өеӯҗж•°зәҰдёә2.408Г—1021дёӘ









