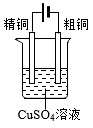
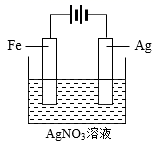
电镀 知识点题库
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
A . 锌作阳极,镀件作阴极,溶液中含有锌离子
B . 铂作阴极,镀件作阳极,溶液中含有锌离子
C . 铁作阳极,镀件作阴极,溶液中含有亚铁离子
D . 锌用阴极,镀件作阳极,溶液中含有锌离子
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。 请回答:

-
(1) B极是电源的极,C极的电极反应式为,一段时间后丁中X极附近的颜色逐渐。(填“变深”或者“变浅”)
-
(2) 若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
-
(3) 现用丙装置给铜件镀银,则H应该是 (填“铜”或“银”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 g,甲中溶液的pH (填“变大”、“变小”或“不变”)。
-
(4) 若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差5.12g,则电镀时电路中通过的电子为mol
下列关于铜电极的叙述中错误的是( )
A . 锌铜原电池铜是正极
B . 在镀件上镀铜时可用金属铜做阳极
C . 用电解法精炼粗铜时粗铜做阴极
D . 用电解法精炼粗铜时,Cu2+移向纯铜电极
下列描述中,不符合生产实际的是( )
A . 电解熔融的氧化铝制取金属铝
B . 在镀件上电镀锌,用锌作阳极
C . 电解法精炼粗铜,用纯铜作阳极
D . 电解饱和食盐水制烧碱,阳极室产生氯气
某小组用如图装置摸拟电镀铜和精炼铜。下列说法错误的是( )

A . 精炼铜时,X电极是粗铜,比铜活波的金属最终变成阳极泥
B . 电镀铜时,Y电极为待镀的金属制品
C . 电镀铜和精炼铜时,Y上的电极反应都是: Cu2++2e-= Cu
D . 电镀铜时,X电极是铜,溶液中的Cu2+浓度保持不变
下列叙述错误的是( )
A . NaHCO3、Fe(OH)3、FeCl2均可通过化合反应生成
B . 电解、电离、电镀均需要通电才可进行
C . CO2、N2O5、SO2均为酸性氧化物
D . 水玻璃、淀粉溶液、胶体均为混合物
下列实验装置符合实验目的是( )
| 目的 | 粗铜的精炼 | 验证NaCl溶液(含酚酞)的产物 | 在铁制品上镀铜 | 构成原电池 |
| 装置 | | | | |
| 选项 | A | B | C | D |
A . A
B . B
C . C
D . D
若要在铁钉上镀铜,下列设计正确的是( )
| 选项 | 接电源正极 | 接电源负极 | 电解质溶液 |
| A | Cu | Fe | CuSO4溶液 |
| B | Cu | Fe | FeSO4溶液 |
| C | Fe | Cu | CuSO4溶液 |
| D | Fe | Cu | FeSO4溶液 |
A . A
B . B
C . C
D . D
下列描述中不符合生产实际的是( )
A . 电解水制氢气时,用铜作阳极
B . 电解法精炼粗铜,用纯铜作阴极
C . 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D . 在镀件上电镀锌,用锌作阳极
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
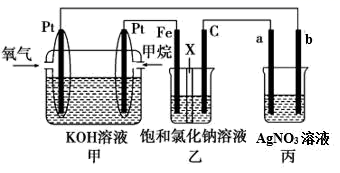
请按要求回答相关问题:
-
(1) 甲烷燃料电池负极电极反应式是:。
-
(2) 乙中X是交换膜,工作一段时间后若要恢复成原溶液,应。
-
(3) 欲用丙装置给铜镀银,b应是(填化学式)。
-
(4) 若乙池中的饱和氯化钠溶液换成一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为mol。(忽略溶液体积的变化)
-
(5) 通过膜电池可除去废水中的乙酸钠和对氯苯酚(
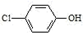 ),其原理如图所示,A极的电极反应为。
),其原理如图所示,A极的电极反应为。 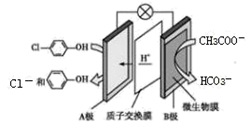
-
(6) 化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3-的原理如图所示。
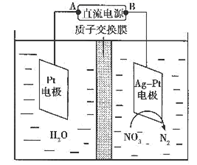
①Ag-Pt电极上的电极反应式为。
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为g。
以下是中学化学常见的四个装置,下列关于这些装置说法正确的是( )
A . 装置在使用过程中,电池内部电子从Ag2O 极通过隔板移向锌粉  B . 装置在使用过程中,电池外壳会逐渐变薄,容易出现漏液
B . 装置在使用过程中,电池外壳会逐渐变薄,容易出现漏液  C . 装置在使用过程中,电解质溶液的 pH 不会发生变化
C . 装置在使用过程中,电解质溶液的 pH 不会发生变化  D . 装置在使用过程中,阳极可以一直使用,不需要更换
D . 装置在使用过程中,阳极可以一直使用,不需要更换 
 B . 装置在使用过程中,电池外壳会逐渐变薄,容易出现漏液
B . 装置在使用过程中,电池外壳会逐渐变薄,容易出现漏液  C . 装置在使用过程中,电解质溶液的 pH 不会发生变化
C . 装置在使用过程中,电解质溶液的 pH 不会发生变化  D . 装置在使用过程中,阳极可以一直使用,不需要更换
D . 装置在使用过程中,阳极可以一直使用,不需要更换 
采用如图所示装置模拟工业生产。已知:钾离子交换摸只让钾离子通过分子及其它离子均不能通过。

回答下列问题:
-
(1) 若在A池中实现铁上镀铜,b电极的电极材料为。
-
(2) 若A池中a、b电极材料均为惰性电极,电解一段时间后,两极均有气体产生,则向溶液中加入(填化学式固体可以使溶液恢复到电解前的情况。
-
(3) B池中,c电极为极(填“正”或“负”),电极反应式为。
-
(4) 若在C池中用
 溶液制取
溶液制取  溶液和氯气,高浓度的
溶液和氯气,高浓度的  溶液从口出(填图中字母),当d电极消耗标准状况下
溶液从口出(填图中字母),当d电极消耗标准状况下  时,C池中阳极室溶液质量减少g。
时,C池中阳极室溶液质量减少g。
利用如图所示装置模拟电解原理在工业生产中的应用,下列说法正确的是( )
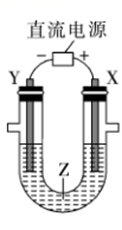
A . 氯碱工业中,X电极上的反应式是4OH--4e-=2H2O+O2↑
B . 电解精炼铜时,Z溶液中的Cu2+浓度不变
C . 在铁片上镀铜时,每转移2mol电子,Y极增重64g
D . 制取金属铝时,Z是熔融的氯化铝
下列实验能达到相应目的的是( )
| | | | |
| A.在铁上镀铜 | B.进行铝热反应 | C.蒸干 | D.证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 |
A . A
B . B
C . C
D . D
下列实验装置能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 电解饱和食盐水并检验气体 | 构成铜锌原电池 | 电解精炼铜 | 铁片镀银 |
A . A
B . B
C . C
D . D
下列关于实验现象的描述错误的是( )
A . 把Cu片和Fe片紧靠在一起浸入稀硫酸中,Cu片表面出现气泡
B . 用Zn片做阳极,Fe片做阴极,电解饱和ZnCl2溶液,Fe片表面出现一层锌
C . 把Cu片浸入FeCl3溶液中,在Cu片表面出现一层铁
D . 把Zn粒放入装有稀盐酸的试管中,加入几滴CuCl2溶液,放出气泡的速率减慢
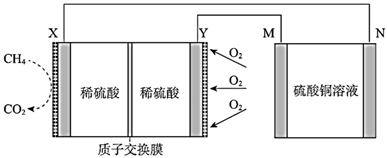
一种甲烷燃料电池的工作原理如图所示。
-
(1) X电极为(填“正极”或“负极”),该电极的电极反应式为。
-
(2) 放电过程中,
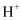 向(填“X极”或“Y极”)移动。
向(填“X极”或“Y极”)移动。
-
(3) 若用该燃料电池进行粗铜精炼,则M极连接的是(填“粗铜”或“精铜”),N极的电极反应式为。
-
(4) 若用该燃料电池进行电镀铜,则N极连接的是(填“镀件”或“精铜”),理论上每消耗
 甲烷时,M极变化(增加或减少)的质量为g。
甲烷时,M极变化(增加或减少)的质量为g。
下列有关电化学装置完全正确的是( )
|
|
|
|
A.铜上镀银 | B.电解法制钠 | C.牺牲阳极的阴极保护法保护铁 | D.铁的析氢腐蚀 |
A . A
B . B
C . C
D . D
下列关于铜电极的叙述中不正确的是( )
A . 锌铜原电池铜是正极
B . 在镀件上镀铜时可用金属铜做阳极
C . 用电解法精炼粗铜时粗铜做阴极
D . 用电解法精炼粗铜时,Cu2+移向纯铜电极
餐具表面镀银可达到增强抗腐蚀性、提升美观等目的。下列关于铁表面镀银的说法错误的是( )
A . 电路中每通过1mole- , 阴极析出1mol银
B . 铁电极应与电源负极相连
C . 阳极电极反应式为Ag﹣e- = Ag+
D . 电镀液需要不断更换
最近更新




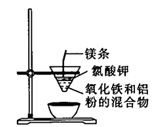
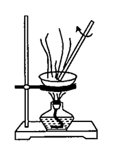
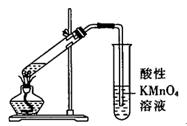
 溶液,制备
溶液,制备