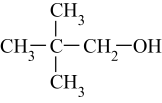
乙醇的消去反应 知识点题库
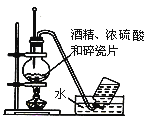 实验室用乙醇制取乙烯
B .
实验室用乙醇制取乙烯
B . 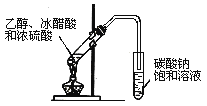 实验室制取乙酸乙酯
C .
实验室制取乙酸乙酯
C . 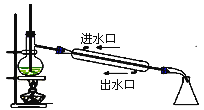 石油分馏
D .
石油分馏
D .  实验室制取硝基苯
实验室制取硝基苯
-
(1) 用下列仪器,以上述三种物质为原料制备1,2﹣二溴乙烷.如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去):
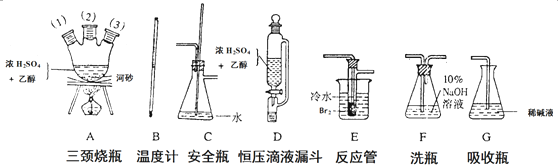
经A(1)插入A中, 接A(2);A(3)接C,C接 接 接G.
-
(2) 在三颈烧瓶A中的主要反应的化学方程式为
-
(3) 在反应管E中进行的主要反应的化学方程式为
-
(4) 温度计水银球的正确位置是
-
(5) 反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为
 CH2=CH2↑+H2O;接着再用液溴与乙烯反应制备1,2﹣二溴乙烷.在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2 , 并进而与Br2反应生成HBr等酸性气体.某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2﹣二溴乙烷
CH2=CH2↑+H2O;接着再用液溴与乙烯反应制备1,2﹣二溴乙烷.在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2 , 并进而与Br2反应生成HBr等酸性气体.某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2﹣二溴乙烷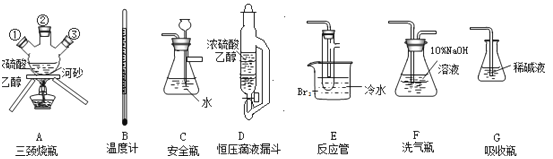
-
(1) )如果气体流向从左到右,正确的连接顺序是:B经A①插入A中,D接入②;A③接 接 接 接 接.
-
(2) 温度计水银球的正确位置是
-
(3) 装置D与分流漏斗相比,其主要优点是
-
(4) 装置C的主要作用是 ,装置F的作用是
-
(5) 在反应管E中进行的主要反应的化学方程式为
-
(6) 装置E烧杯中的泠水和反应管内液溴上的水层作用均是 .若将装置F拆除,在E中的主要反应为
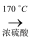 CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是( )
CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是( ) 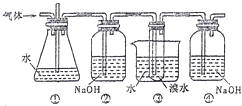
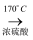 CH2=CH2↑+H2O,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O.
CH2=CH2↑+H2O,加热一段时间后溶液中有黑色现象出现.过一段时间后,经硫酸酸化的高锰酸钾溶液褪色.经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O. 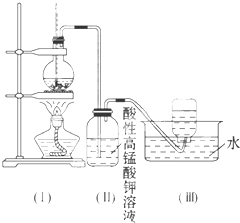
酸性高锰酸钾溶液褪色,甲同学认为能证明乙烯被酸性高锰酸钾溶液氧化了;乙同学认为不能证明乙烯被酸性高锰酸钾溶液氧化了.
-
(1) 你认为哪个同学的观点正确? (填“甲”或“乙”),理由是(从下列选项中选)
A.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了氧化反应
B.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了加成反应
C.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,不能证明通入的气体是纯净物
D.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,只能证明通入的气体一定具有还原性
-
(2) 丙同学取(Ⅱ)瓶中少量溶液于试管里,加入盐酸和氯化钡溶液,产生白色沉淀,他认为乙烯中一定混有二氧化硫,你认为他的结论是否可靠? (填“可靠”或“不可靠”);理由是.
-
(3) 丁同学想证明乙烯能否与溴发生反应,于是对上述实验进行了改进,改进的方法是:在装置(Ⅰ)和(Ⅱ)之间增加一个装有足量的洗气瓶,且将(Ⅱ)瓶中溶液换成.发生加成反应的化学方程式为.
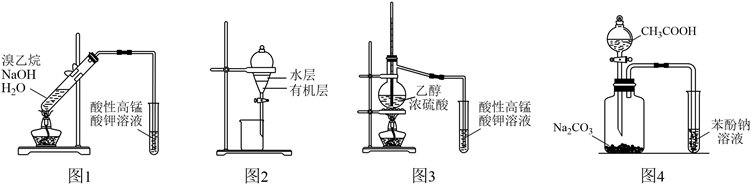
| 实验操作 | 实验目的 | |
| A | 将饱和食盐水滴加到电石中,将产生的气体通入溴水中 | 验证乙炔可与 Br2 发生了加成反应 |
| B | 乙醇与浓硫酸加热至 170℃,将产生的气体先通入NaOH 溶液,再通入 Br2 的 CCl4 溶液 | 检验产生的乙烯 |
| C | 将溴乙烷与 NaOH 乙醇溶液共热,将产生的气体通入酸性 KMnO4 溶液 | 检验产生的乙烯 |
| D | 向纯碱中滴加醋酸,将产生的气体通入苯酚钠浓溶液 | 证明酸性:醋酸>碳酸>苯酚 |
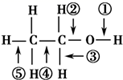
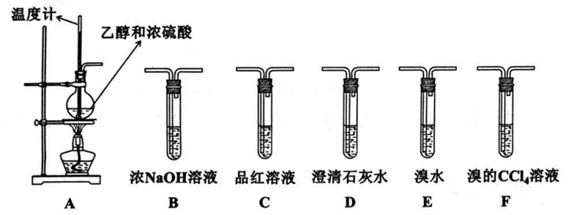
-
(1) A中发生反应的化学方程式为:.
-
(2) 加热混合液时,应迅速升温,否则会产生副产物(写结构简式).
-
(3) 若温度过高或加热时间过长,制得的乙烯中往往混有
 和
和  (假设不含其它杂质).为了确定气体的成分,请用上面给出的实验装置完成下列探究:
(假设不含其它杂质).为了确定气体的成分,请用上面给出的实验装置完成下列探究: ①若要证明混合气体中存在乙烯,可将混合气体依次通过
 ,则装置B的作用是,也可以直接将气体通入中(填装置代号,下同);
,则装置B的作用是,也可以直接将气体通入中(填装置代号,下同);②若要证明混合气体中存在
 ,可以将混合气体通入中
,可以将混合气体通入中③若要证明混合气体中存在
 ,则装置的连接顺序为→→D;
,则装置的连接顺序为→→D;④若要一次性将乙烯、
 、
、  全部检验出来,气体被检验的先后顺序为.
全部检验出来,气体被检验的先后顺序为.
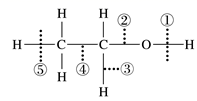
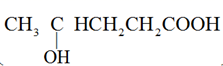 )在浓硫酸存在时加热,可得到分子式为
)在浓硫酸存在时加热,可得到分子式为  的有机物,该有机物不可能是( )
的有机物,该有机物不可能是( )
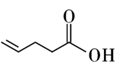 B .
B . 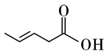 C .
C . 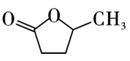
选项 | 实验操作及现象 | 结论 |
A | 将乙醇与浓硫酸的混合物加热至170℃,并将产生的气体干燥后通入少量溴的四氯化碳溶液中,溴的四氯化碳溶液褪色 | 乙醇发生了消去反应 |
B | 向淀粉溶液中先加入稀硫酸并加热,再加入碘水,溶液变蓝 | 淀粉未发生水解或部分水解 |
C | 向稀HNO3溶液中加入铜片并加热,试管口观察到红棕色气体 | 铜与稀HNO3溶液反应生成NO2 |
D | 向浓度均为0.1 mol·L-1的NaCl、NaI混合溶液中滴加1~2 滴0.01 mol·L-1的AgNO3溶液,产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
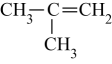 的是( )
的是( )
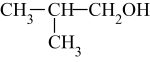 B . CH3CH2CH2CH2OH
C .
B . CH3CH2CH2CH2OH
C . 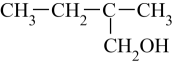 D .
D .