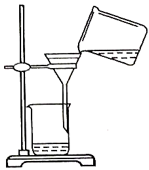
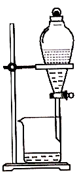
常用仪器及其使用 知识点题库
下列有关氯化钠的实验中,选用的实验用品都能用到的是( )
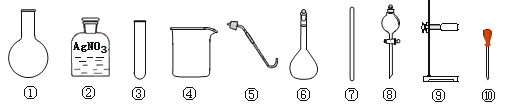
A . 除去粗盐中的不溶性杂质,选用 ④⑦⑧⑨
B . 检验A的滤液中是否含SO42﹣ , 选用 ②③⑩
C . 利用提纯后的NaCl固体配制0.1mol/L的溶液,选用 ④⑥⑦⑩
D . 用NaCl固体与浓H2SO4共热制备HCl气体,选用 ①⑤⑧⑨
下列关于实验操作的叙述中正确的是( )
A . 从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶
B . 可燃性气体点燃之前必须验纯
C . 用胶头滴管向试管中滴加液体,一定要将滴管伸入试管中
D . 用温度计搅拌溶液一定要慢慢搅拌
指出下列操作导致的后果.
-
(1) 把块状固体药品直接丢入试管底部,后果是.
-
(2) 倾倒液体时,标签没对着手心,后果是.
-
(3) 使用胶头滴管后,未经清洗就吸取别的试剂,后果是.
-
(4) 用燃着的酒精灯点燃另一只酒精灯,后果是.
联苄(  )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得。
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得。
联苄的制取原理为: ![]()
反应最佳条件为n(苯):n(1,2-二氯乙烷)=10 :1,反应温度在60-65℃之间。
实验室制取联苄的装置如下图所示(加热和加持仪器略去):

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3 , 由滴液漏斗滴加10. 7 mL1,2-二氯乙烷,控制反应温度在60-65℃,反应约60min。将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静置、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g。
相关物理常数和物理性质如下表

-
(1) 仪器a的名称为,和普通分液漏斗相比,使用滴液漏斗的优点是。
-
(2) 洗涤操作中,水洗的目的是;无水硫酸镁的作用是。
-
(3) 常压蒸馏时,最低控制温度是。
-
(4) 该实验的产率约为。(小数点后保留两位有效数字)
下列关于实验基本操作的叙述正确的是( )
A . 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B . 分液时,需收集上层液体,分层后直接从分液漏斗上口倒出上层液体
C . 将浓硫酸倒入盛水的量筒中稀释成稀硫酸
D . 使用容量瓶应先干燥,如果容量瓶中含有少量蒸馏水,会造成误差
下列有关仪器的性能或者使用方法的说明中正确的是( )
A . 试管、蒸发皿既能用于给固体加热也能用于给溶液加热
B . 分液漏斗既能用于某些混合物的分离也能用于组装气体发生器
C . 碱式滴定管既可用于中和滴定,也可用于量取一定量的NaCl或AlCl3溶液
D . 测量酒精沸点的实验中,应使温度计水银球位于被加热的酒精中
实验室需要0.3 mol·L-1 NaOH溶液480 mL和一定浓度的硫酸溶液。根据这两种溶液的配制情况回答下列问题:

-
(1) 如图所示的仪器中配制溶液肯定不需要的是(填序号),配制上述溶液还需用到的玻璃仪器是(填仪器名称)。
-
(2) 在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度(填“>”、“<”或“=”)0.3 mol·L-1。
-
(3) 实验室采购了98%(ρ=1.84g•cm﹣3)的硫酸配制3.68mol•L﹣1的硫酸溶液500mL需准确量取98%的硫酸mL;
-
(4) 该同学实际配制硫酸溶液的浓度为3.50 mol·L-1 , 原因可能是___________(填序号)。A . 用胶头滴管加水时俯视刻度 B . 容量瓶中原来存有少量水 C . 稀释硫酸的烧杯,溶液转移后未洗涤 D . 用胶头滴管加水定容时仰视刻度
-
(5) 若在滴加蒸馏水时,不慎超过了刻度线,此时应如何处理?。
下列实验操作或装置能达到实验目的的是( )
A .  量取109.3ml稀盐酸
B .
量取109.3ml稀盐酸
B .  称量25g烧碱固体
C .
称量25g烧碱固体
C . 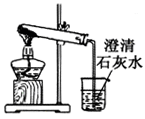 碳酸氢钠受热分解
D .
碳酸氢钠受热分解
D .  配制一定物质的量浓度的稀硫酸
配制一定物质的量浓度的稀硫酸
 量取109.3ml稀盐酸
B .
量取109.3ml稀盐酸
B .  称量25g烧碱固体
C .
称量25g烧碱固体
C .  碳酸氢钠受热分解
D .
碳酸氢钠受热分解
D .  配制一定物质的量浓度的稀硫酸
配制一定物质的量浓度的稀硫酸
下列实验操作(依次为图一至图四),其中错误的是( )

A . 图一:检查容量瓶是否漏水
B . 图二:用四氯化碳提取溴水中的溴单质
C . 图三:检验溶液中的K+
D . 图四:分离沸点不同且互溶的液体混合物
下列仪器名称正确的是( )
A . 三脚架  B . 溶量瓶
B . 溶量瓶  C . 镊子
C . 镊子  D . 坩埚
D . 坩埚 
 C . 镊子
C . 镊子
下列仪器名称为“蒸馏烧瓶”的是( )
A .  B .
B .  C .
C .  D .
D . 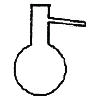
 B .
B .  C .
C .  D .
D . 
有关容量瓶上的说法错误的是( )
A . 标有温度
B . 标有刻度线
C . 标有“0”刻度
D . 标有容量
某学习小组利用蒸馏装置分离四氯化碳和酒精的混合物:

-
(1) 写出标出序号的仪器的名称:①;②
-
(2) 在仪器①中还需加入碎瓷片,其作用是;使用仪器②时水流的方向是进(用“f”“g”表示)
-
(3) 用蒸馏装置分离四氯化碳和酒精的混合物其原理是利用二者的不同
-
(4) 该装置有一个错误的地方是
氮氧化物(NOX)是常见的大气污染物,烟气脱硝是NOX控制措施中最重要的方法。研究氮氧化物的反应机理,对于保护环境有重要意义。
-
(1) Ⅰ.请写出烟气中的氮氧化物对环境的一种危害:。
-
(2) Ⅱ.NO能被灼热的铁粉还原为
 ,同时生成FeO,利用下列装置模拟该反应。
,同时生成FeO,利用下列装置模拟该反应。 
已知:①浓硝酸可将NO氧化为
 ;
;②NaOH溶液能与
 反应,不与NO反应。
反应,不与NO反应。③
 是一种常见干燥剂,与NO、
是一种常见干燥剂,与NO、  不能反应
不能反应装置A中盛放稀硝酸的仪器是。
-
(3) 上述装置接口的连接顺序为:a→→→→→g→h→b→c→d(按气流方向,用小写字母表示)。
-
(4) 装置B的作用是。
-
(5) 装置E中反应的化学方程式为。
-
(6) Ⅲ.开发湿法脱硝技术具有广阔的工业应用前景。湿法脱硝一般有碱液吸收法和氧化吸收法等。
碱液吸收法能将NOX回收为有销路的亚硝酸盐或硝酸盐产品。某实验小组为了证明酸性条件下
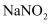 具有氧化性,下列可供选用的试剂有___________。A . KMnO4溶液 B .
具有氧化性,下列可供选用的试剂有___________。A . KMnO4溶液 B .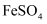 溶液
C . KI—淀粉溶液
D . NaClO溶液
溶液
C . KI—淀粉溶液
D . NaClO溶液
-
(7) 在实验室模拟同时脱硝、脱硫过程:往酸性的
 吸收液中通入含
吸收液中通入含  和NO的模拟烟气,发现脱销效果比脱硫效果差,可能原因是。
和NO的模拟烟气,发现脱销效果比脱硫效果差,可能原因是。
某兴趣小组要配制物质的最浓度为0.1ml/L的NaCl溶液,下列装置中不需要使用的是( )
A .  B .
B .  C .
C . 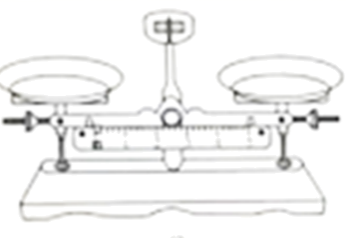 D .
D . 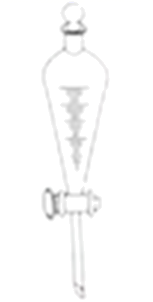
 B .
B .  C .
C .  D .
D . 
完成下列实验需用如图所示仪器的是( )
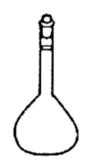
A . 制备少量 气体
B . 溶解少量
气体
B . 溶解少量 固体
C . 配置
固体
C . 配置 的
的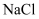 溶液
D . 配制
溶液
D . 配制 溶液
溶液
 气体
B . 溶解少量
气体
B . 溶解少量 固体
C . 配置
固体
C . 配置 的
的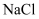 溶液
D . 配制
溶液
D . 配制 溶液
溶液
下列基本实验操作正确的是( )
|
|
|
|
A.过滤 | B.分液 | C.蒸馏 | D.蒸发 |
A . A
B . B
C . C
D . D
仪器名称为“坩埚”的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .
实验室制备、干燥、收集NH3并进行尾气处理,下列装置能达到实验目的的是( )

A . 用图1所示的装置制备NH3
B . 用图2所示的装置干燥NH3
C . 用图3所示的装置收集NH3
D . 用图4所示的装置吸收多余NH3
海带中含有丰富的碘元素。海带灼烧后的海带灰中,碘元素主要以I-形式存在。实验室里,从海带灰中提取碘的甲、乙两种方案如下:
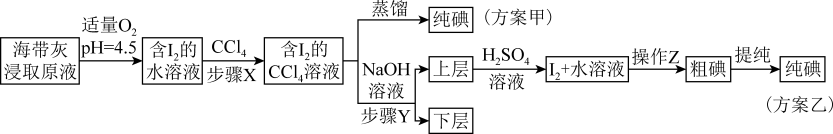
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水中的溶解度很小。
回答下列问题:
-
(1) 灼烧海带实验用到的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、等。
-
(2) “适量O2”也可以用双氧水替代,酸性条件下双氧水氧化碘离子的离子方程式为。
-
(3) 上述方案乙中,“含I2的水溶液”经三步转化为含“I2+水溶液”,主要目的是。
-
(4) 步骤X中,萃取后分液漏斗内观察到的现象是。
-
(5) 下列有关步骤Y的说法中正确的是____(填标号)A . 主要是除浸取原液中的有机杂质 B . 将碘转化成离子进入水层 C . 应控制NaOH溶液的浓度和体积 D . NaOH溶液可由乙醇代替
-
(6) 方案甲中采用蒸馏分离效果不佳,原因是;方案乙中操作Z的名称是。
最近更新