化学实验操作的先后顺序 知识点题库
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4 , 其流程如下:

已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:33℃)。
-
(1) 在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是 ,原料中的金属钠通常保存在 中,实验室取用少量金属钠需要用到的实验用品有 , ,玻璃片和小刀等;
-
(2) 请配平第①步反应的化学方程式: NaBO2+ SiO2+ Na+ H2=NaBH4+2Na2SiO3;
-
(3) 第②步分离采用的方法是 ;第③步分离(NaBH4)并回收溶剂,采用的方法是 .
-
(4) NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g),在25℃,101KPa下,已知每消耗3.8克NaBH4(s)放热21.6KJ,该反应的热化学方程式是 。
①给试管中的药品加热,必须先 ,后集中加热.
②点燃可燃性气体(如H2、CO等)时,都要先 , 后点燃.
③H2还原CuO实验结束时,要先 ,后移去导气管.
(2)要分离下列四组混合物:a.饱和食盐水与沙子 b.从KNO3和NaCl的混合溶液中获得KNO3 c.水和汽油的混合物 d.CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
①分离a、b的操作分别为 、 .
②上述四组分离时需使用酒精灯的有 和 (填序号).
③分离c时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是
A.做铁丝在氧气中燃烧的实验时,先在集气瓶底部铺一层细沙再点燃铁丝
B.先加入药品再检查装置的气密性
C.加热高锰酸钾并用排水法收集氧气结束后,先移走酒精灯,后从水中取出导管
D.
(1)石蕊试纸(检验气体):
(2)容量瓶: .
(3)酸式滴定管:
(4)集气瓶(收集氯化氢):
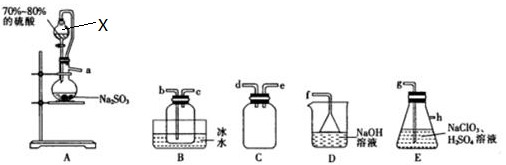
回答下列问题:
-
(1) 仪器X的名称是。
-
(2) 欲选择上图中的装置收集ClO2 , 其连接顺序为a→(按气流方向,用小写字母表示)。
-
(3) 装置C的作用是,装置E中反应的离子方程式为。
-
(4) 处理含硫(Na2S)碱性废水时,ClO2与Na2S反应(S2-被氧化为SO42-)的离子方程式为;处理含硫碱性废水时,相同条件下同体积的ClO2相对于Cl2的优点是。
-
(5) ClO2很不稳定,需现用现配,为测定所得溶液中ClO2的含量,进行下列实验:
步骤1:准确量取V1 mL ClO2溶液加入锥形瓶中。
步骤2:用稀硫酸调节ClO2溶液的pH≤2.0,再加入足量KI晶体,静置片刻。
步骤3:加入指示剂,用c mol·L-1的Na2S2O3标准溶液滴定至终点时,消耗V2 mL Na2S2O3标准溶液。
(已知:2ClO2+8H++10I-=2Cl-+5I2+4H2O;2S2O32-+I2=2I-+S4O62-)
①配制100mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管和。
②原溶液中ClO2的含量为(用含c、V1、V2的代数式表示)g·L-1。
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过1/3容积的试管加热
③将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
④将烧瓶放在桌上,用力塞紧塞子
⑤进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
⑥向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32-
⑦用坩埚钳夹取加热后的蒸发皿
⑧将溶质的质量分数为a%、物质的量浓度为c1 mol•L-1的稀硫酸加热蒸发掉一定量水,使溶质的质量分数变为2a%,则此时硫酸的物质的量浓度大于2c1 mol•L-1。
-
(1) 所需浓硫酸的体积是 mL, 量取浓硫酸所用的量筒的规格是 (用下列编号填空) 。
A.10 mL B.25 mL C.50 mL D.100 mL
-
(2) 第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线, 改用向容量瓶中滴加蒸馏水至为止。塞紧瓶塞,倒转摇匀并转移至试剂瓶中。
-
(3) 下列情况对所配制的稀硫酸浓度有何影响? (填 “ 偏大 ”“ 偏小 ” 或 “ 无影响”)
①容量瓶用蒸馏水洗涤后残留有少量的水
②在转入容量瓶前烧杯中溶液未冷却至室温
③取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯。
④定容结束时俯视刻度线
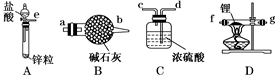
甲同学的实验方案如下:
-
(1) 仪器的组装连接:上述仪器装置接口的连接顺序为,加入药品前首先要进行的实验操作是(不必写出具体的操作方法);其中装置B的作用是。
-
(2) 添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯(一种有机化合物)中浸洗数次,该操作的目的是除去锂表面的石蜡,然后快速把锂放入到石英管中。通入一段时间氢气后加热石英管,在加热D处的石英管之前,必须进行的实验操作是。
-
(3) 加热一段时间后停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险。分析该反应原理,完成LiH与水反应的化学方程式。
-
(4) 准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为。

-
(1) 《实验化学》中制备摩尔盐的化学方程式为
-
(2) 步骤1中少量稀硫酸的作用是,步骤Ⅱ中过量饱和草酸的作用是
-
(3) 请设计实验方案证明FeC2O4•2H2O晶体已经洗涤干净:
-
(4) 步骤Ⅲ在40℃条件下进行的原因
-
(5) 步骤Ⅵ抽滤如图安装好装置,请按符合题意操作顺序补充完整:
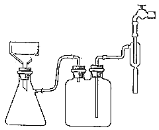
在布氏漏斗中加入滤纸→→确认抽干
a、转移固液混合物;b、开大水龙头;c、关闭水龙头;d、微开水龙头;e、加入少量蒸馏水润湿滤纸
-
(1) Ⅰ.某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。请回答下列问题:
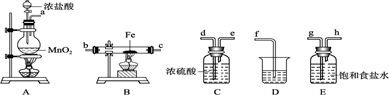
A 中发生反应的化学方程式为。在该反应中当 0.4molHCl发生反应时,生成标准状况下的Cl2 的体积为。浓盐酸在反应中显示出来的性质是(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
-
(2) 各装置的正确连接顺序为(填写装置代号)A→→→→D。
-
(3) 装置 E 的作用是。写出装置 D(D中所盛溶液为 NaOH)中反应的化学方程式
-
(4) 工业上用电解法制备氯气的化学方程式为:。
-
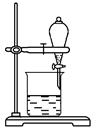
(5) Ⅱ.某小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈色;他们打开分液漏斗活塞,却未见液体流下,原因可能是
①蒸馏时,先点燃酒精灯,再通冷凝水
②加热氯酸钾和二氧化锰的混合物制备氧气,用排水法收集气体后,先移出导管后撤酒精灯
③实验室制取某气体时,先检查装置气密性后装药品
④分液时,先打开分液漏斗上口的塞子,后打开分液漏斗的旋塞
⑤H2还原CuO实验时,先检验气体纯度后点燃酒精灯
⑥使用托盘天平称盘物体质量时,先放质量较小的砝码,后放质量较大的砝码
⑦蒸馏时加热一段时间,发现忘记加沸石,应迅速补加沸石后继续加热
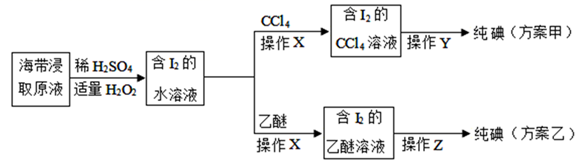
已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5℃,微溶于水,CCl4沸点76.8℃。进行操作Y时,没有观察到碘的升华。
请回答:
-
(1) 写出实验操作名称:操作X;操作Y。
-
(2) 下列说法错误的是________A . 加入过氧化氢的目的是将碘离子氧化为单质碘 B . 碘在乙醚中的溶解度比在水中的溶解度大且乙醚在水中的溶解度小,可用乙醚萃取碘 C . 若用40mLCCl4萃取,甲直接用40mL CCl4萃取1次,乙萃取4次,每次用10mL CCl4 , 甲的萃取效率高 D . 操作Z时,不需要加沸石等来防止暴沸
-
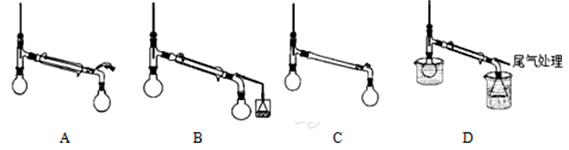
(3) 从下面的装置中选择操作Z的最合适的装置图
-
(4) 请选择合适的编号,按正确的操作顺序完成用乙醚萃取碘的实验(假设只放气一次):c→a→倒入溶液和萃取剂→ →→→→f→a→d→使下层液体慢慢流出→c→上层液体从上口倒出。
a.打开上口玻璃塞; b.塞上上口玻璃塞; c.关闭旋塞;d.打开旋塞;e.倒转分液漏斗振摇; f.放在铁圈上静置;g.手持静置。
-
(5) 从碘的四氯化碳溶液中获取碘,还可以用以下流程:

请解释氢氧化钠溶液的作用。
-
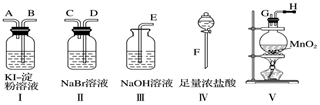
(1) 若所制取气体的流向从左向右时,上述仪器接口的连接顺序为接、 接、接、接(填字母)。
-
(2) 实验开始后装置Ⅴ中反应的离子方程式为。
-
(3) 装置Ⅱ中发生的现象是,反应的化学方程式为。
-
(4) 装置Ⅰ中产生的现象:溶液先变蓝一段时间后蓝色褪去,生成两种强酸,请写出蓝色褪去的化学方程式:。
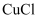 作
作  的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中
的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中 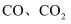 、
、  和
和  的含量(已知:
的含量(已知: 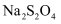 和
和 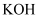 的混合溶液可吸收氧气)。下列说法错误的是( )
的混合溶液可吸收氧气)。下列说法错误的是( ) 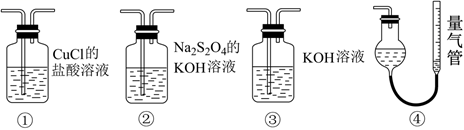
I.实验室制备亚硝酸钠
某化学兴趣小组设计如下实验装置(略去夹持仪器)制各亚硝酸钠。
已知:①2NO+Na2O2=2NaNO2 , ②酸性条件下,NO、NO2或  都能与
都能与  反应生成
反应生成  和Mn2+。
和Mn2+。
回答下列问题:

-
(1) 装置C的名称是,试剂X的名称是。
-
(2) 为制得少量亚硝酸钠,上述装置按气流方向连接顺序为A→()→()→()→()→D(装置可重复使用)。
-
(3) 加入浓HNO3前,需先向装置内通一段时间N2 , 目的是 。
-
(4) D中主要反应的离子方程式为。
-
(5) 已知市售亚硝酸钠主要成分是NaNO2(含NaNO3、水等杂质),可以采用KMnO4测定含量(其中杂质不跟酸性KMnO4溶液反应)。称取5.0 g市售亚硝酸钠样品溶于水配制成250 mL的样品溶液。取25.00mL样品溶液于锥形瓶中,用稀硫酸酸化后,再用0.1000 mol/L的KMnO4标准液进行滴定,消耗KMnO4标准液体积28.00 mL。判断滴定终点的现象是,该市售亚硝酸钠中NaNO2的质量分数是。
已知: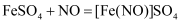
-
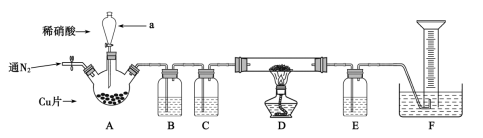
(1) 组装仪器后,应先进行的操作是。
-
(2) 仪器a的名称是,C中的药品是,E的作用是。
-
(3) 装置A中发生反应的离子方程式为;D中固体逐渐变黑,并生成一种无毒气体,反应的方程式为。
-
(4) 通入N2的作用是。
-
(5) 反应前,装置D(硬质玻璃管和铜粉)的质量为m1g,反应后质量为m2g,则该反应生成的气体在标准状况下体积为L(用m1、m2表示)
实验步骤:
I.K2MnO4制备:称取7.0gKOH和5.0gKClO3于铁坩锅中混匀,固定坩埚,小火加热,用铁棒搅拌,待混合物熔融,边搅拌边逐渐加入MnO2 , 可见熔融物黏度增大,不断用力搅拌,以防结块。待反应物快干时,不断搅拌使其呈颗粒状,加大火焰,强热6分钟,即得墨绿色的K2MnO4。
II.K2MnO4浸取:待物料冷却,于研钵中研细,在烧杯中用40mL蒸馏水浸取,搅拌、加热,静置,分离出上层清液于另一个烧杯中,依次用20mL蒸馏水、20mL4.0%KOH溶液重复浸取,合并三次浸取液。
III.K2MnO4歧化:向浸取液中通入CO2气体,溶液逐渐变色,用pH试纸测试溶液,当pH达到10~11时,停止通气,加热溶液,趁热抽滤。
IV.KMnO4结晶:将滤液蒸发浓缩、冷却结晶、抽滤、洗涤、干燥,得到产品。
合成反应:3MnO2+6KOH+KClO3
 3K2MnO4+KCl+3H2O,3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3。
3K2MnO4+KCl+3H2O,3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3。
有关物质的溶解度(g/100g水):
|
|
0℃ |
10℃ |
20℃ |
30℃ |
| K2CO3 |
105 |
109 |
111 |
114 |
| KHCO3 |
22.5 |
27.4 |
33.7 |
39.9 |
请回答:
-
(1) 步骤I不可选用瓷坩埚,原因是。
-
(2) 步骤II不可通过普通过滤操作分离浸取液,宜采取的便捷的分离操作是。
-
(3) 步骤III必须通过监测溶液pH控制CO2通入量,否则产品纯度会降低,原因是。
-
(4) 下列说法不正确的是____。A . 步骤I中不可选用玻璃棒,原因之一是熔融物黏稠,玻璃棒易折断 B . 步骤II中第3次浸取选用4%KOH溶液,目的是防止K2MnO4因pH降低而歧化,影响产率 C . 步骤III中抽滤可使用普通布氏漏斗,预先将滤纸润湿,微开水龙头,使滤纸紧贴瓷板 D . 步骤IV中为避免KMnO4在浓缩后的溶液中的溶解损失,可小心蒸干溶液得到产品,提高产量
-
(5) 使用如图所示装置,经过一系列操作完成步骤IV中的抽滤和洗涤,请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只考虑一次):开抽气泵→转移固液混合物→b→c→→关抽气泵。

a.打开活塞;b.关闭活塞;c.确认抽干;d.用冷水洗涤;e.用无水乙醇洗涤;f.调低抽气泵真空度(减缓抽滤速度)。
-
(6) 可通过氧化还原滴定法用标准草酸溶液测定产品纯度:


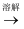


 ……
……①移取一定量KMnO4溶液可选用移液管或(填“酸式”或“碱式”)滴定管。
②滴定时无需另外加入指示剂,滴定终点的现象为。
③若产品中混有少量K2CO3杂质,则滴定结果(填“偏高”“偏低”或“无影响”)。



