氯水、氯气的漂白作用 知识点
氯水和氯气的漂白性:氯水具有漂白性是因为含有次氯酸,次氯酸能漂白物质是因为其具有强氧化性。而氯气的漂白作用,也是因为其和水发生反应生成次氯酸而表现出来。
氯水、氯气的漂白作用 知识点题库
下列说法不正确的是( )
A . Na2O2、HClO、SO2等物质都具有漂白作用
B . 液氨、液氯、液态氯化氢都是电解质
C . 所有的置换反应都是氧化还原反应,而所有的复分解反应都是非氧化还原反应
D . 非金属氧化物不一定是酸性氧化物,有些金属氧化物也能与强碱反应
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A . 将NaHCO3固体加入新制氯水中,有无色气泡(H+)
B . 使红色布条褪色(HCl)
C . 向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
D . 滴加AgNO3溶液生成白色沉淀(Cl﹣)
饱和氯水长期放置后,下列微粒在溶液中不减少的是( )
A . HClO
B . ClO-
C . Cl2
D . Cl-
日常生活和工业生产中常用到漂白剂。下列溶液具有漂白作用的是( )
A . NaClO溶液
B . 久置的氯水
C . KOH溶液
D . 稀H2SO4
能使干燥的有色布条褪色的是( )
A . 氯气
B . 液氯
C . 氯水
D . 盐酸
下列化学实验事实及其解释正确的是( )
A . 将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯气具有氧化性和漂白性
B . 向Na2S2O3稀溶液中加入稀硫酸,发生如下反应:S2O32-+2H+=SO2↑+S↓+H2O,利用产生浑浊的快慢或产生气泡的快慢可以测定该反应在不同条件下的反应速率
C . 乙酸乙酯中少量乙醇杂质可加水除去,其原理与溴水中加四氯化碳萃取溴类似
D . 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,恢复红色,说明亚硫酸不稳定
新制氯水的主要成分有Cl2、HClO、H+、Cl-等试用氯水的成分填空:
①氯水与NaBr溶液反应,起作用是
②氯水用于自来水杀菌消毒,起作用是
③氯水加入硝酸银溶液,出现白色沉淀,起作用是
④石蕊滴入氯水中,先变红后褪色,起作用是
-
(1) 写出正丁烷的结构简式:;写出漂白粉有效成分的化学式:。
-
(2) 写出镁条和氮气反应的化学方程式。写出铁和氯化铁溶液反应的离子方程式。写出乙烯和水反应的化学方程式。
下列各组中的两物质反应时,反应条件或反应物用量的改变对生成物没有影响的是( )
① CO2与Ca(ClO)2 ② Na2CO3与HCl ③ Mg与CO2 ④ Na与H2O ⑤ Na与O2 ⑥ NaOH与CO2
A . ③⑤
B . ③④
C . ①③④
D . ②④⑥
下列有关卤素的说法错误的是( )
A . 新制氯水显浅黄绿色,但放置一段时间之后颜色会褪去
B . 除  外,相对分子质量小的卤素单质可将相对分子质量大的卤素从其盐溶液中置换出来
C . 淀粉-碘化钾溶液在空气中变蓝,发生了反应:
外,相对分子质量小的卤素单质可将相对分子质量大的卤素从其盐溶液中置换出来
C . 淀粉-碘化钾溶液在空气中变蓝,发生了反应:  D . 由
D . 由 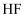 、
、 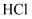 、
、 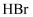 、
、 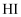 的酸性递增的事实,可推出
的酸性递增的事实,可推出 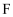 、
、 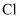 、
、 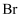 、
、 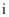 的非金属性递增
的非金属性递增
 外,相对分子质量小的卤素单质可将相对分子质量大的卤素从其盐溶液中置换出来
C . 淀粉-碘化钾溶液在空气中变蓝,发生了反应:
外,相对分子质量小的卤素单质可将相对分子质量大的卤素从其盐溶液中置换出来
C . 淀粉-碘化钾溶液在空气中变蓝,发生了反应:  D . 由
D . 由 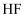 、
、 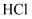 、
、 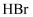 、
、 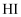 的酸性递增的事实,可推出
的酸性递增的事实,可推出 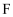 、
、 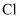 、
、 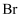 、
、 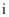 的非金属性递增
的非金属性递增
下列实验操作能达到相应实验目的的是( )
A . 用pH试纸测定新制氯水的pH
B . 用酒精代替CCl4来萃取溴水中的Br2
C . 用向上排气法收集亚硫酸钠与浓硫酸反应产生的SO2
D . 直接加热氯化铵并用向下排气法收集NH3
不能用来作为新冠病毒的消毒剂是( )
A . 84消毒液
B . 漂粉精
C . 75%酒精
D . 明矾
下列两种变化的实质相似的是( )
A . 浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
B . 二氧化硫和氯气均能使品红溶液褪色
C . 常温下浓硫酸用铁制容器存放,浓硝酸能用铝罐车运输
D . 氨气和碘化氢气体均不能用浓硫酸干燥
下列实验方案能够达到目的的是 ( )
| 实验目的 | 实验方案 | |
| A | 除去氯气中的水蒸气 | 将混合气体通过盛有碱石灰的干燥管 |
| B | 检验钠与H2O的反应产物NaOH | 将绿豆粒大小的钠投入盛有适量水的培养皿中,加入稀盐酸 |
| C | 鉴别碳酸钠和碳酸氢钠溶液 | 向溶液中分别滴加稀盐酸 |
| D | 检验新制氯水中含有HClO | 向新制氯水中加入少量CaCO3 |
A . A
B . B
C . C
D . D
某实验小组对氯水成分和性质进行研究,实验如图:

-
(1) 氯水呈黄绿色,说明其中含有(填化学式)。
-
(2) 实验一的现象表明,氯水具有酸性和性。
-
(3) 氯气与水反应的化学方程式为。
-
(4) 用化学方程式说明实验二中“红色不褪去”的原因。
-
(5) 实验四证明了实验三中“红色不褪去”不是因为氯水被稀释所致,补充所加试剂和现象。、。
-
(6) (实验四)
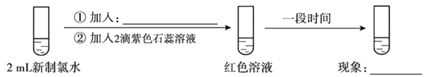
进一步探究实验三中“红色不褪去”的原因。
(实验五)取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
写出氯水和硝酸银溶液反应的化学方程式。
下列对新制氯水与久置氯水性质的叙述正确的是( )
A . 都为黄绿色
B . 都具有漂白性
C . 都能与硝酸银溶液产生白色沉淀
D . 都能使紫色石蕊试液呈红色
下列关于氯气及其化合物的叙述错误的是( )
A . 久置氯水酸性比新制氯水强
B . 因为氯气有毒,所以可用于杀菌、消毒、漂白
C . 氯气泄漏时,人员应向高处撤离
D . 新制备的氯水中滴加酸化硝酸银可出现白色沉淀
将一定量Cl2通过装置甲后,再通过放有湿润紅色布条的装置乙,红色布条不褪色。装置甲中所盛试剂可能是( )
①浓硫酸 ②NaOH溶液 ③饱和食盐水

A . ①②
B . ②③
C . ①③
D . ②
现有久置氯水、氯化钠溶液、氢氧化钠溶液和新制氯水,可用来鉴别它们的试剂是( )
A . AgNO3溶液
B . 酚酞溶液
C . 紫色石蕊溶液
D . 饱和食盐水
为了探究氯水能否和碳酸钡发生反应,某学生设计并完成了如下实验:
【实验一】向盛有饱和氯水的烧杯中加入足量碳酸钡,并充分搅拌,观察到氯水的黄绿色褪去并同时产生气体a。
【实验二】取实验一后烧杯中清液,分别进行如下实验:①往该清液中滴加盐酸时有大量气体产生,其主要成分为气体b;②往该清液中滴加硫酸钠溶液有白色沉淀产生;③将该清液滴在蓝色石蕊试纸上,试纸先变红后褪色。回答下列问题:
-
(1) 写出气体的化学式:a,b
-
(2) 在实验二中,清液使蓝色石蕊试纸先变红后褪色说明该清液中含有(填化学式);清液中滴加硫酸钠溶液产生白色沉淀,该反应的离子方程式为。
-
(3) 实验二中所得气体b可用右图所示装置净化。

①b中所含杂质气体为(填化学式)。
②如果连接在该装置之后的另一活塞发生堵塞,则长颈漏斗中出现的现象为。
-
(4) 写出产生气体b的反应的离子方程式。
-
(5) 通过上述实验,可推知氯水和碳酸钡反应的化学方程式为。
最近更新



