常用仪器及其使用 知识点题库
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体

B .
B . 
C .
C . 
D .
D . 
①A与组合,用于,②B与组合,用于,
③B与组合,用于,④D与组合,用于.


A;B;C;D;E.
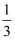 处,手持试管夹长柄末端进行加热
C . 燃着的酒精灯翻倒,酒精洒到桌面并且燃烧,为了人身安全,应立即撤离现场
D . 将玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端并缓慢旋进塞孔中
处,手持试管夹长柄末端进行加热
C . 燃着的酒精灯翻倒,酒精洒到桌面并且燃烧,为了人身安全,应立即撤离现场
D . 将玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端并缓慢旋进塞孔中
 检验K+的存在
B .
检验K+的存在
B .  干燥CO2
C .
干燥CO2
C .  分离溴与CCl4
D .
分离溴与CCl4
D .  蒸发食盐水
蒸发食盐水
-
(1) Ⅰ.老卤中主要含KCl和少量MgCl2、CaCl2、MgSO4等,需要分离提纯得到KCl.现有几种试剂:①盐酸;②K2CO3;③Na2CO3;④NaOH;⑤KOH;⑥Ba(OH)2;⑦BaCl2;⑧Ba(NO3)2 .
为有效除去老卤中的杂质,加入试剂的合理顺序为_________.
A . 先加NaOH,后加Na2CO3 , 再加BaCl2 B . 先加BaCl2 , 后加NaOH,再加Na2CO3 C . 先加K2CO3 , 后加KOH,再加Ba(NO3)2 D . 先加Ba(NO3)2 , 后加K2CO3 , 再加KOH E . 先加Ba(OH)2 , 后加K2CO3 -
(2) 过滤除去沉淀后还需要加入的试剂为 (填序号),还需要进行的实验为.
A.蒸发结晶 B.降温结晶
-
(3) Ⅱ.现有如下图仪器:

①仪器F的名称是.
②在实验室组成一套蒸馏装置肯定需要所给仪器中的一部分,按照实验仪器由下到上、从左到右的顺序,这些仪器依次是(填字母).
-
(4) Ⅲ.小明同学将16.0 g NaOH固体溶于水配成100 mL溶液,其密度为1.60 g/mL,小明计划用配好的NaOH溶液制取简易消毒液。回答下列问题:
①用量筒取小明同学所配的NaOH溶液 mL才能与标准状况下2.24 L氯气恰好完全反应.
②该消毒液即市面上的“84消毒液”,小明将(2)所取体积的NaOH溶液吸收好氯气后的溶液稀释到5 L使用,稀释后溶液中c(Na+)=
③“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员需要520 mL 2.3 mol/L的稀硫酸,拟采用98%(密度为1.84 g/cm3)的浓硫酸进行配制.
①需取用的浓硫酸的体积为mL.
②取上述配好的硫酸溶液50 g与50 g 水混合,所得溶液的物质的量浓度
A.等于1.15 mol/L B.小于2.30 mol/L 大于1.15 mol/L
C.小于1.15 mol/L D.大于2.30 mol/L
-
(1) Ⅰ.有如下化学实验装置:A.L量筒 B.容量瓶 C.滴定管 D.烧杯;标有“0”刻度的化学仪器为;(填代号)
-
(2) 使用前要检验是否漏水的仪器;(填代号)
-
(3) 量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为 。(填代号 )
-
(4) Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的如下表:
物质
Cu(OH)2
Fe(OH)2
Fe(OH)3
开始沉淀pH
6.0
7.5
1.4
沉淀完全pH
13
14
3.7
分离实验的实验操作步骤和目的为:(完成下表空白处)
实验步骤
实验操作
实验操作目的
步骤1
在溶液中加入H2O2
①
步骤2
②
保证将Fe3+完全沉淀
步骤3
③
滤出氢氧化铁
步骤4
洗涤沉淀
④
步骤5
在沉淀中加入适量稀硫酸和铁粉
得到FeSO4溶液
 试纸可以测出某
试纸可以测出某 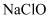 溶液的
溶液的  为9.6
B . 用托盘天平称量
为9.6
B . 用托盘天平称量  氯化钠
C . 用规格为
氯化钠
C . 用规格为  的量筒量取
的量筒量取  的硫酸
D . 用酸式滴定管量取
的硫酸
D . 用酸式滴定管量取  的
的 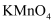 溶液
溶液

回答下列问题:
-
(1) 由FeSO4·7H2O固体配制0.10mol/LFeSO4溶液,需要的仪器有药匙、玻璃棒、(从下列图中选择,写出名称)。

-
(2) 电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择作为电解质。
阳离子
u∞×108(m2•s-1•V-1)
阴离子
u∞×108(m2•s-1•V-1)
Li+
4.07
HCO

4.61
Na+
5.19
NO

7.40
Ca2+
6.59
Cl-
7.91
K+
7.62
SO

8.27
-
(3) 电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入电极溶液中;
-
(4) 电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol/L。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=。
-
(5) 根据(3)、(4)实验结果,可知石墨电极的电极反应式为,铁电极的电极反应式为。因此,验证了Fe2+氧化性小于、还原性小于。
| | | | |
| A.泥三角 | B.长颈漏斗 | C.溶量瓶 | D.镊子 |
①苯甲醛在浓NaOH溶液能反应如反应2![]() +NaOH→
+NaOH→![]() +
+![]()
②C6H5CHO+NaHSO3 → C6H5CH(OH)SO3Na
已知相关物质的性质如表所示:
名称 | 相对 分子质量 | 密度(g/cm3) | 熔点(oC) | 沸点(oC) | 性质 |
苯甲醛 | 106 | 1.04 | -26 | 179.62 | 微溶于水,易溶于醇和醚 |
苯甲醇 | 108 | 1.04 | -15.3 | 206 | / |
苯甲酸 | 122 | / | 122.13 | 249 | 微溶于水,易溶于醇和醚 |
乙醚 | 74 | 0.71 | -116.3 | 34.6 | 不溶于水,易溶于醇;易燃易爆 |
该兴趣小组同学利用上述原理制备苯甲醇,具体实验装置和实验步骤如下:
步骤1:向图1所示装置中加入8gNaOH和30mL水,搅拌溶解。稍冷,加入10mL新蒸馏的苯甲醛。搅拌,加热回流约40min。
步骤2:停止加热,从球形冷凝管上口缓慢加入20mL冷水,摇匀,冷却至室温,然后用乙醚萃取三次,每次10mL,合并有机层,并对其进行一系列洗涤操作。
步骤3:洗涤后的有机层,倒入干燥的锥形瓶,加入无水硫酸镁,过滤,将滤液倒入如图2所示的蒸馏装置,先缓慢加热蒸出乙醚;当乙醚蒸出完毕后,改变加热方式继续升温并收集T℃左右的馏分得到苯甲醇。
请回答:

-
(1) 步骤1中所使用的苯甲醛需新蒸馏的原因是。
-
(2) 步骤2中,进行萃取时所需的玻璃仪器是;在萃取振摇过程中应进行操作,分液时分离得到有机层的操作是。
-
(3) 步骤2中对有机层进行一系列洗涤操作时洗涤剂使用的正确顺序是;其中加入饱和NaHSO3溶液的作用是。
a.10mL 10%的Na2CO3溶液 b.5mL 饱和NaHSO3溶液 c.10mL H2O
-
(4) 下列说法正确的是____。
 A . 步骤1中需冷却、搅拌的原因是防止苯甲醛因温度太高而发生副反应 B . 图1,图2装置中都含有冷凝管,进出水方向相同,故可交换使用 C . 步骤2萃取可采用30mL乙醚一次性完成,既操作方便又节约时间,提高效率 D . 步骤3,无水硫酸镁做干燥剂除去有机层中的水,也可用无水氯化钙代替 E . 步骤3,乙醚的沸点较低,故蒸馏时可采用如图所示的水浴加热方式 F . 步骤3,T应控制在206℃左右,可采用空气冷凝的方式代替水冷
A . 步骤1中需冷却、搅拌的原因是防止苯甲醛因温度太高而发生副反应 B . 图1,图2装置中都含有冷凝管,进出水方向相同,故可交换使用 C . 步骤2萃取可采用30mL乙醚一次性完成,既操作方便又节约时间,提高效率 D . 步骤3,无水硫酸镁做干燥剂除去有机层中的水,也可用无水氯化钙代替 E . 步骤3,乙醚的沸点较低,故蒸馏时可采用如图所示的水浴加热方式 F . 步骤3,T应控制在206℃左右,可采用空气冷凝的方式代替水冷
 B .
B .  C .
C .  D .
D . 





