金属冶炼的一般原理 知识点题库
下列有关物质工业制法的反应原理错误的是( )
A . 侯氏制碱:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓ 2NaHCO3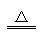 Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O
Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2
H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2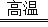 CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融)
CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
 Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O
Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2
H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2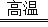 CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融)
CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
下列解释事实的方程式不正确的是( )
A . 铝热法炼铁:2Al+Fe2O3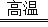 2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2
2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2 2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
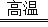 2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2
2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2 2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
有关化学反应的方向和速率的研究可以指导化工生产.下列说法正确的是( )
A . N2+3H2 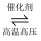 2NH3△H<0,在任何温度下均为自发反应
B . 向新制氯水中加入少量小苏打固体可提高其漂白能力
C . 1L密闭容器中发生反应4NH3+5O2⇌4NO+6H2O,充少量 N2可加快反应速率
D . 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替
2NH3△H<0,在任何温度下均为自发反应
B . 向新制氯水中加入少量小苏打固体可提高其漂白能力
C . 1L密闭容器中发生反应4NH3+5O2⇌4NO+6H2O,充少量 N2可加快反应速率
D . 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替
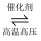 2NH3△H<0,在任何温度下均为自发反应
B . 向新制氯水中加入少量小苏打固体可提高其漂白能力
C . 1L密闭容器中发生反应4NH3+5O2⇌4NO+6H2O,充少量 N2可加快反应速率
D . 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替
2NH3△H<0,在任何温度下均为自发反应
B . 向新制氯水中加入少量小苏打固体可提高其漂白能力
C . 1L密闭容器中发生反应4NH3+5O2⇌4NO+6H2O,充少量 N2可加快反应速率
D . 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(H2或CO)法;③活泼金属置换法;④电解法.四种方法各有优缺点,在工业上均有应用.
-
(1) 一种无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别为 (填序号).A . O2、CO2 B . O2、CO C . CO2、CO D . CO、CO2
-
(2) 下列说法错误的是 (填序号).A . 对废旧金属最好的处理方法是回收、再利用 B . 提炼金属要经过矿石的富集、冶炼、精炼三步 C . 活泼金属的冶炼都是通过电解其盐溶液制得 D . 热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
-
(3) 钛(Ti)有“未来钢铁”之称,工业上常以TiCl4+2Mg
 Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行 (填序号).
A . 稀有气体中 B . 空气中 C . 氮气中 D . CO2气体中.
Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行 (填序号).
A . 稀有气体中 B . 空气中 C . 氮气中 D . CO2气体中.
下列各种冶炼方法中,可制得相应金属的为( )
A . 加热氢氧化铝
B . 加热碳酸钙
C . 电解熔融氯化镁
D . 电解饱和食盐水
下列有关金属的说法中,正确的是( )
①在人类对金属材料的使用过程中,性质活泼的金属单质最早被人们冶炼和使用;
②纯铁比生铁抗腐蚀性更强;
③单质铝在空气中比较耐腐蚀,所以铝是不活泼金属;
④正常人体缺钙会引起骨质疏松症,缺铁会引起贫血等疾病;
⑤青铜、不锈钢、硬铝都是合金;
⑥可通过焰色反应区分钾元素和钠元素.
A . ②④⑤⑥
B . ②③④⑤
C . ①③④⑤
D . ①②⑤⑥
下列关于金属的一些说法不正确的是( )
A . 合金的性质与其成分金属的性质不完全相同
B . 工业上金属Mg、Al都是用电解熔融的氯化物制得的
C . 黑色的氧化铜灼烧会变成砖红色
D . 将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
下列有关工业生产的叙述中错误的是( )
A . 电解氯化钠溶液制金属钠
B . 石灰石是炼铁和制玻璃的原料之一
C . 氯气通入石灰乳中制漂白粉
D . 硫酸工业的主要设备有沸腾炉、接触室、吸收塔
金属锂是密度最小的金属,等质量的金属,锂能释放出更多的电子,故常用来制造高能量电池。已知锂的金属性介于钠和镁之间,则下列能冶炼出金属锂的方法是( )
A . 电解法
B . 热还原法
C . 热分解法
D . 铝热法
下列金属冶炼的反应原理,错误的是( )
A . MgCl2(熔融)  Mg+Cl2↑
B . Al2O3+3H2
Mg+Cl2↑
B . Al2O3+3H2  2Al+3H2O
C . Fe3O4+4CO
2Al+3H2O
C . Fe3O4+4CO  3Fe+4CO2
D . 2HgO
3Fe+4CO2
D . 2HgO  2Hg+O2↑
2Hg+O2↑
 Mg+Cl2↑
B . Al2O3+3H2
Mg+Cl2↑
B . Al2O3+3H2  2Al+3H2O
C . Fe3O4+4CO
2Al+3H2O
C . Fe3O4+4CO  3Fe+4CO2
D . 2HgO
3Fe+4CO2
D . 2HgO  2Hg+O2↑
2Hg+O2↑
下列化学反应在金属冶炼工业中还没有得到应用的是( )
A . 2NaCl(熔融)  2Na+Cl2↑
B . Al2O3+3C2
2Na+Cl2↑
B . Al2O3+3C2  2Al+3CO↑
C . Fe2O3+3CO
2Al+3CO↑
C . Fe2O3+3CO  2Fe+3CO2
D . 2Ag2O
2Fe+3CO2
D . 2Ag2O  4Ag+O2↑
4Ag+O2↑
 2Na+Cl2↑
B . Al2O3+3C2
2Na+Cl2↑
B . Al2O3+3C2  2Al+3CO↑
C . Fe2O3+3CO
2Al+3CO↑
C . Fe2O3+3CO  2Fe+3CO2
D . 2Ag2O
2Fe+3CO2
D . 2Ag2O  4Ag+O2↑
4Ag+O2↑
下列金属的冶炼需要用到电解法的是( )
A . 钠
B . 铁
C . 铜
D . 银
下列说法错误的是( )
A . 硝化甘油在体内能够分解出大量硝酸,会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛
B . 侯氏制碱法的工艺流程应用了物质溶解度的差异
C . 刚玉、红宝石、蓝宝石的主要成分是氧化铝,而青花瓷、分子筛的主要成分是硅酸盐
D . 生物炼铜法就是利用某种能耐受铜盐毒性的细菌,利用空气中的氧气把不溶性的硫化铜转化为可溶性的铜盐,从而使铜的冶炼变得成本低,污染小,反应条件十分简单
化学与生活生产密切相关。下列说法中,错误的是( )
A . 将海水直接电解可获得 Mg及Cl2等单质
B . 把石灰浆喷涂在树干上可消灭树皮上的过冬虫卵
C . 施用适量石膏可降低盐碱地(含较多NaCl、Na2CO3)的碱性
D . 施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用
周期表中短周期6种元素A、B、C、D、E、F,原子序数依次增大。A的原子半径最小,A和D、C和F分别同主族,F的单质是黄色固体,B所形成的化合物种类最多,E的最外层电子数等于其电子层数。
-
(1) 写出元素符号:A、B、C、D、E、F。
-
(2) 写出工业制备E单质的化学方程式。
-
(3) 写出一种由其中两种元素组成的既含极性键又含非极性键的18电子微粒(写化学式)。
-
(4) 由A、C元素组成的化合物甲与由D、C元素组成的化合物乙反应可制备O2 , 请写出乙的电子式。
-
(5) 3molDABC3和2molD2C2混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分及物质的量分别是。
冶炼金属常用以下几种方法:
①用碳、一氧化碳或氢气做还原剂还原;
②用较活泼金属钠、镁等还原;
③电解法;
④热分解法。
选用最佳方法将下列金属从其化合物中还原出来:
-
(1) 铁、锌、铜等中等活泼金属。
-
(2) 钠、镁、铝等活泼或较活泼金属。
-
(3) 汞、银等不活泼金属。
-
(4) 钾、铷、铯、钛等金属通常还原方法是。
下列物质的制备过程或方法描述正确的是( )
A . 海水提镁过程中常选用烧碱做沉淀剂
B . 煤经过气化可制得水煤气
C . 利用空气吹出法得到溴蒸汽,经冷凝后可得纯溴
D . 电解熔融氯化铝可得到金属铝
下列说法正确的是( )
A . 煤的气化液化、海水制溴等过程中都包含化学变化
B . 可通过电解熔融MgCl2来制取金属镁,也能通过电解熔融AlCl3来制取金属铝
C . 铝热剂、胆矾、水玻璃、双氧水、明矾均为混合物
D . Na2O2、MgCl2、NaOH、SiO2 均为含共价键的离子化合物
下列有关判断正确的是( )
A . 金属阳离子被还原,一定会得到金属单质
B . 金属冶炼过程中,金属化合物得到电子发生氧化反应
C . 海带中含有碘单质,能使淀粉变蓝
D . 通过铝热反应可以在野外焊接钢轨
下列有关金属的说法正确的是( )
A . 生铁是合金,钢是纯净的金属
B . 纯金属与其合金相比,一般具有更低的熔点
C . 活泼金属常采用电解熔融化合物的方法制备
D . 铝的化学性质活泼,不宜在生产、生活中广泛应用
最近更新



