金属冶炼的一般原理 知识点题库
化学与社会、生活密切相关,下列说法正确的是( )
A . Fe3O4俗称铁红,常做红色油漆和涂料
B . 燃料电池的燃料都在负极发生氧化反应
C . “歼﹣20”飞机上使用的碳纤维是一种新型的有机高分子材料
D . 工业上通常用电解Na、Mg、Al对应的氯化物制取该三种金属单质
下列关于常见物质的工业冶炼说法正确的是( )
A . 工业制金属钠:电解饱和食盐水
B . 工业炼铁:需要用到的原料有铁矿石、焦炭、空气和生石灰
C . 冶炼镁:将六水合氯化镁晶体在一定条件下加热得到无水氯化镁,电解熔融氯化镁,可以得到金属镁
D . 硫酸工业:在氧气充足的情况下,从接触室进入吸收塔的气体中不可能含有SO2
下列说法中,不正确的是( )
A . 金属的冶炼,就是利用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来
B . 冶炼金属时,必须加入一种物质作为还原剂
C . 金属由化合态变为游离态,都是被还原
D . 金属单质被发现和应用得越早,其活动性一般越弱
分析推理是化学学习的方法之一.下列实验推理中,正确的是( )
A . 金属的冶炼方法与金属的活泼性有很大关系,所以银和汞可以用热分解的方法冶炼
B . 钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜
C . 工业上电解熔融氯化镁可制得金属镁,所以工业上电解熔融氯化铝可制得铝
D . 将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼
生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述正确的是( )
A . “加碘盐”、“高钙牛奶”、“富硒营养品”等食用品中的碘、钙、硒是指单质
B . “酸可以除锈”,“热的纯碱溶液去油污”都是发生了化学变化
C . 医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质
D . 铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝
常温下钛的化学活性很小,在较高温度下可与多种物质反应。
-
(1) 工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:

① 沸腾氯化炉中发生的主要反应为:。
② 已知:Ti (s)+2Cl2(g)=TiCl4(l) △H=akJ/mol;
2Na(s)+Cl2(g)=2NaCl(s) △H=bkJ/mol;
Na(s) = Na (l) △H=ckJ/mol
则TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s) △H=kJ/mol
③ TiCl4遇水强烈水解,写出其水解的化学方程式。
-
(2) TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示。二氧化钛电极连接电源极,该极电极反应为。

-
(3) 若以二甲醚(CH3OCH3)、空气、氢氧化钾溶液为原料,多孔石墨为电极构成的燃料电池提供上述电解的电源,则该电池工作时负极的电极反应式为。
古籍中对“鍮石”有如下记载:“鍮石,自然铜之精也。今炉甘石(主要成分为碳酸锌)炼成者,假鍮也。崔昉曰:铜一斤,炉甘石一斤,炼之成鍮石(假鍮)。”“水银坠地,鍮石可引上。”下列叙述错误的是( )
A . 假鍮是一种合金
B . 炉甘石中的碳酸锌在冶炼中被还原
C . 可以用盐酸鉴别真假“鍮石”
D . 分别用硫磺和“鍮石”处理“水银坠地”的原理是相同的
根据题目信息完成下列方程式。
-
(1) 钛(Ti)因为具有神奇的性能越来越引起人们的关注。地壳中含钛铁矿石之一是金红石(TiO2),目前大规模生产的方法是:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为:;
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。写出此反应的化学方程式:。
-
(2) 用100mL 0.1mol/L的NaOH溶液吸收224mLCO2气体(标准状况),恰好完全吸收。再将所得溶液加入100mL 0.1mol/L氢氧化钙溶液中。请写出所得溶液与氢氧化钙溶液反应的离子方程式:。
下列各种金属冶炼方法中,不能制得相应金属的是( )
A . 加热氧化汞
B . 氧化铁和铝粉高温共热
C . 电解熔融氯化钠
D . 高温煅烧碳酸钙
下列说法错误的是( )
A . 门捷列夫根据元素的性质随着相对原子质量递增呈现周期性变化规律,制出了第一张元素元素周期律
B . 侯氏制碱法的原理是将CO2通入氨的NaCl饱和溶液中,使NaHCO3析出,NaHCO3受热分解生成Na2CO3 , NaHCO3和Na2CO3在食品工业上都有着广泛的应用
C . 石灰乳与海水混合,过滤得Mg(OH)2 , 将其溶于盐酸,再蒸发结晶得到MgCl2 , 电解熔融MgCl2可得到金属镁
D . 工业炼铁、从海水中提取镁、制玻璃、水泥过程中都需要用到石灰石
下列冶炼金属的方法错误的是( )
A . 电解熔融氯化铝制铝
B . 加热氧化银制银
C . CO还原铁矿石制铁
D . 电解熔融氯化钠制钠
山西南部中条山地区采矿炼铜历史悠久。黄铜矿[主要成分是 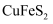 ,含少量氯磷灰石
,含少量氯磷灰石  等]为原料的火法炼铜主要流程如下:
等]为原料的火法炼铜主要流程如下:
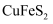 ,含少量氯磷灰石
,含少量氯磷灰石  等]为原料的火法炼铜主要流程如下:
等]为原料的火法炼铜主要流程如下: 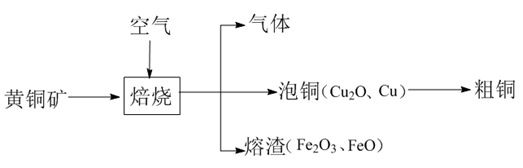
已知:氯磷灰石高温下易被氧化为  。某化学兴趣小组以黄铜矿为原料进行如下实验探究。请根据题意回答相关问题:
。某化学兴趣小组以黄铜矿为原料进行如下实验探究。请根据题意回答相关问题:
-
(1) 燃烧碘量法测定黄铜矿中硫元素的含量。将
 矿样与足量
矿样与足量  混合,以氮气为载气,在1250℃左右高温炉中加热,将产生的
混合,以氮气为载气,在1250℃左右高温炉中加热,将产生的  气体用含淀粉及碘化钾的稀硫酸溶液吸收,同时连续用
气体用含淀粉及碘化钾的稀硫酸溶液吸收,同时连续用 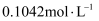 的
的 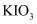 标准溶液缓慢滴定。装置如图所示(
标准溶液缓慢滴定。装置如图所示( 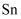 的
的 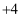 价化合物比
价化合物比 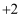 价稳定)。
价稳定)。 
①酸性高锰酸钾溶液的作用是。
②滴定过程中涉及反应有:
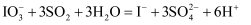 、(写离子方程式),终点现象为。
、(写离子方程式),终点现象为。③滴定至终点时,消耗标准液体积
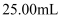 ,矿样中硫元素的质量百分含量为(结果保留两位有效数字),若
,矿样中硫元素的质量百分含量为(结果保留两位有效数字),若  不通过
不通过 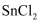 ,则测定结果会(填“偏高”、“偏低”、“不影响”)。
,则测定结果会(填“偏高”、“偏低”、“不影响”)。 -
(2) 利用如下装置制取粗铜。
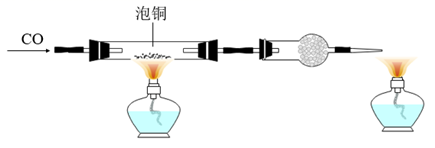
实验开始时的操作依次为(填写序号)。
①检查装置的气密性 ②通入
 气体 ③收集
气体 ③收集  并检验其纯度 ④组装仪器 ⑤点燃酒精灯 ⑥加装药品
并检验其纯度 ④组装仪器 ⑤点燃酒精灯 ⑥加装药品 -
(3) 由熔渣制得绿矾
 的流程如下(已知
的流程如下(已知  难溶于水)。
难溶于水)。 
步骤①溶解熔渣选用的试剂最好是,步骤②加入
 的目的是将
的目的是将  还原(硫元素被氧化为
还原(硫元素被氧化为  ),发生反应的离子方程式为,步骤③的系列操作为、(用乙醇)洗涤、干燥。
),发生反应的离子方程式为,步骤③的系列操作为、(用乙醇)洗涤、干燥。
下列有关工业生产的叙述中正确的是( )
A . 电解氯化钠溶液可得到金属钠
B . 光照氯气和氢气的混合物生产盐酸
C . 从铝土矿到铝单质过程中未涉及氧化还原反应
D . 工业接触法制硫酸的主要设备有沸腾炉、接触室、吸收塔
下列说法正确的的是( )
A . 用电解饱和食盐水制取金属钠
B . 用澄清石灰水可鉴别Na2CO3和NaHCO3溶液
C . 饱和碳酸钠溶液中通入过量CO2 , 最终生成白色沉淀
D . 除去碳酸氢钠固体中的少量碳酸钠,可用加热的方法
已知X、Y、Z三种元素均为短周期主族元素,X、Z同周期,X、Z的最低价离子分别为X2-和Z- , Y2+和Z-具有相同的电子层结构,下列说法正确的是( )
A . 原子半径:Z>X
B . X、Y两种元素形成的化合物YX为共价化合物
C . Z的单质与X的最简单氢化物反应可得到X的单质
D . 工业上常采用电解Y的氯化物的水溶液来获得Y的单质
下列关于金属冶炼的说法正确的是( )
A . 金属的冶炼都是把金属单质从其矿物中分离出来
B . 古代火烧孔雀石炼铜的方法属于热还原法中的焦炭法
C . 工业上可用电解熔融态的MgCl2、AlCl3来制备Mg、Al
D . 利用该铝热反应 炼铁,1mol氧化剂参加反应转移9NA个电子
炼铁,1mol氧化剂参加反应转移9NA个电子
 炼铁,1mol氧化剂参加反应转移9NA个电子
炼铁,1mol氧化剂参加反应转移9NA个电子
下列反应原理中,不符合工业冶炼金属实际情况的是( )
A . 2HgO 2Hg+O2↑
B . Cu2S+O2
2Hg+O2↑
B . Cu2S+O2 2Cu+SO2↑
C . 2AlCl3
2Cu+SO2↑
C . 2AlCl3 2Al+3Cl2↑
D . 4CO+Fe3O4
2Al+3Cl2↑
D . 4CO+Fe3O4 3Fe+4CO2
3Fe+4CO2
 2Hg+O2↑
B . Cu2S+O2
2Hg+O2↑
B . Cu2S+O2 2Cu+SO2↑
C . 2AlCl3
2Cu+SO2↑
C . 2AlCl3 2Al+3Cl2↑
D . 4CO+Fe3O4
2Al+3Cl2↑
D . 4CO+Fe3O4 3Fe+4CO2
3Fe+4CO2
下列冶炼金属的方法错误的是( )
A . 火法炼 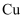 B . 电解食盐水炼
B . 电解食盐水炼 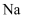 C . 铝热法炼
C . 铝热法炼  D . 热分解法炼
D . 热分解法炼 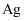
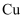 B . 电解食盐水炼
B . 电解食盐水炼 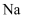 C . 铝热法炼
C . 铝热法炼  D . 热分解法炼
D . 热分解法炼 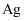
工业上冶炼钠、银、铁,常采用的方法分别是( )
A . 电解法、热还原法、热分解法
B . 电解法、 热分解法、热还原法
C . 热分解法、热还原法、电解法
D . 热还原法、热分解法、电解法
“劳动创造幸福,实干成就伟业”。下列劳动项目所涉及的化学知识正确的是( )
选项 | 劳动项目 | 化学知识 |
A | 用明矾处理较浑浊的天然水 | 明矾主要起净水和杀菌作用 |
B | 在盐田中晾晒海盐,得到粗盐 | NaCl的溶解度随温度变化不大 |
C | 工业上用FeCl3溶液刻蚀印刷电路板 | 利用还原性:Fe>Cu |
D | 利用含小苏打的发酵粉烘焙蛋糕 | 小苏打是碳酸钠 |
A . A
B . B
C . C
D . D
最近更新



