氨的性质及用途 知识点题库
①氨可用作制冷剂; ②可用铝制容器盛装浓盐酸;
③漂粉精可用作游泳池的消毒剂; ④铁红常用于制红色油漆和涂料;
⑤SO2常用于漂白纸浆、草帽及一些食物 ⑥明矾常用于净水.
-
(1)
NH3 是制碱工业中不可缺少的重要物质.继侯德榜“联合制碱法”后,上世纪50年代某些化工专家开始研究有机胺制碱法,其工艺流程如下:

已知:NR3+CO2+NaCl+H2O═NaHCO3+NR3•HCl,NR3+HCl═NR3•HCl,且NR3•HCl 易溶于有机溶剂.
①操作Ⅰ名称为 ;
②某实验小组同学查阅资料知,有机溶剂和有机胺沸点差别较大,现欲将A中各成分进行分离,请写出除了导管、酒精灯、牛角管、锥形瓶外,该分离操作所需的玻璃仪器名称 ;
-
(2)
N2 在化工生产、农业、医疗、航天航空等领域用途广泛.现提供以下装置(连接仪器略去):

①某化学兴趣小组甲同学欲用加热NaNO2和NH4Cl的浓溶液制得N2 , 应该选择的发生装置是 ,检验该发生装置气密性的操作为 ;
②在加热条件下,用NH3还原CuO可制得N2 , 同时获得铜粉,此反应的化学方应方程式是 .乙同学用此法制得干燥、纯净的N2 , 且需要的NH3以生石灰和浓氨水作原料.按气流从左到右,整套装置的连接顺序是 (填写字母序号);最后一个装置中试剂的作用是

-
(1) 下列有关NH3的说法中,错误的是__________(双选)。A . 工业合成NH3需要在高温高压下进行 B . NH3可用来生产碳铵和尿素等化肥 C . NH3可用浓硫酸或无水氯化钙干燥 D . NH3受热易分解,须置于冷暗处保存
-
(2) NH3易于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为mol.L-1。
-
(3) 氨气在氧化炉中所发生反应的化学方程式为。
-
(4) “吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为:Na2CO3+2NO2=NaNO3++CO2 (请填写完成化学方程式)。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2 , 则混合气体中NO和NO2的物质的量之比为。

 4NH3+3O2
C . 该过程中涉及极性键和非极性键的断裂与生成
D . 在该合成氨反应条件下,每转移2NA个电子需要22.4L的H2O
4NH3+3O2
C . 该过程中涉及极性键和非极性键的断裂与生成
D . 在该合成氨反应条件下,每转移2NA个电子需要22.4L的H2O
| 选项 | 性质 | 用途 |
| A | 氧化铁呈红棕色 | 红色涂料 |
| B | 氧化铝熔点很高 | 耐火材料 |
| C | 浓硫酸具有脱水性 | 干燥剂 |
| D | 液氨汽化时要吸收大量的热 | 制冷剂 |
 或性质实验
或性质实验  装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是
装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是 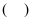
| 选项 | Ⅰ中的物质 | Ⅱ中收集的气体 | Ⅲ中的物质 | |
| A | Cu和稀硝酸 | NO | NaOH溶液 | |
| B | 浓盐酸和 | | NaOH溶液 | |
| C | 亚硫酸钠和浓硫酸 | | 品红溶液 | |
| D | 浓氨水和CaO | | 酚酞溶液 |
-
(1) 工业上制备氨气反应的化学方程式
-
(2) 铜和浓硫酸发生反应的化学方程式
-
(3) 氨气催化氧化生成一氧化氮的化学方程式
-
(4) 工业上制备漂白液发生反应的离子方程式
-
(5) 将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式
 通入
通入 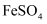 溶液中
B .
溶液中
B .  通入的
通入的 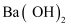 溶液中
C .
溶液中
C .  通入
通入 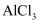 溶液中
D .
溶液中
D .  通入
通入  溶液中
溶液中
①氨水和液氨不同,氨水是由多种粒子组成的,液氨的组成中只有氨分子
②水泥、玻璃、水晶饰物都是硅酸盐制品
③向铜与浓硫酸反应后的溶液中加水稀释,溶液变蓝,则证明产物有Cu2+生成
④SiO2是酸性氧化物,它不能与任何酸发生反应
⑤铵盐受热分解一定都会产生氨气
⑥可用湿润的淀粉-KI试纸鉴别红棕色的Br2蒸气和NO2气体
| 选项 | 实验 | 现象 | 结论 |
| A | 蔗糖中滴加浓硫酸并不断搅拌 | 产生黑色蓬松多孔固体 | 浓硫酸具有吸水性 |
| B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
| C | 炭粉中加入浓硝酸并加热,导出的气体通入少量澄清石灰水中 | 有水红棕色气体产生,石灰不变浑浊 | 有NO2和CO2产生 |
| D | 向含I-的无色溶液中滴加少量新加制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 还原性:Cl->I- |