气体摩尔体积 知识点题库
下列物理量与所对应的单位不正确的是( )
A . n:mol
B . M:g•mol﹣1
C . NA:个
D . Vm:L•mol﹣1
设NA为阿伏加德罗常数的值.下列说法中,正确的是( )
A . 标准状况下,22.4L的NO2和CO2混合气体中含有的氧原子数为4NA
B . 密闭容器中,46gNO2和N2O4的混合气体所含分子个数为NA
C . 常温常压下,22.4L的液态水含有2.24×10﹣8NA个OH﹣
D . 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
下列指定微粒的数目相等的是( )
A . 等物质的量的水与重水含有的中子数
B . 等质量的乙烯和丙烯中含有的共有电子对数
C . 同温、同压、同体积的CO和NO含有的质子数
D . 等物质的量的铁和铝分别与足量氯气完全反应时转移的电子数
用NA代表阿伏加德罗常数,下列说法正确的是( )
A . 1 mol Fe与足量的稀盐酸完全反应,铁所失去的电子总数为3NA
B . 标准状况下,1mol水的体积约为22.4 L
C . 0.012kg12C所含碳原子数即为阿伏加德罗常数
D . 1molAl与足量NaOH溶液反应转移电子数为2NA
下列说法正确的是( )
A . 22.4 L·mol-1就是气体摩尔体积
B . 物质的量浓度为0.5 mol·L-1的MgCl2溶液中,含有Cl-个数为NA
C . 标准状况下,将33.6 L HCl溶于水形成1 L溶液,其物质的量浓度是1.5 mol·L-1
D . 从1 L 0.5 mol·L-1 NaCl溶液中取出100 mL,其物质的量浓度为0.05 mol·L-1
设NA为阿伏加罗常数的数值,下列说法正确的是()
A . 常温常正下,22.4LCO2所含的原子数为3NA
B . 1molNa2O2固体中阳离子和阴离子总数为3NA
C . 14g乙烯和乙烷混合气体中的碳原子数为NA
D . 2L1mol/L的盐酸中所含HCl分子数约为2NA
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 常温常压下,20g氖气所含有的原子数目为0.5NA
B . 2.8铁粉与50mL4 mol·L-1盐酸完全反应转移电子的数目为0.1NA
C . 标准状况下,22.4 LSO2和SO3混合物中含有的硫原子数目为0.1NA
D . 28g的C2H4和N2混合气体中含有的原子数为2NA
用NA表示阿伏加德罗常数的数值,下列说法中不正确的是( )
A . 20gD2O含有的电子数为10NA
B . 标准状况下,22.4LCl2通入足量NaOH溶液中,完全反应时转移的电子数为2NA
C . 1L0.1mol·L-1NH4NO3溶液中的氮原子数为0.2NA
D . 25℃时,1.0LpH=12的NaClO溶液中由水电离出的OH-的数目为0.01NA
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 常温下,1mol—OH所含的电子数目为9NA
B . 常温下,在16g 18O2中含有NA个氧原子
C . 1 mol乙烷中含有C—H的键数为7NA
D . 标准状况下,11.2LSO2与足量O2反应生成SO3分子数 0.5NA
标准状况下11.2LCH4在空气中完全燃烧,请完成下列问题:
-
(1) 写出该反应的化学方程式;
-
(2) 计算标准状况下11.2LCH4的质量;
-
(3) 计算生成CO2的质量。
下列说法正确的是( )
A . 摩尔是一种国际基本物理量
B . 氧气的摩尔质量为32 g
C . H2的气体摩尔体积约为22.4 L
D . 1 mol H2O约含有6.02×1023个水分子
下列说法正确的是( )
A . 1mol氧气的质量是16g,它所占的体积是22.4L
B . H2O的摩尔质量为18g
C . 1mol任何物质都含有约6.02×1023个分子
D . 标准状况下,以任意比例混合的H2和CO2混合物22.4L,含有的分子数为NA
设NA为阿伏加德罗常数的值( )
A . 标准状况下,将22.4LCl2通入水中发生反应,转移的电子数为NA
B . 常温常压下,48gO2与O3混合物含有的氧原子数为3NA
C . 将78gNa2O2与过量CO2反应转移的电子数为2NA
D . 标准状况下,18gD2O中所含电子数为10NA
设NA是阿伏加德罗常数的值,下列说法正确的是( )
A . 28g乙烯和环丙烷的混合气体中所含原子总数为6NA
B . 92.0g甘油(丙三醇)中含有羟基数为2.0NA
C . 1mol的羟基与1mol的氢氧根离子所含电子数均为9NA
D . 标准状况下,2.24L己烷含有分子的数目为0.1NA
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物  和
和  ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。
 和
和  ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。
-
(1) E元素在周期表中的位置。将B过量的最高价氧化物通入E的含氧酸盐溶液中,可以观察到的现象为。
-
(2)
 分子中存在的,不同于
分子中存在的,不同于  中的化学键被称为。用
中的化学键被称为。用  和稀硫酸浸泡废印刷电路板可溶解其中的
和稀硫酸浸泡废印刷电路板可溶解其中的 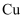 ,试写出反应的离子方程式。
,试写出反应的离子方程式。
-
(3)
 和入足量的水充分反应,生成气体的体积为(标准状况下).
和入足量的水充分反应,生成气体的体积为(标准状况下).
设  为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A . 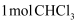 含有
含有 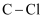 键的数目为
键的数目为 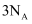 B .
B .  的盐酸含有阴离子总数为
的盐酸含有阴离子总数为  C .
C . 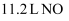 与
与 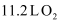 混合后的分子数目为
混合后的分子数目为  D .
D .  与足量
与足量  反应生成的
反应生成的  分子数目为
分子数目为 
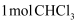 含有
含有 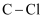 键的数目为
键的数目为 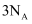 B .
B .  的盐酸含有阴离子总数为
的盐酸含有阴离子总数为  C .
C . 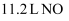 与
与 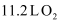 混合后的分子数目为
混合后的分子数目为  D .
D .  与足量
与足量  反应生成的
反应生成的  分子数目为
分子数目为 
下列说法中,正确的是( )
A . 22.4L N2中一定含有2molN原子
B . 18g H2O在标准状况下的体积约为22.4L
C . 在标准状况下,20mLNH3和60mLO2所含分子个数比为1:3
D . 80g NaOH溶解在1L水中,所得溶液的物质的量浓度为2mol/L
物质的量是联系宏观的和微观的桥梁。
-
(1) 标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为g。
-
(2) 将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取mL的浓硫酸。
)=mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取mL的浓硫酸。
-
(3) 某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1 , 溶液中c(K+)=。
)=0.016mol·L-1 , 溶液中c(K+)=。②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为。
Cl2与过量NH3反应的化学方程式为3Cl2+8NH3=6NH3Cl+N2.下列叙述正确的是( )
A . 1molN2的体积为22.4L
B . Cl2的摩尔质量为71g·mol-1
C . 1molNH3的质量为17g·mol-1
D . 22.4LNH3物质的量为1mol
气体摩尔体积的大小主要取决于( )
A . 分子数目
B . 分子间距
C . 分子大小
D . 分子种类
最近更新



