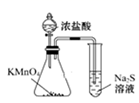
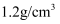氯水、氯气的漂白作用 知识点题库
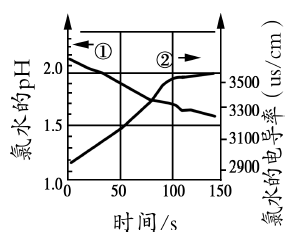
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;第二份与稀盐酸混合,立即产生大量无色气体;第三份滤液加热,看到滤液变浑浊且有大量无色气体产生.经检测,上述实验中产生的无色气体均为CO2 . 依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有( )


-
(1) 制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为。
-
(2) 装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象。
-
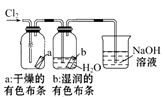
(3) 装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入(选填表中字母)。
①
②
③
a
干燥的有色布条
碱石灰
湿润的有色布条
b
干燥的有色布条
硅胶
湿润的有色布条
c
湿润的有色布条
浓硫酸
干燥的有色布条
d
湿润的有色布条
无水氯化钙
干燥的有色布条
-
(4) 设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装置E中,振荡;观察到的现象是,则说明溴的非金属性大于碘。
-
(5) 有同学提出该实验方案仍有不足,请说明其中的不足及后果。
①;②。
①钠、氢气都能在氯气中燃烧生成白色烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
-
(1) i.某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl2 , 其中含有少量水蒸气。 请回答下列问题:
分别描述B、C装置中的现象;。结合化学方程式及物质性质说明B、C装置中现象不同的原因 。
-
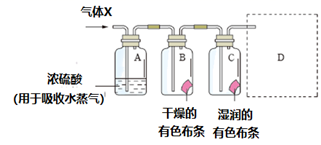
(2) Cl2是有毒气体,为了防止多余Cl2污染空气,可以在D处用如图装置进行尾气处理,用化学方程式表示该原理。气体应该由装置中的(填“a”或“b”)管通入。
-
(3) ii.为验证Cl2、Fe3+、I2三者氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器己略去,气密性已检验)。 查阅资料:Fe3+遇KSCN溶液变红;I2易溶于CCl4 , 且显紫色。
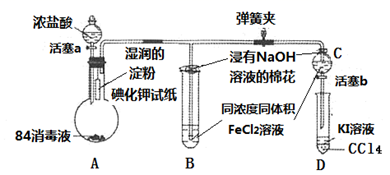
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B中溶液红色加深,关闭活塞a。
Ⅳ.……
①A中产生黄绿色气体,写出A中发生反应的离子方程式。
②验证氯气的氧化性强于碘单质的实验现象是。
③B中溶液发生反应的离子方程式是。
④为验证Fe3+的氧化性强于碘单质,过程Ⅳ的操作和现象是,对应的离子方程式是。
⑤浸有氢氧化钠溶液的棉花作用是。
⑥过程Ⅲ实验的目的是。

-
(1) ①盛装浓盐酸的仪器名称为,盛装二氧化锰的仪器名称为。
②请写出装置A中发生反应的化学方程式。
③标准状况下,上述反应每生成2.24L氯气,转移电子的物质的量为mol。
-
(2) 要将C装置接入B和D之间,正确的接法是:a→→→d。
-
(3) 实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为。
-
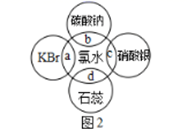
(4) 氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图2所示四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
①能证明氯水具有漂白性的是(填“a”“b”“c”或“d”)。
②c过程中的现象是。
 ,它具有氧化漂白作用。下列物质中漂白原理与过氧乙酸不同的是( )
,它具有氧化漂白作用。下列物质中漂白原理与过氧乙酸不同的是( )
-
(1) 氢键是微粒间的一种常见作用力,如存在于醋酸分子间(
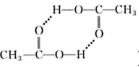 )和硝酸分子内(
)和硝酸分子内(  )等。已知邻氨基苯甲醛(
)等。已知邻氨基苯甲醛( 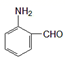 )的熔点为39℃,对氨基苯甲醛(
)的熔点为39℃,对氨基苯甲醛( 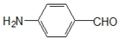 )的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因。
)的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因。
-
(2) 请用一个化学方程式并结合适当的文字说明HClO、H2CO3和HCO
 酸性的强弱。
酸性的强弱。
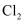 防止污染环境
C . 漂白粉的有效成分为
防止污染环境
C . 漂白粉的有效成分为 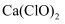 ,可用作游泳池的消毒剂
D . 磁性氧化铁具有磁性,其主要成分为
,可用作游泳池的消毒剂
D . 磁性氧化铁具有磁性,其主要成分为 
 B .
B .  C .
C .  D .
D . 
| | | | |
| 图1 | 图2 | 图3 | 图4 |
 )用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
)用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
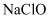 )回答下列问题:
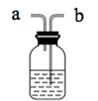
)回答下列问题:84消毒液 (有效成分) (规格) (质量分数)25% (密度) |
-
(1) 用氯气制备“84”消毒液的离子方程式为,如图是某“84”消毒液的标签,
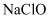 的物质的量浓度为
的物质的量浓度为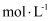 (保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、。
(保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、。
-
(2) 资料显示“84”消毒液不能与洁厕灵(含
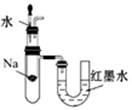
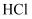 )混合使用,对此某小组开展如图所示的研究。
)混合使用,对此某小组开展如图所示的研究。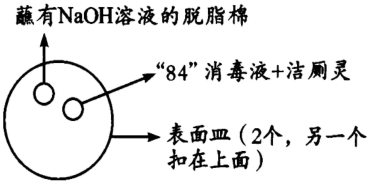
①两表面皿之间充满黄绿色气体。则“84”消毒液与洁厕灵反应的化学方程式为;
 的作用是。
的作用是。②生活中“84”消毒液不能与洁厕灵混合使用的原因是。
-
(3) “84”消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是。

-
(1) 如图为氯及化合物的“价-类”二维图。物质A为、物质B为(填化学式)。

-
(2) 1774年,舍勒制得
 , 请写出实验室制取氯气的化学方程式。
, 请写出实验室制取氯气的化学方程式。
-
(3) HOF与HClO结构相似,写出HOF的电子式。但HOF更不稳定,更易分解,其反应为
 , 该反应属于。
, 该反应属于。A.化合反应 B.分解反应 C.置换反应 D.氧化还原反应
-
(4)
 与
与 均能用于自来水消毒。标准状况下,
均能用于自来水消毒。标准状况下, 和
和 组成的混合气体的密度为
组成的混合气体的密度为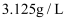 , 则混合气体的摩尔质量为
, 则混合气体的摩尔质量为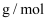 , 混合气体中
, 混合气体中 的体积分数为(用分数表示)。
的体积分数为(用分数表示)。