胶体的性质和应用 知识点题库
-
(1) 配制一定物质的量浓度溶液时,会使所配溶液浓度偏高的是(填序号)
a.容量瓶在使用前内壁沾有水珠 b.定容时俯视读刻度
c.未冷却至室温就注入容量瓶并马上定容 d.向容量瓶转移液体时有少量流出
-
(2) 容量瓶上标有(填序号)
①温度 ②浓度 ③容量 ④质量 ⑤刻度线 ⑥酸式或碱式
-
(3) 将4g NaOH 固体溶解在10mL的水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度是.
-
(4) 溶液、胶体和浊液这三种分散系的本质区别是(填序号),
A.是否是大量分子或离子的集合体 B.分散质粒子的大小
C.是否能通过滤纸 D.是否均一、透明、稳定
光束通过Fe(OH)3胶体时,可看到光亮的通路,这种现象叫.
-
(5) 实验室制取氯气的反应方程式是:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O,在此反应中,被氧化的元素是,还原产物是.
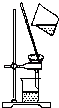 过滤
B .
过滤
B . 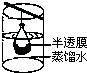 渗析
C .
渗析
C . 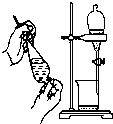 萃取
D .
萃取
D . 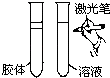 丁达尔效应
丁达尔效应
| 选项 | 实验目的 | 实验操作 |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| B | 证明淀粉水解后产生葡萄糖 | 淀粉溶液加稀硫酸,水浴加热一段时间后,加新制的Cu(OH)2悬浊液,加热 |
| C | 配制 0.1000 mol/L的NaOH溶液 | 称取1.0 g NaOH固体于烧杯中,加人少量蒸馏水溶解,转移至250mL 容量瓶中定容 |
| D | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
-
(1) Ⅰ.现有7种物质:①Na、②FeCl3溶液、③稀盐酸、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl晶体。
属于非电解质的是;上述状态下的物质能导电的电解质有 (填序号)。
-
(2) 制备⑥的方法是:在小烧杯中加入40mL蒸馏水,加热至沸腾后,向烧杯中加入5至6滴FeCl3饱和溶液,继续煮沸至液体呈色,即可制得
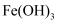 胶体。区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是。
胶体。区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是。
-
(3) FeCl3在水溶液中的电离方程式是。
-
(4) Ⅱ.完成下列问题
在标准状况下,33.6LCH4的质量是。
-
(5) 相同质量的SO2和SO3 , 氧原子数之比为。
选项 | 目的 | 实验操作 |
A | 测量氯水的pH | 用玻璃棒蘸氯水点在pH试纸中部,并与标准比色卡对照 |
B | 制取Fe(OH)3胶体 | 将FeCl3饱和溶液煮沸 |
C | 将海水淡化为饮用水 | 将海水蒸馏 |
D | 实验室制备氨气 | NH4Cl稀溶液与消石灰共热 |
 是一种重要的盐,主要用于金属蚀刻、污水处理等。同学们在实验室中进行了与
是一种重要的盐,主要用于金属蚀刻、污水处理等。同学们在实验室中进行了与 有关的实验。
有关的实验。
-
(1) 实验I:配制
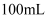

 溶液下
溶液下
①需要
 固体的质量是。
固体的质量是。②步骤C中玻璃棒的作用是。
③步骤F的名称是,若仰视刻度线,会导致所配溶液的浓度(填“偏大”、“偏小”或“无影响”)。
④步骤G结束后,将所配溶液装瓶、贴标签,请将标签内容填写在下图中。

-
(2) 实验II:探究
 的性质
的性质将少量
 溶液滴入一定量的
溶液滴入一定量的 溶液中,观察到的现象是,有关反应的离子方程式是。
溶液中,观察到的现象是,有关反应的离子方程式是。 -
(3) 实验III:制备
 胶体
胶体将5~6滴
 饱和溶液滴入一定量的沸水中,继续煮沸一段时间,停止加热,有关反应的化学方程式是,用红色激光笔照射
饱和溶液滴入一定量的沸水中,继续煮沸一段时间,停止加热,有关反应的化学方程式是,用红色激光笔照射 胶体,观察到的现象是。
胶体,观察到的现象是。
|
|
|
|
A.过滤 | B.渗析 | C.萃取 | D.丁达尔效应 |







