阿伏加德罗定律及推论 知识点题库
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的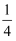 )、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央.则原来H2、O2的体积之比可能为
)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央.则原来H2、O2的体积之比可能为

现有m g某气体,由双原子分子构成,摩尔质量为M g•mol﹣1
. 若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为 mol.
(2)该气体所含原子总数为 个.
(3)该气体在标准状况下的体积为 L.
(4)该气体在标准状况下的密度为 g/L.
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为 mol/L.
下列说法不正确的是( )
A . 干燥的氯气能使湿润的有色布条褪色
B . 影响气体体积大小的主要因素是微粒间的距离与微粒的大小
C . 汤姆生发现原子中存在电子,并提出了“葡萄干面包式”原子结构模型
D . 干冰升华的过程只需克服分子间作用力
下列关于0.3mol氧气和0.2mol臭氧气(O3)的说法正确的是( )
A . 原子数之比为3:2
B . 同温同压下密度比是2:3
C . 同温同压下质量比是3:2
D . 标准状况下体积比是2:3
对于相同物质的量的SO2和SO3 , 下列说法中正确的是( )
A . 硫元素的质量比为5:4
B . 任何情况下体积比均为1:1
C . 含有的O2、O3两分子数之比为1:1
D . SO2、SO3两分子数之比为1:1
标准状况下,a g气体A和b g气体B的体积相同,下列叙述正确的是( )
A . A和B的原子个数比是1:1
B . A和B的密度之比为b:a
C . A和B的摩尔质量比是a:b
D . A和B的分子数之比是b:a
标准状况下有①6.72L CH4②3.01×1023个HCl ③13.6g H2S ④0.2mol NH3四种气体,气体所占体积由小到大的顺序是(填序号,下同);所含氢原子数由小到大的顺序是.
-
(1) 同温同压下,有两瓶体积相等的CO和CO2 , 这两种气体中所含的分子数目之比为 ,质量比为。
-
(2) 在Cu + 2H2SO4(浓)
 CuSO4+ SO2↑+ 2H2O反应中,
CuSO4+ SO2↑+ 2H2O反应中,①是氧化剂。
②用双线桥标出该反应电子转移的方向和数目。
Cu + 2H2SO4(浓)
 CuSO4+ SO2↑+ 2H2O
CuSO4+ SO2↑+ 2H2O③若有2.4mol的H2SO4参与反应,生成标况下的二氧化硫气体 L,转移电子的数目为。(NA表示阿伏加德罗常数的值)
如图所示,相同状况下,分别用氯化氢和四种混合气体吹出体积相等的五个气球。A、B、C、D四个气球中所含原子数与氯化氢气球中所含原子数一定相等的是( ) 

A . 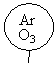 B .
B .  C .
C . 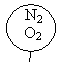 D .
D . 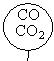
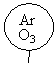 B .
B .  C .
C . 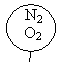 D .
D . 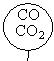
根据阿伏加德罗定律,下列说法中正确的是( )
A . 同温同压下两种气体的体积之比等于摩尔质量之比
B . 同温同压下两种气体的物质的量之比等于密度之比
C . 同温同压下两种气体的摩尔质量之比等于密度之比
D . 同温同压下两种气体的物质的量之比等于压强之比
同温同压下,分子数相同的任意两种气体,它们的( )
A . 所占体积相同
B . 密度相同
C . 原子数目相同
D . 体积都是22.4 L
质量相同的两种气体A、B,在同温、同压下,A的分子数比B多。下列说法正确的( )
A . A占的体积比B小
B . A的摩尔质量比B大
C . A的密度比B小
D . A的物质的量比B小
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
A . 体积比为8∶11
B . 分子个数之比为11∶12
C . 密度之比为8∶11
D . 原子个数之比为12∶11
-
(1) 0.5mol某固体A的质量是30g,A的摩尔质量为。
-
(2) 在同温同压同体积的条件下,H2与气体B的密度之比是1∶8,则B的相对分子质量为。
-
(3) 在25℃ 101kPa的条件下,同质量的CH4和C气体的体积之比是15∶8,则1摩尔C的质量为。
-
(4) .质量之比为8∶7∶6的三种气体SO2、CO、NO,其分子数之比为;氧原子数之比为;相同条件下的体积之比为。
-
(5) 4.8g碳在一定量的氧气中燃烧,反应后生成的气体质量为12.8g。则在标准状况下,生成物CO和CO2的体积比为。
三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是( )
A . 原子数目相等的三种气体,质量最大的是Z
B . 相同条件下,同质量的三种气体,气体密度最小的是Z
C . 若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1mol
D . 同温下,体积相同的两容器分别充2gY气体和4 gZ气体,则其压强比为1︰1
在 0℃、1.01×105 Pa 下,有关 H2、O2 的叙述错误的是( )
A . 等质量的两种气体,其体积比等于 16:1
B . 其密度之比等于 1:16
C . 等质量的两种气体,所含电子数之比等于1:1
D . 等体积的两种气体,其质量之比等于 1:16
相同温度和压强下,1molCO和1molCO2相比较,下列说法错误的是( )
A . 分子数相同,但原子数不同
B . 体积相同,但不一定是22.4L
C . 质子数不同,电子数也不同
D . 两者的密度相同
已知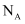 是阿伏加德罗常数的值,下列说法正确的是( )
是阿伏加德罗常数的值,下列说法正确的是( )
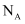 是阿伏加德罗常数的值,下列说法正确的是( )
是阿伏加德罗常数的值,下列说法正确的是( )
A . 常温下,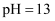 的
的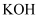 溶液中
溶液中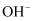 数目为
数目为 B . 56g
B . 56g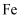 与足量硫粉充分反应转移电子数为
与足量硫粉充分反应转移电子数为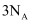 C .
C . 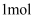
 和
和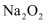 的混合物中所含阴离子数目为
的混合物中所含阴离子数目为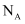 D . 标准状况下,2.24L
D . 标准状况下,2.24L 所含极性键数目为
所含极性键数目为
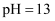 的
的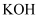 溶液中
溶液中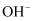 数目为
数目为 B . 56g
B . 56g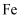 与足量硫粉充分反应转移电子数为
与足量硫粉充分反应转移电子数为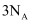 C .
C . 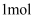
 和
和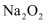 的混合物中所含阴离子数目为
的混合物中所含阴离子数目为 D . 标准状况下,2.24L
D . 标准状况下,2.24L 所含极性键数目为
所含极性键数目为
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,2.24LCCl4含有的分子数为0.1NA
B . 1mol铵根离子中含有的电子数为11NA
C . 工业制硫酸用6.4gSO2与过量空气反应制SO3转移电子0.2NA
D . 标况下,2.24L乙烷中含有碳氢键的数目为0.6NA
标准状况下,①6.72LNH3②1.204×1023个H2S③5.6gCH4④0.5molHCl,下列关系错误的是( )
A . 体积大小:④>③>①>②
B . 质量大小:④>③>②>①
C . 密度大小:④>②>①>③
D . 原子数目:③>①>④>②
最近更新



