物质的量与其浓度和气体摩尔体积的综合应用 知识点题库
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol.若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为 mol.
(2)该气体所含原子总数为 个.
(3)该气体在标准状况下的体积为 L.
(4)该气体溶于1L水中(不考虑反应),形成的溶液溶质的质量分数为 .
(5)该气体溶于水形成VL溶液,其溶液的物质的量浓度为 mol/L.
某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为  ②m g该硫原子的物质的量为
②m g该硫原子的物质的量为  mol
mol
③该硫原子的摩尔质量是aNA g ④a g该硫原子所含的电子数为16NA .
A . ①③
B . ②④
C . ①②
D . ②③
溶液中有0.2mol XO4﹣ , 加入0.3mol Na2SO3恰好反应,已知Na2SO3被氧化成Na2SO4 , 则还原产物中X的化合价为( )
A . 0
B . +1
C . +3
D . +4
将32g铜与100mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2的混合气体标准状况下的体积为11.2L,气体全部逸出后,向溶液中加入VmL n mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度为 mol/L.(结果须化简)
一定温度和压强下,用m g的CH4、CO2、O2、SO2四种气体分别吹出四个体积大小不同的气球,下列说法中正确的是( )
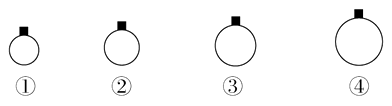
A . 气球②中装的是O2
B . 气球①和气球③中气体分子数相等
C . 气球①和气球④中气体物质的量之比为4∶1
D . 气球③和气球④中气体密度之比为2∶1
标准状况下将44.8LHCl气体溶于1L水中,所得盐酸溶液的密度为1.1g/cm3 , 该盐酸的物质的量浓度为( )
A . 2mol/L
B . 2.1mol/L
C . 2.2mol/L
D . 2.3mol/L
 是阿伏加德罗常数的值,下列说法正确的是( )
是阿伏加德罗常数的值,下列说法正确的是( )
A . 23 g Na在氧气中充分燃烧生成 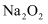 ,转移电子数为2
,转移电子数为2  B .
B . 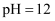 的NaOH溶液中,含有
的NaOH溶液中,含有 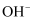 的数日为0.01
的数日为0.01  C . 电子数为
C . 电子数为  的
的  分子的质量为1.6g
D . 标准状况下,3.36 L的
分子的质量为1.6g
D . 标准状况下,3.36 L的 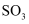 中含有氧原子的数目为0.45
中含有氧原子的数目为0.45 
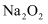 ,转移电子数为2
,转移电子数为2  B .
B . 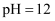 的NaOH溶液中,含有
的NaOH溶液中,含有 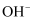 的数日为0.01
的数日为0.01  C . 电子数为
C . 电子数为  的
的  分子的质量为1.6g
D . 标准状况下,3.36 L的
分子的质量为1.6g
D . 标准状况下,3.36 L的 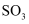 中含有氧原子的数目为0.45
中含有氧原子的数目为0.45 
下列叙述正确的是( )
A . 1mol任何气体的体积都为22.4 L
B . 1 mol任何物质在标准状况下所占的体积都为22.4 L
C . 标准状况下,1 mol水所占的体积是22.4 L
D . 标准状况下,22.4 L的任何气体的物质的量都是1 mol
已知某饱和溶液的以下条件:①溶液的质量、②溶剂的质量、③溶液的体积、④溶质的摩尔质量、⑤溶质的溶解度、⑥溶液的密度,其中不能用来计算该饱和溶液的物质的量浓度的组合是( )
A . ④⑤⑥
B . ①②③④
C . ①③⑤
D . ①③④⑤
由CH4和CO2组成的混合气体,标准状况下的密度为1.25 g·L-1 , 则该混合气体中CH4和CO2的体积比为( )
A . 2:1
B . 1:1
C . 4:3
D . 3:2
同温同压下,相同体积的SO2和CO2:①质量相等;②密度相等;③分子数相等;④氧原子数相等;⑤电子数相等,其中正确的是( )
A . ①②③④
B . ②③④⑤
C . ③④
D . ③⑤
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 1mol羟基(-OH)中所含的质子数为9NA
B . 标准状况下,22.4L单质溴所含有的原子数目为2NA
C . 100mL0.1mol•L-1NH4Cl溶液含NH  的数目是0.01NA
D . 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
的数目是0.01NA
D . 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
 的数目是0.01NA
D . 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
的数目是0.01NA
D . 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
设NA代表阿伏加德罗常数,下列说法正确的是( )
A . 0oC、101kPa下,11.2 L N2和O2的混合气体中所含原子数为NA
B . 18g H2O在标况下的体积为22.4 L
C . 物质的量浓度为2 mol/L的BaCl2溶液中,含有Cl-个数为4NA
D . 22.4 L氨气溶于水制得1 L氨水,氨水的物质的量浓度为1 mol·L-1
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C处分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等,下列说法正确的是( )

A . X的相对分子质量等于Y的相对分子质量
B . X的相对分子质量比Y的相对分子质量小
C . 气体的体积:V(X) >V(H2)>V(Y)
D . 物质的量:n(X)< n(H2) <n(Y)
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 100g质量分数为46%的CH3CH2OH溶液中所含氢原子数为6NA
B . 标准状况下,11.2LHF所含的原子总数为NA
C . 常温下,100mL1 mol∙L−1AlCl3溶液中Al3+离子总数等于0.1NA
D . 含1molNH4Cl的溶液中加入适量氨水使溶液呈中性,此时溶液中  数目为NA
数目为NA
 数目为NA
数目为NA
下列说法正确的是( )
A . 在常温常压下,11.2LN2含有的分子数为 0.5NA
B . 标准状况下,22.4LH2和O2的混合物所含分子数为NA
C . 标准状况下,18gH2O 的体积是 22.4L
D . 1molSO2的体积是 22.4L
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm-3,质量分数为ω,其中含N的物质的量为b mol。下列叙述中错误的是( )
A . 溶质的质量分数ω=  ×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
 ×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
×100%
B . 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C . 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D . 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
侯氏制碱法涉及的主要反应为  。
。  为阿伏加德罗常数的值,下列有关说法错误的是( )
为阿伏加德罗常数的值,下列有关说法错误的是( )
 。
。  为阿伏加德罗常数的值,下列有关说法错误的是( )
为阿伏加德罗常数的值,下列有关说法错误的是( )
A . 标准状况下,5.6L  的分子数为0.25
的分子数为0.25  B . 1个
B . 1个  晶胞的质量为
晶胞的质量为  C . 1L0.1
C . 1L0.1 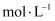
 溶液中NH
溶液中NH 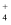 数目小于0.1
数目小于0.1  D . 反应消耗0.1
D . 反应消耗0.1 
 析出
析出  数目为0.1
数目为0.1 
 的分子数为0.25
的分子数为0.25  B . 1个
B . 1个  晶胞的质量为
晶胞的质量为  C . 1L0.1
C . 1L0.1 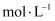
 溶液中NH
溶液中NH 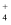 数目小于0.1
数目小于0.1  D . 反应消耗0.1
D . 反应消耗0.1 
 析出
析出  数目为0.1
数目为0.1 
标准状况下,V L某气体(此气体不与水反应)溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为  ,溶质的摩尔质量为
,溶质的摩尔质量为  ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为  ,溶液的体积为
,溶液的体积为  ,下列关系中正确的是( )
,下列关系中正确的是( )
 ,溶质的摩尔质量为
,溶质的摩尔质量为  ,溶质的质量分数为w,溶质的物质的量浓度为
,溶质的质量分数为w,溶质的物质的量浓度为  ,溶液的体积为
,溶液的体积为  ,下列关系中正确的是( )
,下列关系中正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
在加热条件下,  铜丝与
铜丝与  的硝酸恰好完全反应,产生一定量
的硝酸恰好完全反应,产生一定量 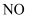 和
和  的混合气体(反应过程中溶液体积变化忽略不计)。
的混合气体(反应过程中溶液体积变化忽略不计)。
 铜丝与
铜丝与  的硝酸恰好完全反应,产生一定量
的硝酸恰好完全反应,产生一定量 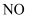 和
和  的混合气体(反应过程中溶液体积变化忽略不计)。
的混合气体(反应过程中溶液体积变化忽略不计)。
-
(1) 硝酸铜物质的量浓度为
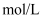 。
。
-
(2) 整个过程中被还原的硝酸物质的量为
 。
。
-
(3) 混合气体中
 的体积为
的体积为  。(标准状况下)
。(标准状况下)
最近更新



