化学键和分子间作用力的区别 知识点题库
下列物质的变化,破坏的主要是分子间力的是( )
A . 碘单质的升华
B . NaCl溶于水
C . 将金属Mg加热变为气态
D . NH4Cl受热分解
共价键、离子键、分子间作用力都是微粒间的作用力,下列物质中含有以上两种作用力的晶体是( )
A . SiO2
B . CCl4
C . NaCl
D . NA0H
下列说法正确的是( )
A . 利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料,可减少“白色污染”
B . 硅晶体的导电性介于导体与绝缘体之间,是一种重要的半导体材料,广泛应用于制造集成电路、光导纤维、太阳能电池板等
C . pH计不能用于酸碱中和滴定终点的判断
D . 2013年11月22日,中科院国家纳米科学中心宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
下列说法正确的是( )
①极性分子一定含有极性键,非极性分子一定含有非极性键
②极性分子中一定不含有非极性键,非极性分子中可能含有极性键
③N2O和CO2是互为等电子体,因此每个分子均含有2个π 键,且中心原子均为sp杂化
④丙酮的沸点为57℃高于丁烷的沸点为﹣0.5℃是由于丙酮分子间有氢键
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低与氢键有关.
A . ③⑤
B . ②④⑤
C . ②③④⑤
D . ①②③④⑤
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
(Ⅰ)在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
-
(1) 写出与
 分子互为等电子体的微粒(填1种)。
分子互为等电子体的微粒(填1种)。
-
(2) 水分子在特定条件下容易得到一个
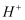 ,形成水合氢离子(
,形成水合氢离子(  )。下列对上述过程的描述不合理的是__________________。
A . 氧原子的杂化类型发生了改变 B . 微粒的形状发生了改变 C . 微粒的化学性质发生了改变 D . 微粒中的键角发生了改变
)。下列对上述过程的描述不合理的是__________________。
A . 氧原子的杂化类型发生了改变 B . 微粒的形状发生了改变 C . 微粒的化学性质发生了改变 D . 微粒中的键角发生了改变 -
(3)
 分子内的O-H键、分子间的范德华力和氢键从强到弱依次为
分子内的O-H键、分子间的范德华力和氢键从强到弱依次为
-
(4) (Ⅱ)胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
写出铜原子价电子层的电子排布式 ,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有 (填元素符号)。
-
(5) 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;以上过程中发生的离子反应方程式为:
;。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有。
-
(6) 实验过程中加入
 后可观察到析出深蓝色
后可观察到析出深蓝色  晶体。实验中所加
晶体。实验中所加  的作用是
的作用是
干冰气化过程中发生变化的是( )
A . 分子间作用力
B . 分子内共价键的极性
C . 分子内原子间距离
D . 分子的空间构型
下列说法正确的是( )
A . 冰和水晶都是分子晶体
B . 原子晶体一定是共价化合物
C . 某物质固态时不导电但在熔融状态下能导电,则该物质中一定含有离子键
D . 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力
下列有关化学键与晶体结构说法正确的是( )
A . 共价键的键能越大,分子晶体的熔、沸点越高
B . 离子化合物的熔点一定比共价化合物的高
C . 非金属元素组成的化合物一定是共价化合物
D . 含有阴离子的化合物一定含有阳离子
下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
A . 二氧化硅和铁分别受热熔化
B . 干冰和氯化铵分别受热变为气体
C . 液溴和苯分别受热变为气体
D . 食盐和葡萄糖分别溶解在水中
将下列晶体熔化:过氧化钠、二氧化硫、氯化铵、二氧化硅,需要克服的微粒间的相互作用①共价键 ②离子键 ③分子间作用力,符合题意的顺序是( )
A . ①②②③
B . ②①②③
C . ②③②①
D . ②③①③
下列说法正确的是( )
A . CaO与水反应过程中,有共价键的断裂和形成
B . H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大
C . KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物
D . 葡萄糖、二氧化碳和足球烯(C60)都是共价化合物,它们的晶体都属于分子晶体
下列各项中有关判断正确的是( )
A . ①醋酸除水垢 ②石油分馏 ③煤的气化 ④海水中提取碘,过程中只涉及物理变化的是②③
B . ①CH4 和C3H8 ②O2 和O3 ③35Cl 和37Cl ④H2 和D2 , 属于同位素的微粒组是③④
C . ①金刚石熔化②氯化氢溶于水③氢氧化钾熔化④冰融化,上述过程与化学键断裂无关的是①④
D . ①酒精 ②冰醋酸 ③硝酸钾 ④醋酸钠,上述物质溶于水时会破坏水的电离平衡,且属于强电解质的仅是④
下列每组物质发生状态变化所克服的粒子间的相互作用属于同种类型的是( )
A . 食盐和蔗糖熔化
B . 钠和硫熔化
C . 碘和干冰升华
D . 二氧化硅和氧化钠熔化
下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
A . 液溴和己烷分别受热变为气体
B . 干冰和氯化铵分别受热变为气体
C . 硅和铁分别受热熔化
D . 氯化氢和蔗糖分别溶解于水
海洋是元素的摇篮,海水中含有的大量元素在生产、生活、科学研究等多方面具有重要作用。回答下列问题。
-
(1) 写出基态溴原子的价电子排布式,氟、氯、溴、氧四种元素中,电负性由大到小的顺序为(填元素符号) 。
-
(2) Mg、Al的氟化物晶格能分别是2957 kJ•mol-1、5492 kJ•mol-1 , 二者相差很大的原因是。
-
(3) X射线衍射测定等发现,I3AsF6 中存在I
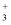 离子。I
离子。I 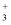 离子的几何构型为,中心原子的杂化类型为。
离子的几何构型为,中心原子的杂化类型为。
-
(4) C原子可以形成多种有机物,如图所示是一种吡啶和一种嘌呤的结构,两种分子中所有原子都在一个平面上。
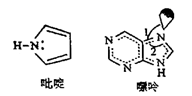
①1mol吡啶分子中含有σ键数目是NA。
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因。
③分子中的大π键可以用符号
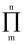 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为  )。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为。
)。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为。 -
(5) CaF2可用于冶金、化工和建材等很多行业,为立方晶胞,结构如下图所示:
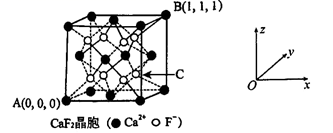
①“ 原子坐标参数”可表示晶胞内部各原子的相对位置,已知A、B两点的原子坐标参数如图所示,则C点的“原子坐标参数”为(,,
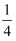 )
)②已知晶胞参数为0.5462 nm,阿伏加德罗常数的值为NA , 则其密度为g•cm-3 (列出计算式即可) 。
下列叙述正确的是( )
A . 化学键存在所有单质和化合物中
B . 化学键的断裂和形成是化学反应能量变化的主要原因
C . 只要有能量变化,则一定发生了化学反应
D . 当反应物的总能量低于生成物的总能量时,该反应放出能量
水电解生成H2和O2 , 水受热汽化成水蒸气。下列说法正确的是( )
A . 前者属化学变化,只破坏分子间作用力
B . H2O比H2S的沸点高是因为水分子间存在氢键
C . 后者属物理变化,破坏了化学键
D . 分子间作用力比化学键强,比氢键弱
铬及其化合物应用广泛。例如用经硫酸酸化处理的三氧化铬(CrO3)硅胶测试司机呼出的气体,根据硅胶颜色的变化可以判断司机是否酒驾。
-
(1) 基态铬原子的电子排布式为。
-
(2) 如图是部分主族元素第一电离能梯度图,图中,a点对应的元素为氢,b、c两点对应的元素分别为、(填元素符号)。

-
(3) 将CrCl3·6H2O溶解在适量水中得到深绿色溶液,溶液中Cr3+以[Cr(H2O)5Cl]2+形式存在。
①上述溶液中,不存在的微粒间作用力是(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
②[Cr(H2O)5Cl]2+中Cr3+的轨道杂化方式不是sp3 , 理由是。
-
(4) 在酸性溶液中,H2O2能与重铬酸盐作用生成蓝色的CrO5 , 离子方程式为:4H2O2+2H+ +Cr2O
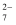 =2CrO5+5H2O根据下图所示Cr2O
=2CrO5+5H2O根据下图所示Cr2O 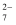 和CrO5的结构判断,上述反应(填“是”或“不是”)氧化还原反应。
和CrO5的结构判断,上述反应(填“是”或“不是”)氧化还原反应。 
下列变化需克服相同类型作用力的是( )
A . 碘和干冰的升华
B . 硅和冰的熔化
C . 氯化氢和氯化钾的溶解
D . 溴和汞的气化
下列说法正确的是( )
A . 分子的稳定性与分子间作用力无关
B . 键长等于成键两原子的半径之和
C . 在可燃冰(CH4•nH2O)中,甲烷分子与水分子之间形成了氢键
D . 凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形
最近更新



